名校
解题方法
1 . 回答下列问题:
(1)已知下列热化学方程式:
①
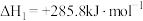
②
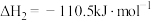
③
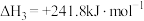
上述反应中属于放热反应的是__________ 。
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为_________ 。
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么 将
将_______ (填“增大”“减小”或“不变”)
(4)反应 的
的
______  。
。
(5) 气态高能燃料乙硼烷
气态高能燃料乙硼烷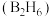 在氧气中燃烧,生成固态三氧化二硼
在氧气中燃烧,生成固态三氧化二硼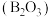 和气态水,释放
和气态水,释放 的热。
的热。
①写出反应的热化学方程式____________ 。
②11.2L(标准状况)气态乙硼烷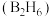 完全燃烧生成液态水生成的热
完全燃烧生成液态水生成的热_______  。
。
(1)已知下列热化学方程式:
①

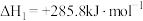
②

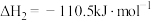
③

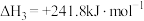
上述反应中属于放热反应的是
(2)①的反应过程是太阳光催化分解水制氢气,该反应中主要能量转化形式为
a.太阳能转化为化学能 b.化学能转化为电能
(3)若反应③使用催化剂,那么
 将
将(4)反应
 的
的
 。
。(5)
 气态高能燃料乙硼烷
气态高能燃料乙硼烷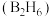 在氧气中燃烧,生成固态三氧化二硼
在氧气中燃烧,生成固态三氧化二硼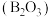 和气态水,释放
和气态水,释放 的热。
的热。①写出反应的热化学方程式
②11.2L(标准状况)气态乙硼烷
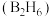 完全燃烧生成液态水生成的热
完全燃烧生成液态水生成的热 。
。
您最近一年使用:0次
2 . 页岩气中含有 、
、 、
、 等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的
等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的 和
和 。
。
(1)去除废气中 的相关热化学方程式如下:
的相关热化学方程式如下:
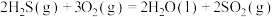
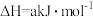
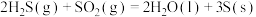

反应 的
的
______ 
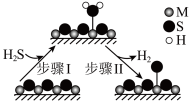
(2)金属硫化物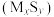 催化反应
催化反应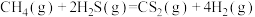 ,既可以除去天然气中的
,既可以除去天然气中的 ,又可以获得
,又可以获得 ,下列说法正确的是______。
,下列说法正确的是______。
(3)通过电化学循环法可将 转化为
转化为 和
和 (如图所示),其中氧化过程发生如下两步反应:
(如图所示),其中氧化过程发生如下两步反应: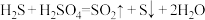 、
、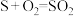 。
。
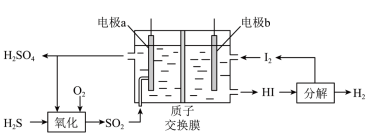
①电极a上发生反应的电极反应式为__________________ 。
②理论上1mol 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为__________________ 。
(4)我国科学家设计了一种 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,装置如下图所示,电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯。
的高效去除,装置如下图所示,电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯。
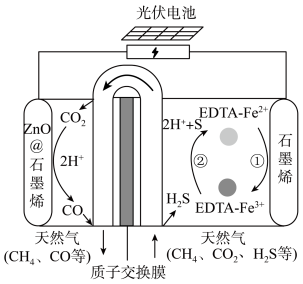
①Zno@石墨烯是______ 极(填“阳”或“阴”)。
②石墨烯电极区发生反应为:
ⅰ.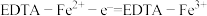
ⅱ.__________________ 。
 、
、 、
、 等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的
等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的 和
和 。
。(1)去除废气中
 的相关热化学方程式如下:
的相关热化学方程式如下: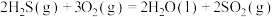
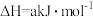
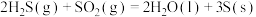

反应
 的
的

(2)金属硫化物
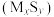 催化反应
催化反应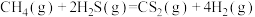 ,既可以除去天然气中的
,既可以除去天然气中的 ,又可以获得
,又可以获得 ,下列说法正确的是______。
,下列说法正确的是______。
A.该反应的 |
B.该反应的平衡常数 |
C.题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的S与催化剂中的M之间发生作用 中带部分负电荷的S与催化剂中的M之间发生作用 |
D.该反应中每消耗1mol ,转移电子的数目约为 ,转移电子的数目约为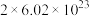 |
(3)通过电化学循环法可将
 转化为
转化为 和
和 (如图所示),其中氧化过程发生如下两步反应:
(如图所示),其中氧化过程发生如下两步反应: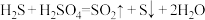 、
、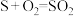 。
。
①电极a上发生反应的电极反应式为
②理论上1mol
 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为(4)我国科学家设计了一种
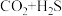 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,装置如下图所示,电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯。
的高效去除,装置如下图所示,电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯。
①Zno@石墨烯是
②石墨烯电极区发生反应为:
ⅰ.
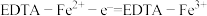
ⅱ.
您最近一年使用:0次
3 . 温室气体让地球“发烧”,倡导低碳生活,是可持续发展的环保责任,将 应用于生产中实现其综合利用是目前的研究热点。回答下列问题:
应用于生产中实现其综合利用是目前的研究热点。回答下列问题:
(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为二甲醚( )也有广泛的应用。
)也有广泛的应用。
反应Ⅰ:
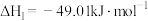
反应Ⅱ:
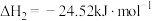
反应Ⅲ:
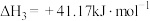
则

______  。
。
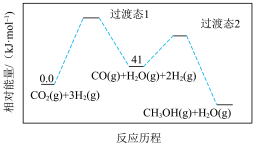
(2)一定条件下, 的反应历程如图所示。该反应的反应速率由第
的反应历程如图所示。该反应的反应速率由第___________ (填“1”或“2”)步决定。
(3)向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,在一定条件下,仅发生上述反应Ⅰ;在甲、乙两种不同催化剂的作用下,反应时间均为
,在一定条件下,仅发生上述反应Ⅰ;在甲、乙两种不同催化剂的作用下,反应时间均为 时,测得甲醇的物质的量分数随温度的变化如图所示。
时,测得甲醇的物质的量分数随温度的变化如图所示。
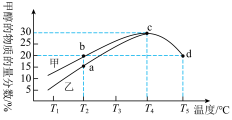
①相同温度下,催化剂效果更好的_______ 是(填“甲”或“乙”);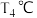 下,甲醇的平均反应速率为
下,甲醇的平均反应速率为________  。
。
② 和
和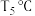 下,平衡常数:
下,平衡常数:
_________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③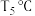 下,反应开始时容器中的总压为
下,反应开始时容器中的总压为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
___________ (只列出计算式,不必化简,气体分压=气体总压×气体的物质的量分数)。
(4)已知 的选择性为
的选择性为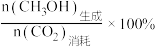 。其他条件相同时,反应温度对
。其他条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如图所示。
的选择性的影响如图所示。
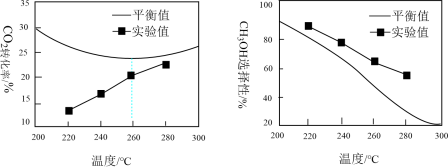
①由上左图可知,实验中反应均未达到化学平衡状态的依据是___________ 。
②由上右图可知,温度相同时 选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是
选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是___________ 。
 应用于生产中实现其综合利用是目前的研究热点。回答下列问题:
应用于生产中实现其综合利用是目前的研究热点。回答下列问题:(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为二甲醚(
 )也有广泛的应用。
)也有广泛的应用。反应Ⅰ:

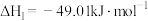
反应Ⅱ:

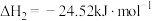
反应Ⅲ:

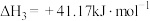
则


 。
。(2)一定条件下,
 的反应历程如图所示。该反应的反应速率由第
的反应历程如图所示。该反应的反应速率由第
(3)向
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,在一定条件下,仅发生上述反应Ⅰ;在甲、乙两种不同催化剂的作用下,反应时间均为
,在一定条件下,仅发生上述反应Ⅰ;在甲、乙两种不同催化剂的作用下,反应时间均为 时,测得甲醇的物质的量分数随温度的变化如图所示。
时,测得甲醇的物质的量分数随温度的变化如图所示。
①相同温度下,催化剂效果更好的
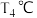 下,甲醇的平均反应速率为
下,甲醇的平均反应速率为 。
。②
 和
和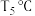 下,平衡常数:
下,平衡常数:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③
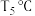 下,反应开始时容器中的总压为
下,反应开始时容器中的总压为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
(4)已知
 的选择性为
的选择性为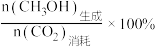 。其他条件相同时,反应温度对
。其他条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如图所示。
的选择性的影响如图所示。
①由上左图可知,实验中反应均未达到化学平衡状态的依据是
②由上右图可知,温度相同时
 选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是
选择性的实验值略高于其平衡值,从化学反应速率的角度解释其原因是
您最近一年使用:0次
4 . 化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是___________(填字母)。
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得: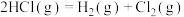 ∆H=
∆H=___________ kJ/mol
②通过盖斯定律可计算。已知在25℃、101kPa时:
I.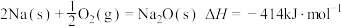
II.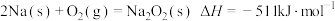
写出Na2O2与Na反应生成Na2O的热化学方程式:___________ 。
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
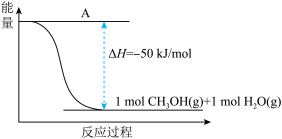
该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H___________ (填“变大”“变小”或“不变”)。
(4)有机物M经过太阳光光照可转化成N,转化过程如下:
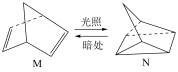
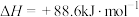
则M、N相比,较稳定的是___________ 。
(1)下列反应中,属于吸热反应的是___________(填字母)。
| A.NaOH与盐酸反应 | B.甲烷的燃烧反应 |
| C.Ba(OH)2∙8H2O与氯化铵反应 | D.锌与盐酸反应 |
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 |  |  |  |
| 键能(kJ/mol) | 436 | 247 | 434 |
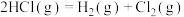 ∆H=
∆H=②通过盖斯定律可计算。已知在25℃、101kPa时:
I.
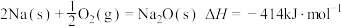
II.
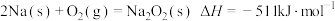
写出Na2O2与Na反应生成Na2O的热化学方程式:
(3)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的∆H
(4)有机物M经过太阳光光照可转化成N,转化过程如下:

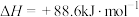
则M、N相比,较稳定的是
您最近一年使用:0次
名校
5 . 温室气体让地球发烧,倡导低碳生活,是一种可持续发展的环保责任,将 应用于生产中实现其综合利用是目前的研究热点。
应用于生产中实现其综合利用是目前的研究热点。
(1)在催化作用下由 和
和 转化为
转化为 的反应历程示意图如下图。
的反应历程示意图如下图。

在合成 的反应历程中,下列有关说法正确的是
的反应历程中,下列有关说法正确的是___________ (填字母)。
a.该催化剂使反应的平衡常数增大
b. 过程中,有
过程中,有 键断裂和
键断裂和 键形成
键形成
c.生成乙酸的反应原子利用率等于100%
d.
(2)以 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
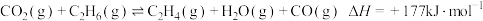 (主反应)
(主反应)
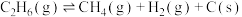
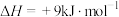 (副反应)
(副反应)
①主反应的反应历程可分为如下两步,反应过程中能量变化如图所示:

i.

ii.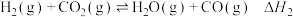

___________ ,主反应的决速步骤为___________ (填“反应i”或“反应ii”)。
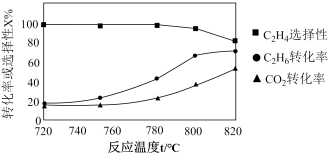
②向恒压密闭容器中充入 和
和 ,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是
,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是___________ 。
 应用于生产中实现其综合利用是目前的研究热点。
应用于生产中实现其综合利用是目前的研究热点。(1)在催化作用下由
 和
和 转化为
转化为 的反应历程示意图如下图。
的反应历程示意图如下图。
在合成
 的反应历程中,下列有关说法正确的是
的反应历程中,下列有关说法正确的是a.该催化剂使反应的平衡常数增大
b.
 过程中,有
过程中,有 键断裂和
键断裂和 键形成
键形成c.生成乙酸的反应原子利用率等于100%
d.

(2)以
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下: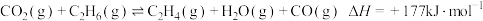 (主反应)
(主反应)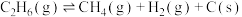
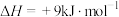 (副反应)
(副反应)①主反应的反应历程可分为如下两步,反应过程中能量变化如图所示:

i.


ii.
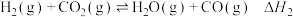

②向恒压密闭容器中充入
 和
和 ,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是
,温度对催化剂K—Fe—Mn/Si—2性能的影响如图所示,工业生产中主反应应选择的温度是
您最近一年使用:0次
名校
解题方法
6 . 氢能是一种理想的绿色能源,一种太阳能两步法甲烷蒸气重整制氢原理合成示意图如下:
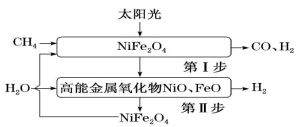
(1)第I步: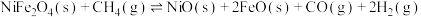
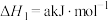 。总反应可表示为:
。总反应可表示为: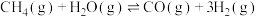
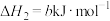 。写出第II步反应的热化学方程式:
。写出第II步反应的热化学方程式:___________ 。
(2)实验测得分步制氢比直接利用 和
和 反应具有更高的反应效率,原因是
反应具有更高的反应效率,原因是________ 。
(3)第I、II步反应的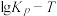 图像如下。
图像如下。
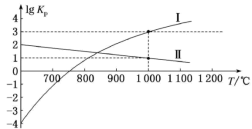
由图像可知a___________ b(填“大于”或“小于”), 时第I步反应平衡时
时第I步反应平衡时 的平衡分压
的平衡分压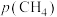
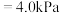 ,则平衡混合气体中
,则平衡混合气体中 的体积分数为
的体积分数为___________ (保留一位小数)。
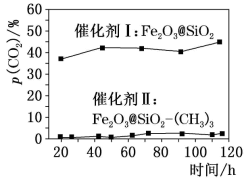
(4)第I步反应产生的合成气(CO和 的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应:
的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应: ,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内
,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内 的分数,据此应选择的催化剂是
的分数,据此应选择的催化剂是___________ (填“I”或“II”),选择的依据是___________ 。

(1)第I步:
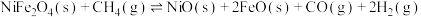
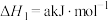 。总反应可表示为:
。总反应可表示为: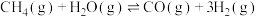
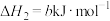 。写出第II步反应的热化学方程式:
。写出第II步反应的热化学方程式:(2)实验测得分步制氢比直接利用
 和
和 反应具有更高的反应效率,原因是
反应具有更高的反应效率,原因是(3)第I、II步反应的
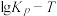 图像如下。
图像如下。
由图像可知a
 时第I步反应平衡时
时第I步反应平衡时 的平衡分压
的平衡分压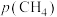
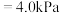 ,则平衡混合气体中
,则平衡混合气体中 的体积分数为
的体积分数为(4)第I步反应产生的合成气(CO和
 的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应:
的混合气体)可用于F—T合成(以合成气为原料在催化剂和适当条件下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应: ,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内
,如下图为相同条件下用不同催化剂在不同时间段测得反应体系内 的分数,据此应选择的催化剂是
的分数,据此应选择的催化剂是
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)已知反应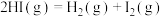 的
的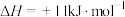 ,1
,1
 、1
、1
 分子中化学键断裂时分别需要吸收436
分子中化学键断裂时分别需要吸收436 、151
、151 的能量,则1
的能量,则1
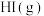 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为___________  。
。
(2)已知:
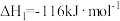

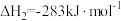

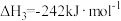
则表示1 气态甲醇完全燃烧生成
气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为___________ 。
(3)25℃时有甲、乙、丙三种溶液,甲为 溶液,乙为
溶液,乙为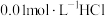 溶液,丙为
溶液,丙为 溶液,请回答下列问题:
溶液,请回答下列问题:
①甲溶液的
___________ 。乙溶液中由水电离出的
___________  。
。
②写出丙的电离方程式___________ 。
③用 的HCl和
的HCl和 两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
___________  (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(4)室温时,向 的醋酸溶液中加入等体积的
的醋酸溶液中加入等体积的 的
的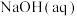 ,充分反应后所得溶液的
,充分反应后所得溶液的 ,所得溶液中
,所得溶液中
___________  。
。
(1)已知反应
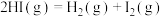 的
的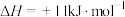 ,1
,1
 、1
、1
 分子中化学键断裂时分别需要吸收436
分子中化学键断裂时分别需要吸收436 、151
、151 的能量,则1
的能量,则1
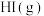 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为 。
。(2)已知:

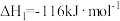

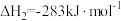

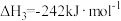
则表示1
 气态甲醇完全燃烧生成
气态甲醇完全燃烧生成 和水蒸气时的热化学方程式为
和水蒸气时的热化学方程式为(3)25℃时有甲、乙、丙三种溶液,甲为
 溶液,乙为
溶液,乙为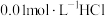 溶液,丙为
溶液,丙为 溶液,请回答下列问题:
溶液,请回答下列问题:①甲溶液的


 。
。②写出丙的电离方程式
③用
 的HCl和
的HCl和 两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(4)室温时,向
 的醋酸溶液中加入等体积的
的醋酸溶液中加入等体积的 的
的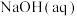 ,充分反应后所得溶液的
,充分反应后所得溶液的 ,所得溶液中
,所得溶液中
 。
。
您最近一年使用:0次
名校
8 . 天然气经 和
和 重整制合成气,再由合成气制备甲醇的相关反应如下:
重整制合成气,再由合成气制备甲醇的相关反应如下:
①主反应: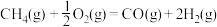
 ;
;
②副反应:
 ;
;
③主反应:
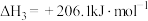
④主反应: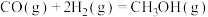
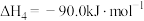 ;
;
⑤主反应: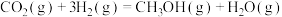
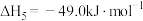 。下列说法不正确的是
。下列说法不正确的是
 和
和 重整制合成气,再由合成气制备甲醇的相关反应如下:
重整制合成气,再由合成气制备甲醇的相关反应如下:①主反应:
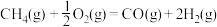
 ;
;②副反应:

 ;
;③主反应:

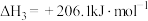
④主反应:
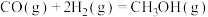
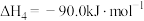 ;
;⑤主反应:
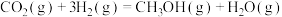
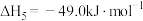 。下列说法不正确的是
。下列说法不正确的是A. 大于 大于 |
| B.反应①为反应③提供能量 |
C.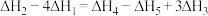 |
D. 为放热反应 为放热反应 |
您最近一年使用:0次
名校
解题方法
9 . 已知: ,
,
 ,
,
 ,
,
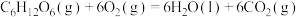 ,
,
下列说法错误的是
 ,
,
 ,
,
 ,
,
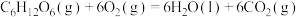 ,
,
下列说法错误的是
A. , , | B.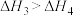 |
C.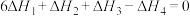 | D. |
您最近一年使用:0次
2023-12-19更新
|
126次组卷
|
2卷引用:福建省福州黎明中学2023-2024学年高二上学期11月期中考试化学试题
名校
10 . Ⅰ.2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知: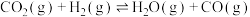
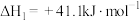

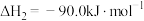
写出 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:___________ 。
(2)250℃,在体积为2.0L的恒容密闭容器中加入 、
、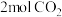 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。
①前10min的平均反应速率
___________  。
。
②下列选项中,能使化学反应速率增大的是___________ (填字母)。
A.增大 的浓度B.减小
的浓度B.减小 的浓度
的浓度
C.降低反应温度D.缩小反应容器体积
Ⅱ.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:实验原理为
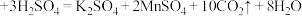 ,实验内容及记录如下:
,实验内容及记录如下:
(3)根据上表中的实验数据,可以得到的结论是___________ 。
(4)忽略混合前后溶液体积的微小变化,实验1在1.5min内的平均反应速率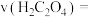
___________  。
。
 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。(1)已知:
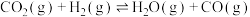
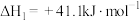

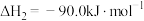
写出
 催化氢化合成甲醇的热化学方程式:
催化氢化合成甲醇的热化学方程式:(2)250℃,在体积为2.0L的恒容密闭容器中加入
 、
、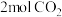 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。①前10min的平均反应速率

 。
。②下列选项中,能使化学反应速率增大的是
A.增大
 的浓度B.减小
的浓度B.减小 的浓度
的浓度C.降低反应温度D.缩小反应容器体积
Ⅱ.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:实验原理为

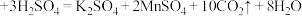 ,实验内容及记录如下:
,实验内容及记录如下:| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液紫色褪去所需时间/min | |||
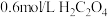 溶液 | H₂O | 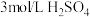 溶液 | 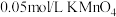 溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
(3)根据上表中的实验数据,可以得到的结论是
(4)忽略混合前后溶液体积的微小变化,实验1在1.5min内的平均反应速率
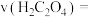
 。
。
您最近一年使用:0次



