1 . 如图是温度和压强对X + Y  2Z 反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z 反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是

 2Z 反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z 反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
| A.上述可逆反应的正反应为吸热反应 |
| B.X、Y、Z均为气态 |
| C.X和Y是气态,Z为固态 |
| D.上述反应的逆反应的△H>0 |
您最近半年使用:0次
名校
2 . 下列图示与对应的叙述相符的是
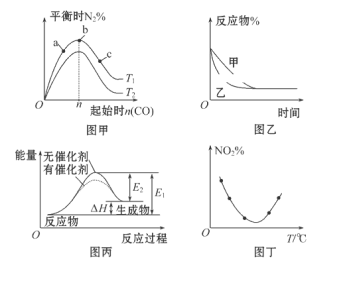

A.图甲表示反应:4CO(g)+2NO2(g)  N2(g)+4CO2(g) ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1<T2 N2(g)+4CO2(g) ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1<T2 |
B.图乙表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(g)的影响,乙的压强比甲的压强小 3C(g)+D(g)的影响,乙的压强比甲的压强小 |
| C.图丙表示的反应是吸热反应,该图表明催化剂能够降低反应的△H值 |
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)  N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H>0 N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H>0 |
您最近半年使用:0次
名校
3 . 已知可逆反应aA(g)+bB(g) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
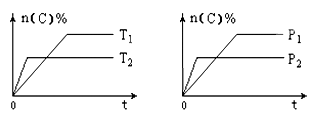
 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是
| A.T1>T2 | B.△H<0 | C.P1>P2 | D.a+b>c+d |
您最近半年使用:0次
名校
4 . 可逆反应aA(s)+bB(g)  cC(g)+dD(g);△H=QkJ/mol,在反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如下图所示:则以下正确的是
cC(g)+dD(g);△H=QkJ/mol,在反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如下图所示:则以下正确的是

 cC(g)+dD(g);△H=QkJ/mol,在反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如下图所示:则以下正确的是
cC(g)+dD(g);△H=QkJ/mol,在反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如下图所示:则以下正确的是
| A.T1>T2,Q>0 |
| B.T2>T1,Q>0 |
| C.P1<P2,a+b=c+d |
| D.P1<P2,b=c+d |
您最近半年使用:0次
5 . 对于可逆反应A(g)+2B(g)⇌2C(g)△H>0,下列图像中正确的是
A.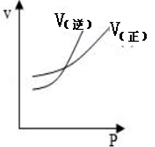 | B.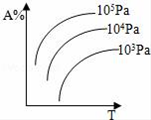 |
C. | D. |
您最近半年使用:0次
2018-11-12更新
|
133次组卷
|
2卷引用:【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高二上学期期中联考化学试题
6 . (一)以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法可以制备四甲基氢氧化铵[(CH3)4NOH],装置如图所示。
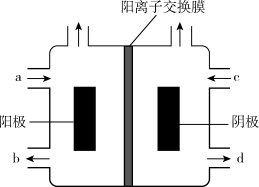
(1)收集到(CH3)4NOH的区域是_______ (填a、b、c或d)。
(2)写出电池总反应_______ 。
(二)乙酸乙酯一般通过乙酸和乙醇酯化合成:CH3COOH(l)+C2H5OH(l)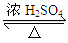 CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
已知纯物质和相关恒沸混合物的常压沸点如下表:
请完成:
(1)关于该反应,下列说法不合理 的是_______ 。
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
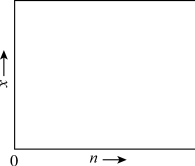
(2)一定温度下该反应的平衡常数K=4.0。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y =_______ ;若乙酸和乙醇的物质的量之比为n : 1,相应平衡体系中乙酸乙酯的物质的量分数为x,请在图中绘制x随n变化的示意图(计算时不计副反应)_______ 。
(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有_______ 。
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g) CH3COOC2H5(g)+2H2(g)
CH3COOC2H5(g)+2H2(g)
在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是_______ 。
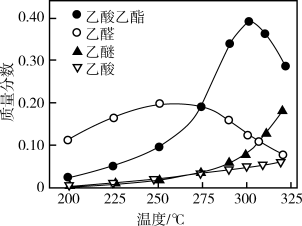
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键

(1)收集到(CH3)4NOH的区域是
(2)写出电池总反应
(二)乙酸乙酯一般通过乙酸和乙醇酯化合成:CH3COOH(l)+C2H5OH(l)
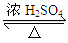 CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1
CH3COOC2H5(l)+H2O(l) ΔH=-2.7kJ·mol-1已知纯物质和相关恒沸混合物的常压沸点如下表:
| 纯物质 | 沸点/℃ | 恒沸混合物(质量分数) | 沸点/℃ |
| 乙醇 | 78.3 | 乙酸乙酯(0.92)+水(0.08) | 70.4 |
| 乙酸 | 117.9 | 乙酸乙酯(0.69)+乙醇(0.31) | 71.8 |
| 乙酸乙酯 | 77.1 | 乙酸乙酯(0.83)+乙醇(0.08) +水(0.09) | 70.2 |
请完成:
(1)关于该反应,下列说法
A.反应体系中硫酸有催化作用
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
(2)一定温度下该反应的平衡常数K=4.0。若按化学方程式中乙酸和乙醇的化学计量数比例投料,则乙酸乙酯的平衡产率y =

(3)工业上多采用乙酸过量的方法,将合成塔中乙酸、乙醇和硫酸混合液加热至110℃左右发生酯化反应并回流,直到塔顶温度达到70~71℃,开始从塔顶出料。控制乙酸过量的作用有
(4)近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g)
 CH3COOC2H5(g)+2H2(g)
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液体收集物中主要产物的质量分数如图所示。关于该方法,下列推测合理的是

A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
您最近半年使用:0次
2018-11-09更新
|
2237次组卷
|
4卷引用:浙江省普通高校招生选考科目2018年4月考试化学试题
浙江省普通高校招生选考科目2018年4月考试化学试题三轮冲刺2020届高三化学考题必刷——有机物制备类探究实验题山东省滕州市第一中学2020届高三3月线上模拟考试化学试题(已下线)专题20.化学反应原理综合应用-十年(2012-2021)高考化学真题分项汇编(浙江专用)
名校
7 . 可逆反应:L(s)+aG(g) bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是
bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是

 bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是
bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是
| A.ΔH<0 |
| B.增加L的物质的量,可提高G的转化率 |
| C.升高温度,G的转化率减小 |
| D.a<b |
您最近半年使用:0次
名校
8 . 下图表示可逆反应 mA(g)+nB(g)  pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是
pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是
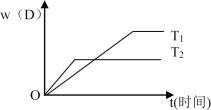
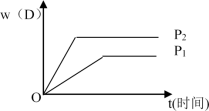
 pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是
pC(g)+qD(g) 在不同温度(T)和压强(P)下生成物D的体积分数w(D)随时间的变化情况。关于上述正反应的判断正确的是 

| A.T1>T2 ,△H<0 | B.T2>T1 ,△H>0 |
| C.P2>P1 ,m+n>p+q | D.P1>P2 ,m+n>p+q |
您最近半年使用:0次
名校
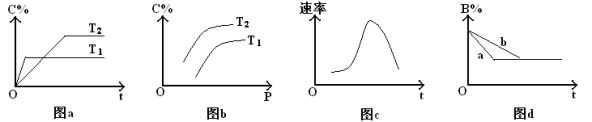
9 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
 pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
| A.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图像,由此说明该反应吸热 |
| D.图d中,若m+n=p,则曲线a一定增大了压强 |
您最近半年使用:0次
2018-10-31更新
|
1102次组卷
|
11卷引用:重庆市铜梁一中2018-2019学年高二上学期10月月考化学试题
重庆市铜梁一中2018-2019学年高二上学期10月月考化学试题河北省唐山市开滦第二中学2019-2020学年高二上学期期中考试化学试题吉林省长春市第151中学2019-2020学年高二上学期期中考试化学试题湖南省娄底市双峰县第一中学2020-2021学年高二上学期9月入学考试化学试题辽宁省黑山县黑山中学2020-2021学年高二10月月考化学试题吉林省长春市第一五一中学2020-2021学年高二上学期第一次月考化学试题(希望班)河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题吉林公主岭范家屯一中2020-2021学年高二上学期期中考试化学试题辽宁省大连市普兰店区第一中学2020-2021学年高二上学期第二阶段考试化学试题吉林省吉林市永吉县第四中学2021-2022学年高二上学期期中考试化学试题云南省保山市腾冲市第八中学2023-2024学年高二下学期开学化学试题
名校
解题方法
10 . 反应mX(g) +nY(g)  pZ(g) 在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间的关系如图所示。下述判断
pZ(g) 在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间的关系如图所示。下述判断
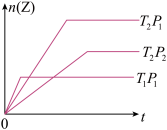
| A.T1<T2 ,P1>P2 |
| B.T1<T2 ,m+n<p |
| C.m+n>p ,正反应放热 |
| D.P1>P2,正反应吸热 |
您最近半年使用:0次
2018-10-31更新
|
206次组卷
|
4卷引用:湖南省醴陵市第二中学2018-2019学年高二上学期第一次月考化学试题



