1 . 以下哪个说法是正确的
| A.同核双原子分子的分子轨道,如果对于分子中心反对称,那么是反键轨道 |
| B.杂化轨道是体系几何构型的反映,它不是真实存在的 |
| C.分子的几何构型可通过计算中心原子的价层电子对数来判断 |
D.根据电子云的重叠形式可以把共价键分成 和 和 成键形式 成键形式 |
您最近一年使用:0次
名校
解题方法
2 . 前四周期原子序数依次增大的六种元素A、B、C、D、E、F 中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D原子的价电子排布式为3d64s2,E原子与D原子的原子序数相差为2。
(1)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式___________ ,黄血盐晶体中各种微粒间的作用力不涉及___________ (填序号)。
A.氢键 B.分子间的作用力 C.金属键
D.配位键 E.离子键 F.共价键
(2)A的简单氢化物的键角比B的简单氢化物键角大,原因是___________ 。
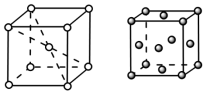
(3)金属C、F晶体的晶胞如图所示(金属C采取体心立方堆积),C、F两种晶体晶胞中金属原子的配位数之比为___________ 。金属F的晶胞中,若设其原子半径为r,晶胞的边长为a,则 r =___________ (用含a的字母表示)。
(1)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式
A.氢键 B.分子间的作用力 C.金属键
D.配位键 E.离子键 F.共价键
(2)A的简单氢化物的键角比B的简单氢化物键角大,原因是
(3)金属C、F晶体的晶胞如图所示(金属C采取体心立方堆积),C、F两种晶体晶胞中金属原子的配位数之比为

您最近一年使用:0次
3 . 下列有关描述正确的是
| A.第一电离能:Be > B > Li |
B.1-溴丁烷的键线式: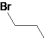 |
C.PCl3的空间填充模型: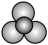 |
| D.Br-的核外电子排布式为:[Ar]4s24p6 |
您最近一年使用:0次
解题方法
4 . 下列说法中不正确的是
| A.ABn型分子中,若中心原子没有孤对电子,则ABn为空间对称结构,属于非极性分子 |
| B.NH3、H2O、CH4分子中的N、O、C原子均是采取sp3杂化的 |
| C.NH3、H2O、CH4分子的几何构型均为三角锥形 |
| D.配合物[Cu(H2O)4]SO4中,中心离子是Cu2+,配体是H2O,配位数是4 |
您最近一年使用:0次
2023-05-10更新
|
190次组卷
|
2卷引用:福建省福州市八县一中2022-2023学年高二下学期7月期末联考化学试题
解题方法
5 . 硼单质及其化合物在生产生活中应用广泛。
(1)离子液体是指室温或接近室温时呈液态,而本身由阴、阳离子构成的化合物,被认为是21世纪理想的绿色溶剂。氯代1-丁基-3-甲基咪唑离子液([bmim]Cl)可以与NH4BF4发生离子交换反应合成离子液体([bmim]BF4),如图所示:

①第二周期中第一电离能介于B与N之间的元素有______ 种;NH4BF4中N原子的杂化方式为______ ,BF 的立体构型为
的立体构型为______ 。
②已知分子或离子中的大π键可以用π 表示,其中m表示参与形成大π键的原子数,n表示大π键中的电子数,则[bmim]+中的大π键可以表示为
表示,其中m表示参与形成大π键的原子数,n表示大π键中的电子数,则[bmim]+中的大π键可以表示为_______ 。
(2)硼酸(H3BO3)是极弱的一元酸,如图为H3BO3晶体的片层结构,同一层内硼酸分子间通过_____ 相结合,层与层之间通过______ 相结合。H3BO3在热水中比冷水中溶解度显著增大的主要原因是______ 。

(3)一种新型轻质储氢材料的晶胞结构如图所示:
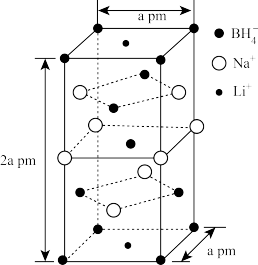
①该化合物的化学式为______ 。
②设阿伏加德罗常数的值为NA,则晶胞的密度为ρ=______ g•cm-3(用含a、NA的代数式表示)。
(1)离子液体是指室温或接近室温时呈液态,而本身由阴、阳离子构成的化合物,被认为是21世纪理想的绿色溶剂。氯代1-丁基-3-甲基咪唑离子液([bmim]Cl)可以与NH4BF4发生离子交换反应合成离子液体([bmim]BF4),如图所示:

①第二周期中第一电离能介于B与N之间的元素有
 的立体构型为
的立体构型为②已知分子或离子中的大π键可以用π
 表示,其中m表示参与形成大π键的原子数,n表示大π键中的电子数,则[bmim]+中的大π键可以表示为
表示,其中m表示参与形成大π键的原子数,n表示大π键中的电子数,则[bmim]+中的大π键可以表示为(2)硼酸(H3BO3)是极弱的一元酸,如图为H3BO3晶体的片层结构,同一层内硼酸分子间通过

(3)一种新型轻质储氢材料的晶胞结构如图所示:

①该化合物的化学式为
②设阿伏加德罗常数的值为NA,则晶胞的密度为ρ=
您最近一年使用:0次
名校
解题方法
6 . 下列化学用语表示不正确的是
A. 的价层电子对互斥模型: 的价层电子对互斥模型: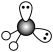 |
B.用原子轨道描述氯化氢分子中化学键的形成: |
C.基态C原子的价层电子轨道表示式: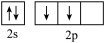 |
D. 的电子式: 的电子式: |
您最近一年使用:0次
2023-05-03更新
|
208次组卷
|
2卷引用:福建省宁德市一级达标校五校联合体2022-2023学年高二下学期4月期中考试化学试题
7 . 观察下列图形,判断下列说法不正确的是
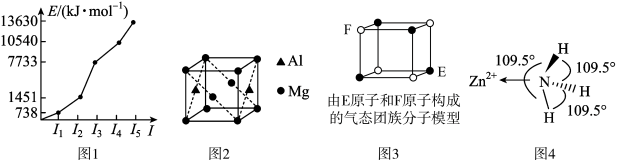

| A.第三周期某元素的前5个电子的电离能如图1所示,该元素是Mg |
| B.铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有8个镁原子最近且等距离 |
| C.某气态团簇分子结构如图3所示,该气态团簇分子的分子式为EF或FE |
| D.图4所示是[Zn(NH3)6]2+的部分结构,其中H-N-H键的键角比NH3的键角大,与NH3中N原子的孤电子对在该配离子中转化为成键电子对有关 |
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题
(1)对于基态Cr原子,下列叙述正确的是_______ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为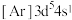
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应键角如图所示。
的空间结构和相应键角如图所示。

 的VSEPR模型为
的VSEPR模型为_______ ; 的沸点比
的沸点比 的
的_______ (填写“高”或“低”),原因是_______ ; 的键角小于
的键角小于 的键角,原因是
的键角,原因是_______ 。
(3) 和NaClO均可作化工生产的氧化剂或氯化剂。制备
和NaClO均可作化工生产的氧化剂或氯化剂。制备 的反应为
的反应为 。
。
①上述方程式中涉及的非金属元素电负性由大到小的顺序是_______ (用元素符号表示)。
②常温时 是一种易溶于
是一种易溶于 的液体,则
的液体,则 分子属于
分子属于_______ 分子(填“极性”或“非极性”)。
③配合物 中心离子
中心离子 的配位数为6,向含
的配位数为6,向含 的溶液中滴加
的溶液中滴加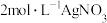 溶液,反应完全后共消耗
溶液,反应完全后共消耗 溶液
溶液 ,则该配合物的化学式为
,则该配合物的化学式为_______ 。
(1)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为
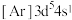
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应键角如图所示。
的空间结构和相应键角如图所示。
 的VSEPR模型为
的VSEPR模型为 的沸点比
的沸点比 的
的 的键角小于
的键角小于 的键角,原因是
的键角,原因是(3)
 和NaClO均可作化工生产的氧化剂或氯化剂。制备
和NaClO均可作化工生产的氧化剂或氯化剂。制备 的反应为
的反应为 。
。①上述方程式中涉及的非金属元素电负性由大到小的顺序是
②常温时
 是一种易溶于
是一种易溶于 的液体,则
的液体,则 分子属于
分子属于③配合物
 中心离子
中心离子 的配位数为6,向含
的配位数为6,向含 的溶液中滴加
的溶液中滴加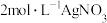 溶液,反应完全后共消耗
溶液,反应完全后共消耗 溶液
溶液 ,则该配合物的化学式为
,则该配合物的化学式为
您最近一年使用:0次
名校
9 . P原子在形成PCl5分子时,3s、3p轨道和1个3d轨道参与形成sp3d杂化,PCl5的空间构型为三角双锥形(如图所示)。下列关于PCl5分子的说法不正确的是
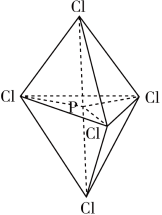

| A.PCl5分子中价电子对数为5 |
B.PCl5分子中没有形成 键 键 |
| C.PCl5分子中所有Cl-P-Cl的键角都相等 |
| D.PCl5晶体融化时不需破坏化学键 |
您最近一年使用:0次
名校
解题方法
10 . 下列粒子的VSEPR模型为四面体形且其空间结构为三角锥形的是
A. | B. | C. | D. |
您最近一年使用:0次
2023-04-16更新
|
117次组卷
|
2卷引用:福建省厦门第二中学2022-2023学年高二下学期4月月考化学试题



