名校
解题方法
1 . 砷化氢(AsH3)是一种无色、可溶于水的气体,其分子构型是三角锥形。下列关于AsH3的叙述中正确的是
| A.AsH3分子中有未成键的电子对 | B.AsH3是非极性分子 |
| C.AsH3是强氧化剂 | D.AsH3分子中的As-H键是非极性键 |
您最近一年使用:0次
2020-11-16更新
|
298次组卷
|
5卷引用:海南省2020届高三下学期新高考线上诊断性测试化学试题
名校
解题方法
2 . Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。5种元素核电荷数之和为54,最外层电子数之和为20。W、Z最外层电子数为6,Z的核电荷数是W的2倍。工业上一般通过电解氧化物的方法获得Y的单质,Y的氧化物有两性。则下列说法不正确的是
| A.原子半径:X>Y>Q>W |
| B.X、Y的氧化物的水化物的碱性:X>Y |
| C.Q和W所形成的分子一定为极性键形成的非极性分子 |
| D.Y和Z的简单离子不能在水中化合形成化合物Y2Z3 |
您最近一年使用:0次
解题方法
3 . 请填写下表:
 | 空间构型 | 杂化方式 | 分子类型(极性或非极性) |
| 二氧化硫 | |||
| 氨气 | |||
| 三氧化硫 |
您最近一年使用:0次
名校
4 . 膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。以下关于PH3的叙述正确的是
| A.PH3分子中有未成键的孤对电子 |
| B.PH3是非极性分子 |
| C.PH3分子的VSEPR模型是三角锥形 |
| D.PH3分子的P-H键是非极性键 |
您最近一年使用:0次
2020-11-01更新
|
269次组卷
|
3卷引用:内蒙古自治区呼伦贝尔市阿荣旗第一中学2019-2020学年高二下学期3月月考化学试题
内蒙古自治区呼伦贝尔市阿荣旗第一中学2019-2020学年高二下学期3月月考化学试题(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记河北省沧州市吴桥县吴桥中学2023-2024学年高二下学期3月月考化学试题
5 . 有关乙烯分子的描述不正确的是
| A.两个碳原子采用sp杂化方式 |
| B.分子中既有极性键又有非极性键 |
| C.分子中既有σ键又有π键 |
| D.乙烯分子为非极性分子 |
您最近一年使用:0次
解题方法
6 . 在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是__________________ ;
(2)实验测得:μ(PF3)=1.03、μ(BF3)=0。由此可知,PF3分子构型是___________________ ,BF3分子构型是 __________________ 。
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,A:棕黄色者μ>0,B:淡黄色者μ=0。在水中溶解度较大的是______________________ (填序号)。
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是
(2)实验测得:μ(PF3)=1.03、μ(BF3)=0。由此可知,PF3分子构型是
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,A:棕黄色者μ>0,B:淡黄色者μ=0。在水中溶解度较大的是
您最近一年使用:0次
名校
解题方法
7 . 下列关于物质结构的命题中,错误的项数有
①乙醛分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为[Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2中阴阳离子个数比不同
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为: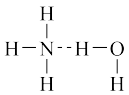
⑦HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
①乙醛分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为[Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2中阴阳离子个数比不同
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为:
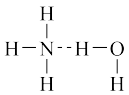
⑦HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
| A.4项 | B.5项 | C.6项 | D.7项 |
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、W四种元素原子的质子数依次增多,W是原子序数最大的短周期主族元素,X与Y形成的化合物M为沼气的主要成分,雷电天气时可形成一种具有杀菌作用的Z单质。下列说法正确的是( )
| A.基态Y、Z、W原子的最高能级均为p能级且能量相同 |
| B.M与W的单质光照时生成的四种有机物均为极性分子 |
| C.M与X2Z两种分子中心原子杂化类型相同 |
| D.酸性:XWZ3>X2YZ3,所以非金属性:W>Y |
您最近一年使用:0次
名校
解题方法
9 . 下列说法中错误的是
| A.SO2、SO3都是极性分子 |
B.在 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.CO可以和很多金属形成配合物,如Ni(CO)2,Ni与CO之间的键型为配位键 |
您最近一年使用:0次
名校
10 . 下列说法正确的是
| A.正四面体分子中键角一定是109º28ˊ |
| B.在分子中,两个成键的原子间的距离叫做键长 |
| C.HCl的键能比HI键能大,说明HCl比HI稳定 |
| D.含有极性键的分子一定是极性分子 |
您最近一年使用:0次



