名校
解题方法
1 . 配位化合物物广泛的应用于物质分离、定量测定.医药、催化等方面。利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O
下列说法正确的是
下列说法正确的是
| A.该配位化合物的配位数为5 |
| B.提供孤电子对的成键原子是N和Cl |
| C.[Co(NH3)5Cl]2+中存在配位键、共价键和离子键 |
| D.氧化剂H2O2是非极性分子 |
您最近一年使用:0次
2020-08-22更新
|
954次组卷
|
10卷引用:山东省菏泽市东明县第一中学2019-2020学年高二期末考试化学试题
山东省菏泽市东明县第一中学2019-2020学年高二期末考试化学试题海南省儋州市第二中学2020-2021学年高二下学期3月月考化学试题山东省聊城市第三中学2021-2022学年高二下学期第一次质量检测化学试题第四节 配合物与超分子湖南省邵东市第一中学2022-2023学年高二上学期第三次月考化学试题(已下线)【知识图鉴】单元讲练测选择性必修2第三章01讲核心(已下线)第五章 物质结构与性质 元素周期律 必做实验提升(五) 简单配合物的形成与制备广东省顺德市(李兆基中学、郑裕彤中学、华侨中学)等2022-2023学年高二下学期4月期中考试化学试题辽宁省葫芦岛市绥中县第一高级中学2022-2023学年高二下学期4月监测化学试题黑龙江省佳木斯市三校联考2023-2024学年高三上学期第三次调研考试化学试题
名校
解题方法
2 . CO2在低压条件下能与H2合成甲醇:CO2+3H2=CH3OH+H2O,该反应所涉及的4种物质中,沸点从高到低的顺序为
| A.H2O>CH3OH>CO2>H2 | B.CH3OH>H2O>CO2>H2 |
| C.H2O>CO2>CH3OH>H2 | D.CH3OH>CO2>H2O>H2 |
您最近一年使用:0次
解题方法
3 . 下列说法错误的是
| A.C3H8 中碳原子都采用sp3 杂化 |
| B.O2、CO2、N2 都是非极性分子 |
| C.酸性:H2CO3<H3PO4<HClO |
D.CO 的一种等电子体为 NO+ ,它的电子式为 |
您最近一年使用:0次
2020-08-21更新
|
137次组卷
|
2卷引用:吉林省松原市扶余市第一中学2019-2020学年高二下学期期中考试化学试题
解题方法
4 . 下列关于O、S及其化合物结构与性质的论述错误的是
| A.O与S的基态原子最高能级均为p能级 | B.H2S与H2O2均为极性分子 |
| C.H2O 分子中的键角小于SO3分子中的键角 | D.键能O-H>S-H,因此H2O的沸点高于H2S |
您最近一年使用:0次
解题方法
5 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W是宇宙中含量最丰富的元素,X是第二周期未成对电子最多的元素,Y最外层有2个未成对电子,其单质常做半导体,Z的第一电离能是同周期主族元素中最大的。下列说法正确的是( )
| A.Y与Z形成的最简单化合物属于非极性分子 |
| B.W与X、Y形成的最简单化合物在水中溶解度:X<Y |
| C.W、X、Y的最高价氧化物沸点最高的是:W的最高价氧化物 |
| D.X、Z的氧化物对应水化物的酸性:X<Z |
您最近一年使用:0次
解题方法
6 . BF3与一定量的水形成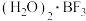 ,一定条件下
,一定条件下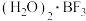 可发生如图转化,下列说法中正确的是
可发生如图转化,下列说法中正确的是

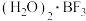 ,一定条件下
,一定条件下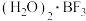 可发生如图转化,下列说法中正确的是
可发生如图转化,下列说法中正确的是
A.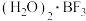 熔化后得到的物质属于离子晶体 熔化后得到的物质属于离子晶体 |
B.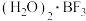 分子之间存在着配位键和氢键 分子之间存在着配位键和氢键 |
| C.H3O+中氧原子为sp3杂化 |
| D.BF3是仅含极性共价键的非极性分子 |
您最近一年使用:0次
2020-08-13更新
|
185次组卷
|
2卷引用:山东省德州市2019-2020学年高二下学期期末考试化学试题
解题方法
7 . 下列各组物质性质的比较,结论不正确的是
| A.分子的极性:异戊烷>新戊烷 |
B.沸点: < <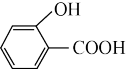 |
C.碳碳键的键长: |
| D.在H2O中的溶解度:CH3CH2Br<CH3CH2OH |
您最近一年使用:0次
8 . 某一化合物分子式为AB2,A属于第VIA族元素,B属于第VIIA族元素,A和B在同一周期,它们的电负性值分别为3.44和3.98。下列推断不正确的是
| A.AB2分子的空间构型为V形 |
| B.A-B键为极性键,AB2分子为非极性分子 |
| C.AB2与水相比,AB2的熔沸点比水的熔沸点低 |
| D.A原子的杂化方式是sp3杂化 |
您最近一年使用:0次
2020高三·全国·专题练习
解题方法
9 . 下列说法正确的是________ 。
①CO2、H2S都属于含极性键的非极性分子
②S2Cl2(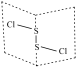 )为含有极性键和非极性键的非极性分子
)为含有极性键和非极性键的非极性分子
③SF6(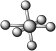 )是由极性键构成的非极性分子
)是由极性键构成的非极性分子
④SO2和NH3均易溶于水,原因之一是它们都是极性分子
⑤CCl4是非极性分子,C原子处在4个Cl原子所组成的正方形的中心
⑥卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大
⑦H2O比H2S稳定是因为水分子间存在氢键
⑧极性分子中可能含有非极性键
⑨HClO2、H2SeO3、H3BO3、HMnO4四种含氧酸中酸性最强的是H3BO3
⑩BF3和NH3化学键的类型和分子的极性(极性或非极性)皆相同
⑪H2O的沸点比HF的沸点高,是由于水中氢键键能大
⑫邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高
①CO2、H2S都属于含极性键的非极性分子
②S2Cl2(
 )为含有极性键和非极性键的非极性分子
)为含有极性键和非极性键的非极性分子③SF6(
 )是由极性键构成的非极性分子
)是由极性键构成的非极性分子④SO2和NH3均易溶于水,原因之一是它们都是极性分子
⑤CCl4是非极性分子,C原子处在4个Cl原子所组成的正方形的中心
⑥卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大
⑦H2O比H2S稳定是因为水分子间存在氢键
⑧极性分子中可能含有非极性键
⑨HClO2、H2SeO3、H3BO3、HMnO4四种含氧酸中酸性最强的是H3BO3
⑩BF3和NH3化学键的类型和分子的极性(极性或非极性)皆相同
⑪H2O的沸点比HF的沸点高,是由于水中氢键键能大
⑫邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高
您最近一年使用:0次
10 . 过硝酸钠(NaNO4)能与水发生反应:NaNO4+H2O=NaNO3+H2O2,下列说法错误的是
| A.过硝酸钠中N表现+5价 |
B.根据VSEPR理论可知: 中心N原子孤电子对数为1 中心N原子孤电子对数为1 |
| C.过硝酸钠中含有“-O-O-”结构 |
| D.H2O2与H2O都属于极性分子 |
您最近一年使用:0次
2020-08-11更新
|
82次组卷
|
2卷引用:山东省青岛胶州市2019-2020学年高二下学期期末考试化学试题



