名校
解题方法
1 . 下列说法正确的是
| A.无机含氧酸分子中有几个氢原子,它就属于几元酸 |
| B.CH4、C2H2、HCN都是含有极性键的非极性分子 |
C. 和CH3-中所有原子都在同一平面 和CH3-中所有原子都在同一平面 |
| D.范德华力:HI>HBr>HCl |
您最近一年使用:0次
名校
解题方法
2 . 在酸性介质中,天然气脱硫原理如图所示。下列说法正确的是
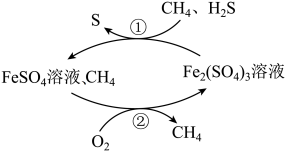

| A.CH4、H2S均属于非极性分子 |
| B.CH4是反应的催化剂 |
| C.过程①使介质溶液酸性增强 |
| D.过程①与过程②转移电子的物质的量之比为1:2 |
您最近一年使用:0次
2020-10-17更新
|
168次组卷
|
2卷引用:山东省高密市2021届高三10月份联考化学试题
名校
解题方法
3 . 标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是
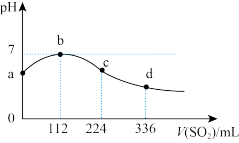

| A.a点对应溶液的导电性比d点强 |
| B.SO2是由极性键形成的非极性分子 |
| C.向d点的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀 |
| D.H2S饱和溶液的物质的量浓度为0.05 mol∙L-1 |
您最近一年使用:0次
解题方法
4 . 焦性没食子酸在气体分析中可用作氧的吸收剂,其结构简式为 ,下列关于焦性没食子酸的说法错误的( )
,下列关于焦性没食子酸的说法错误的( )
 ,下列关于焦性没食子酸的说法错误的( )
,下列关于焦性没食子酸的说法错误的( )| A.所有原子可能共平面 |
| B.含有三种极性共价键 |
| C.熔点高于苯的原因为其键能总和更大 |
| D.相同条件下,在乙醇中的溶解度大于在二硫化碳中的溶解度 |
您最近一年使用:0次
2020-10-04更新
|
242次组卷
|
3卷引用:河北省石家庄市2021届高三上学期质量检测(一)化学试题
名校
解题方法
5 . 为防止新冠肺炎疫情蔓延,防疫人员使用了多种消毒剂进行环境消毒,其中有机化合物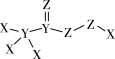 是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力。该化合物中X、Y、Z 为原子序数依次增大的短周期元素。下列叙述不正确的是
是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力。该化合物中X、Y、Z 为原子序数依次增大的短周期元素。下列叙述不正确的是
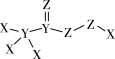 是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力。该化合物中X、Y、Z 为原子序数依次增大的短周期元素。下列叙述不正确的是
是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力。该化合物中X、Y、Z 为原子序数依次增大的短周期元素。下列叙述不正确的是| A.该化合物是既含有极性键又含有非极性键的极性分子 |
| B.该化合物中X、Y、Z的原子半径大小顺序为:Z>Y>X |
| C.三种元素的非金属性强弱顺序为:Z > Y > X |
D.X与Z组成的一种化合物(X2Z2)也是一种“绿色”消毒剂,其电子式为: |
您最近一年使用:0次
2020-09-30更新
|
649次组卷
|
5卷引用:四川省绵阳南山中学2021届高三上学期9月月考理综化学试题
6 . A、B、C均为短周期元素,可形成A2C和BC2两种化合物。A、B、C的原子序数依次递增,A原子的K层的电子数目只有一个,B位于A的下一周期,它的最外层电子数比K层多2个,而C原子核外M层电子数比次外层电子数少2个。
(1)它们的元素符号分别为:A_________ ;B_________ ;C__________ ;
(2)BC2是由______ 键组成的________ (填“极性”或“非极性”)分子。
(3)C原子的外围电子排布式___________ ;
(4)画出B的轨道排布式___________
(1)它们的元素符号分别为:A
(2)BC2是由
(3)C原子的外围电子排布式
(4)画出B的轨道排布式
您最近一年使用:0次
7 . 六氟化硫(SF6)具有良好的高压绝缘性,在电器工业中有着广泛的用途,SF6分子呈正八面体结构,S原子位于正八面体的中心.下列关于SF6的推测中,正确的是( )
| A.SF6在氧气中燃烧可生成SO2 |
| B.SF6是离子化合物 |
| C.SF6是非极性分子 |
| D.SF6中各原子的最外电子层都达到8电子稳定结构 |
您最近一年使用:0次
解题方法
8 . 下列说法错误的是
| A.O2、CO2、N2都是非极性分子 |
B.酸性: |
| C.C3H8中碳原子都采用sp3杂化 |
D.CO的一种等电子体为NO+,它的电子式为 |
您最近一年使用:0次
名校
解题方法
9 . 研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
Ⅰ.利用反应:6NO2+8NH3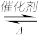 7N2+12H2O处理
7N2+12H2O处理
Ⅱ.一定条件下NO2与SO2可发生反应:NO2(g)+SO2(g) SO3(g)+NO(g)-Q (Q>0)
SO3(g)+NO(g)-Q (Q>0)
Ⅲ.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(1)硫离子的电子结构示意图为_____ ,氨气分子的电子式为______ ,氨气分子属于______ 分子(填“极性”或者“非极性”)。
(2)C、O、S这三种元素中属于同周期元素的非金属性由强到弱的顺序为_____________ ,能证明其递变规律的事实是_______ 。
a.最高价氧化物对应水化物的酸性 b.气态氢化物的沸点
c.单质与氢气反应的难易程度 d.其两两组合形成的化合物中元素的化合价
(3)对于Ⅰ中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均速率v(NO2)=______________ 。
(4)对于Ⅱ中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是______ 。
a.体系压强保持不变 b.NO2浓度保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
Ⅰ.利用反应:6NO2+8NH3
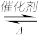 7N2+12H2O处理
7N2+12H2O处理Ⅱ.一定条件下NO2与SO2可发生反应:NO2(g)+SO2(g)
 SO3(g)+NO(g)-Q (Q>0)
SO3(g)+NO(g)-Q (Q>0)Ⅲ.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)(1)硫离子的电子结构示意图为
(2)C、O、S这三种元素中属于同周期元素的非金属性由强到弱的顺序为
a.最高价氧化物对应水化物的酸性 b.气态氢化物的沸点
c.单质与氢气反应的难易程度 d.其两两组合形成的化合物中元素的化合价
(3)对于Ⅰ中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均速率v(NO2)=
(4)对于Ⅱ中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.NO2浓度保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
您最近一年使用:0次
2020-09-20更新
|
610次组卷
|
4卷引用:湖南省湘西土家族苗族自治州花垣县边城高级中学2020-2021学年高二上学期入学考试化学试题
湖南省湘西土家族苗族自治州花垣县边城高级中学2020-2021学年高二上学期入学考试化学试题(已下线)第二章 化学反应速率与化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)辽宁省辽阳市第二高级中学2022-2023学年高二上学期12月月考化学试题河南省周口恒大中学2023-2024学年高二上学期9月月考化学试题
10 . 镍(Ni)、钴(Co) 、钛(Ti)是重要的金属,在材料科学等领域应用广泛。
(1)Ni在元素周期表中的位置是_______ , 其价电子层中有______ 个未成对电子。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属于______ ( 填“极性”“非极性”)分子,其立体构型为_______ 。
(3)铁、钴、镍三种元素并称铁系元素,它们的性质相似。某含镍化合物的结构如图所示,则分子内不可能含有_ (填字母)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键

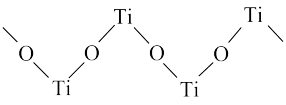
(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式为____ 。阴离子 中硫原子的杂化方式为
中硫原子的杂化方式为________ ,写出一种与 互为等电子体的分子:
互为等电子体的分子:_______ 。
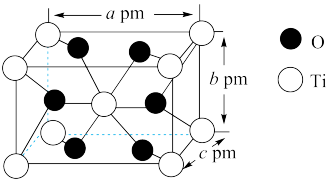
(5)自然界的钛主要以金红石(主要成分为TiO2 )的形式存在。TiO2的晶胞属于四方晶系,其长方体结构如图所示,已知TiO2的摩尔质量为Mg·mol-1,阿伏加 德罗常数的数值为NA,根据图中所示数据可知该晶体的密度ρ=______ (用NA表示阿伏加 德罗常数的数值,用含M、a、b、c、NA的代数式表示)g·cm-3。
(1)Ni在元素周期表中的位置是
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属于
(3)铁、钴、镍三种元素并称铁系元素,它们的性质相似。某含镍化合物的结构如图所示,则分子内不可能含有
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键

(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式为
 中硫原子的杂化方式为
中硫原子的杂化方式为 互为等电子体的分子:
互为等电子体的分子:
(5)自然界的钛主要以金红石(主要成分为TiO2 )的形式存在。TiO2的晶胞属于四方晶系,其长方体结构如图所示,已知TiO2的摩尔质量为Mg·mol-1,阿伏加 德罗常数的数值为NA,根据图中所示数据可知该晶体的密度ρ=

您最近一年使用:0次



