解题方法
1 . 焦亚硫酸钠( )常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的
)常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的 ,制备焦亚硫酸钠,流程如下:
,制备焦亚硫酸钠,流程如下:
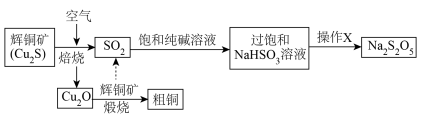
回答下列问题:
(1)焙烧、煅烧之前,辉铜矿要粉碎过筛,其目的是________ 。
(2)“煅烧”中发生反应的化学方程式为________ ,其中 ,还原产物和氧化产物的物质的量之比为________ 。
(3) 转化成
转化成 的离子方程式为
的离子方程式为________ 。
(4)操作X包括蒸发浓缩、________ 、过滤、洗涤、干燥。
(5)探究 的性质。取少量
的性质。取少量 产品溶于水,滴加酸性
产品溶于水,滴加酸性 溶液,振荡,溶液褪色,表明
溶液,振荡,溶液褪色,表明 具有的性质有________(填字母)。
具有的性质有________(填字母)。
(6)为了探究 溶液在空气中的变化情况,小组展开如下研究:
溶液在空气中的变化情况,小组展开如下研究:
查阅资料:常温下, 溶液
溶液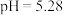 ,
,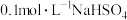 溶液
溶液 ,
, 溶液
溶液 。常温下,取
。常温下,取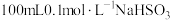 溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
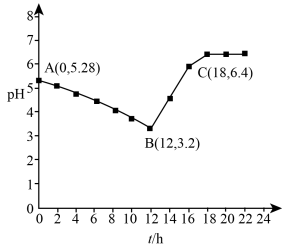
AB段pH降低的主要原因是________ 。B点pH不能降至1.0的主要原因可能是________ (用离子方程式表示)。
 )常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的
)常作食品防腐剂、漂白剂、疏松剂。某小组回收以辉铜矿为原料火法治铜的尾气中的 ,制备焦亚硫酸钠,流程如下:
,制备焦亚硫酸钠,流程如下:
回答下列问题:
(1)焙烧、煅烧之前,辉铜矿要粉碎过筛,其目的是
(2)“煅烧”中发生反应的化学方程式为
(3)
 转化成
转化成 的离子方程式为
的离子方程式为(4)操作X包括蒸发浓缩、
(5)探究
 的性质。取少量
的性质。取少量 产品溶于水,滴加酸性
产品溶于水,滴加酸性 溶液,振荡,溶液褪色,表明
溶液,振荡,溶液褪色,表明 具有的性质有________(填字母)。
具有的性质有________(填字母)。| A.氧化性 | B.还原性 | C.不稳定性 | D.碱性 |
 溶液在空气中的变化情况,小组展开如下研究:
溶液在空气中的变化情况,小组展开如下研究:查阅资料:常温下,
 溶液
溶液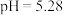 ,
,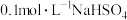 溶液
溶液 ,
, 溶液
溶液 。常温下,取
。常温下,取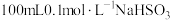 溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
溶液放置某环境下空气中,用pH计测定pH与时间关系如图所示(体积变化忽略不计)。
AB段pH降低的主要原因是
您最近一年使用:0次
名校
2 . 某小组同学制备碘酸盐( )并探究其性质。
)并探究其性质。
资料:① 可与
可与 溶液反应生成
溶液反应生成 和
和 。
。
②碘酸钙 [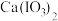 ]为难溶于水、能溶于硝酸的白色固体。
]为难溶于水、能溶于硝酸的白色固体。
③ 的氧化性,
的氧化性, 的还原性与溶液的酸碱性无关:
的还原性与溶液的酸碱性无关: 与氧化性随溶液酸性增强而增强(X为
与氧化性随溶液酸性增强而增强(X为 、
、 或I)。
或I)。
实验装置如图(加热与夹持装置略)
I.打开A中分液漏斗活塞,加热圆底烧瓶;一段时间后,B中溶液由无色变为棕黄色。
II.将B中棕黄色溶液倒入烧杯中,再加入 溶液,烧杯中溶液由棕黄色变为无色。
溶液,烧杯中溶液由棕黄色变为无色。
(1)A装置发生的化学方程式为___________ 。
(2)C装置发生的离子方程式为___________ 。
(3)取少量步骤Ⅱ后所得无色溶液,加入过量盐酸和 ,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下
,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下 可以氧化
可以氧化 为
为 。
。
①乙同学认为上述结论不合理,可能原因如下:
原因一:空气中 在酸性条件下将溶液中的
在酸性条件下将溶液中的 氧化,离子方程式为
氧化,离子方程式为___________ 。
原因二:___________ (填化学式)在酸性条件下将溶液中的 氧化。
氧化。
②为了进一步证明在酸性条件下 可氧化
可氧化 为
为 ,完成如下实验:
,完成如下实验:
ⅰ.另取与(3)等量的步骤Ⅱ后所得无色溶液,加入稍过量 固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。
固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。
ⅱ.向无色溶液X,加入与(3)等量的盐酸和 ,振荡后静置,溶液分层,上、下层均几乎无色。
,振荡后静置,溶液分层,上、下层均几乎无色。
ⅲ.取少量洗涤后的沉淀Y加入稀 ,固体溶解,继续加入少量KI溶液,溶液呈黄色。
,固体溶解,继续加入少量KI溶液,溶液呈黄色。
ⅳ.……
a.由实验ⅰ、ⅱ得出结论:___________ 。
b.由实验ⅲ和ⅳ得出结论:在酸性条件下 可以氧化
可以氧化 为
为 。补全实验ⅳ的操作和现象
。补全实验ⅳ的操作和现象___________ 。
(4)根据实验ⅲ得出:氧化性
___________  (填“
(填“ ”或“
”或“ ”),而实验ⅰ表明
”),而实验ⅰ表明 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
(5)查阅资料发现,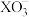 与相应的
与相应的 (
( ,
, )均有类似上述反应。浓度相同时,氧化性
)均有类似上述反应。浓度相同时,氧化性 ,但浓度均为
,但浓度均为 的
的 和
和 开始发生反应时的pH为1,而浓度均为
开始发生反应时的pH为1,而浓度均为 的
的 和
和 开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因
开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因___________ 。
 )并探究其性质。
)并探究其性质。资料:①
 可与
可与 溶液反应生成
溶液反应生成 和
和 。
。②碘酸钙 [
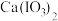 ]为难溶于水、能溶于硝酸的白色固体。
]为难溶于水、能溶于硝酸的白色固体。③
 的氧化性,
的氧化性, 的还原性与溶液的酸碱性无关:
的还原性与溶液的酸碱性无关: 与氧化性随溶液酸性增强而增强(X为
与氧化性随溶液酸性增强而增强(X为 、
、 或I)。
或I)。实验装置如图(加热与夹持装置略)
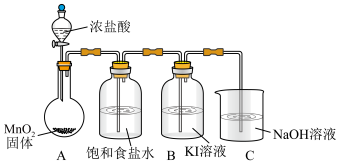
I.打开A中分液漏斗活塞,加热圆底烧瓶;一段时间后,B中溶液由无色变为棕黄色。
II.将B中棕黄色溶液倒入烧杯中,再加入
 溶液,烧杯中溶液由棕黄色变为无色。
溶液,烧杯中溶液由棕黄色变为无色。(1)A装置发生的化学方程式为
(2)C装置发生的离子方程式为
(3)取少量步骤Ⅱ后所得无色溶液,加入过量盐酸和
 ,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下
,振荡后静置,溶液分层,上层呈浅黄色,下层呈紫色。甲同学得出结论:在酸性条件下 可以氧化
可以氧化 为
为 。
。①乙同学认为上述结论不合理,可能原因如下:
原因一:空气中
 在酸性条件下将溶液中的
在酸性条件下将溶液中的 氧化,离子方程式为
氧化,离子方程式为原因二:
 氧化。
氧化。②为了进一步证明在酸性条件下
 可氧化
可氧化 为
为 ,完成如下实验:
,完成如下实验:ⅰ.另取与(3)等量的步骤Ⅱ后所得无色溶液,加入稍过量
 固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。
固体,振荡,充分反应后过滤得到无色溶液X和沉淀Y。ⅱ.向无色溶液X,加入与(3)等量的盐酸和
 ,振荡后静置,溶液分层,上、下层均几乎无色。
,振荡后静置,溶液分层,上、下层均几乎无色。ⅲ.取少量洗涤后的沉淀Y加入稀
 ,固体溶解,继续加入少量KI溶液,溶液呈黄色。
,固体溶解,继续加入少量KI溶液,溶液呈黄色。ⅳ.……
a.由实验ⅰ、ⅱ得出结论:
b.由实验ⅲ和ⅳ得出结论:在酸性条件下
 可以氧化
可以氧化 为
为 。补全实验ⅳ的操作和现象
。补全实验ⅳ的操作和现象(4)根据实验ⅲ得出:氧化性

 (填“
(填“ ”或“
”或“ ”),而实验ⅰ表明
”),而实验ⅰ表明 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是(5)查阅资料发现,
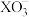 与相应的
与相应的 (
( ,
, )均有类似上述反应。浓度相同时,氧化性
)均有类似上述反应。浓度相同时,氧化性 ,但浓度均为
,但浓度均为 的
的 和
和 开始发生反应时的pH为1,而浓度均为
开始发生反应时的pH为1,而浓度均为 的
的 和
和 开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因
开始发生反应的pH为5。试从原子结构的角度解释两个反应开始发生时pH不同的原因
您最近一年使用:0次
2023-05-01更新
|
856次组卷
|
3卷引用:重庆市万州第二高级中学2023-2024学年高三上学期7月月考化学试题
名校
解题方法
3 . 化学消毒剂能够有效阻断病毒的传播与扩散。本题中,将探讨2种常见的消毒剂:
Ⅰ.二氧化氯 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于 就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
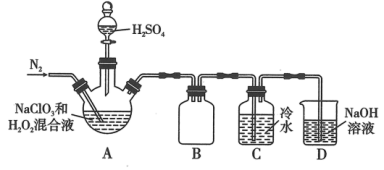
(1)某小组按照文献中制备 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。_______ 。
②装置A中,装 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)测定装置 中
中 溶液的浓度:取
溶液的浓度:取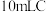 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化(
酸化( ),然后加入
),然后加入_______ 作指示剂,用 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液(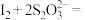 2I-+S4O
2I-+S4O ),当看到
),当看到_______ 现象时,测得标准液消耗的体积为 ,通过计算可知
,通过计算可知 中
中 溶液的浓度为
溶液的浓度为_______  。
。
Ⅱ.84消毒液在生活中有广泛的应用,其主要成分是 和
和 。
。
资料: 的电离常数
的电离常数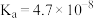 ;
; 的电离常数
的电离常数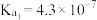 ,
,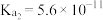 ;
; 的氧化性和杀菌消毒效果强于
的氧化性和杀菌消毒效果强于 。
。
(3)84消毒液溶液呈_______ (填“酸性”或“碱性”)。
(4)84消毒液可由氯气与 溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的
溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的 ,请运用平衡移动原理解释
,请运用平衡移动原理解释 的作用
的作用_______ 。
(5)待消杀物品喷洒上84消毒液后,露置于空气中10~30分钟可增强消毒效果,该过程中发生反应的离子方程式为_______ 。
Ⅰ.二氧化氯
 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于 就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:(1)某小组按照文献中制备
 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。
②装置A中,装
 溶液的仪器名称为
溶液的仪器名称为(2)测定装置
 中
中 溶液的浓度:取
溶液的浓度:取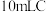 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化(
酸化( ),然后加入
),然后加入 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液(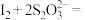 2I-+S4O
2I-+S4O ),当看到
),当看到 ,通过计算可知
,通过计算可知 中
中 溶液的浓度为
溶液的浓度为 。
。Ⅱ.84消毒液在生活中有广泛的应用,其主要成分是
 和
和 。
。资料:
 的电离常数
的电离常数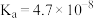 ;
; 的电离常数
的电离常数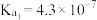 ,
,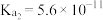 ;
; 的氧化性和杀菌消毒效果强于
的氧化性和杀菌消毒效果强于 。
。(3)84消毒液溶液呈
(4)84消毒液可由氯气与
 溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的
溶液反应制得。为了防止消毒液在存储过程中失效,通常要在84消毒液中残余一定量的 ,请运用平衡移动原理解释
,请运用平衡移动原理解释 的作用
的作用(5)待消杀物品喷洒上84消毒液后,露置于空气中10~30分钟可增强消毒效果,该过程中发生反应的离子方程式为
您最近一年使用:0次
2024-02-04更新
|
62次组卷
|
2卷引用:江苏省无锡市锡东高级中学2023-2024学年高二下学期5月月考化学试题
4 . 某小组探究H2O2氧化性、还原性的变化规律。
资料:Na2O2 + 2H2O=2NaOH+ H2O2、2H2O2=2H2O+O2↑
(1)制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。向A中加入过量稀H2SO4,得溶液B。溶解Na2O2用冰水,目的是_______ 。
(2)检验H2O2:向溶液A、B中分别滴加适量酸性KMnO4溶液。
I:B中产生气泡,滴入的溶液紫色褪去。
 发生还原反应:
发生还原反应:  +5e-+8H+=Mn2+ +4H2O
+5e-+8H+=Mn2+ +4H2O
H2O2发生氧化反应:_______ 。
II: A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1. 有氧化性,能被还原为MnO2;
有氧化性,能被还原为MnO2;
猜想2. Mn2+有_______ 性,能与H2O2反应产生MnO2;
猜想3. ……
(3)探究猜想2的合理性,并分析I中没有产生棕褐色固体的原因,设计实验如下:
注:iii是ii和i的对照实验。
①X是_______ 。(填化学式,下同)
②a是_______ 和_______ ;b是_______ 和_______ 。
③取i中棕褐色固体,滴加浓盐酸,加热,产生黄绿色气体。
(4)向一定浓度的H2O2溶液中加入少量MnO2,迅速产生大量气泡;发生的反应为: 2H2O2 2H2O+O2↑,MnO2 作催化剂;随后加入 H2SO4,固体溶解,气泡产生明显减弱,该过程发生反应的化学方程式为
2H2O+O2↑,MnO2 作催化剂;随后加入 H2SO4,固体溶解,气泡产生明显减弱,该过程发生反应的化学方程式为_______ ,MnO2作氧化剂。
(5)综上所述,H2O2在反应中做氧化剂还是还原剂,与其它反应物的氧化性、还原性以及_______ 等因素有关。
资料:Na2O2 + 2H2O=2NaOH+ H2O2、2H2O2=2H2O+O2↑
(1)制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。向A中加入过量稀H2SO4,得溶液B。溶解Na2O2用冰水,目的是
(2)检验H2O2:向溶液A、B中分别滴加适量酸性KMnO4溶液。
I:B中产生气泡,滴入的溶液紫色褪去。
 发生还原反应:
发生还原反应:  +5e-+8H+=Mn2+ +4H2O
+5e-+8H+=Mn2+ +4H2OH2O2发生氧化反应:
II: A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.
 有氧化性,能被还原为MnO2;
有氧化性,能被还原为MnO2;猜想2. Mn2+有
猜想3. ……
(3)探究猜想2的合理性,并分析I中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 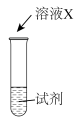 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,滴加浓盐酸,加热,产生黄绿色气体。
(4)向一定浓度的H2O2溶液中加入少量MnO2,迅速产生大量气泡;发生的反应为: 2H2O2
 2H2O+O2↑,MnO2 作催化剂;随后加入 H2SO4,固体溶解,气泡产生明显减弱,该过程发生反应的化学方程式为
2H2O+O2↑,MnO2 作催化剂;随后加入 H2SO4,固体溶解,气泡产生明显减弱,该过程发生反应的化学方程式为(5)综上所述,H2O2在反应中做氧化剂还是还原剂,与其它反应物的氧化性、还原性以及
您最近一年使用:0次
名校
解题方法
5 . 某小组探究Cu和H2O2的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
【实验探究】
实验i:向装有0.5g Cu的烧杯中加入20mL30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)①写出该反应的化学方程式:_______ 。
②电极反应式:
ⅰ.氧化反应:_______ 。
ⅱ.还原反应: H2O2+ 2e- = 2OH-
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是_______ (用化学方程式表示)。
(3)对比实验i和iii,为探究浓氨水对Cu的还原性或H2O2氧化性的影响,该同学利用下图装置继续实验。
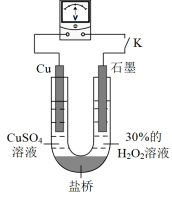
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加浓氨水后,电压减小了y。
c.继续向U型管左侧溶液中滴加浓氨水后,电压增大了z。
①从电极反应角度解释产生现象c的原因:_______ 。
②利用该方法也可证明酸性增强可提高H2O2的氧化性,具体实验操作及现象是_______ 。
(4)总结:物质氧化性和还原性变化的一般规律是_______ 。
【实验探究】
实验i:向装有0.5g Cu的烧杯中加入20mL30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)①写出该反应的化学方程式:
②电极反应式:
ⅰ.氧化反应:
ⅱ.还原反应: H2O2+ 2e- = 2OH-
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
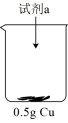 | ii | 20mL30% H2O2与4mL5mol/L H2SO4混合液 | Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30% H2O2与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究浓氨水对Cu的还原性或H2O2氧化性的影响,该同学利用下图装置继续实验。

已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加浓氨水后,电压减小了y。
c.继续向U型管左侧溶液中滴加浓氨水后,电压增大了z。
①从电极反应角度解释产生现象c的原因:
②利用该方法也可证明酸性增强可提高H2O2的氧化性,具体实验操作及现象是
(4)总结:物质氧化性和还原性变化的一般规律是
您最近一年使用:0次
6 . FeSO4溶液放置在空气中容易变质,因此为了方便使用Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)2•6H2O],它比绿矾或绿矾溶液更稳定。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______ 、冷却结晶、过滤、洗涤和干燥后得到一种浅蓝绿色的晶体。
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
【资料1】
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因___________________ 。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:__________________________________________________ 。
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
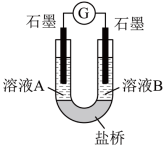
【资料2】原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
【资料3】常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式_________________ 。
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为______ 。
③对比实验_____ 和_____ 还可得出在一定 pH范围内,溶液酸碱性变化是对O2氧化性强弱的影响因素。
④对【资料3】实验事实的解释为____________________ 。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
【资料1】
| 沉淀 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀 pH | 7.6 | 2.7 |
| 完全沉淀 pH | 9.6 | 3.7 |
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
| 序号 | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | 电流计读数 |
| 实验1 | pH=1 | pH=5 | 8.4 |
| 实验2 | pH=1 | pH=1 | 6.5 |
| 实验3 | pH=6 | pH=5 | 7.8 |
| 实验4 | pH=6 | pH=1 | 5.5 |

【资料2】原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
【资料3】常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为
③对比实验
④对【资料3】实验事实的解释为
您最近一年使用:0次
2020-04-02更新
|
346次组卷
|
4卷引用:山东省2020届高三模拟考试化学试题
山东省2020届高三模拟考试化学试题北京市门头沟区2020届高三3月综合练习化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究江苏省昆山中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
7 . FeSO4溶液放置在空气中容易变质,因此为了方便使用 Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)2•6H2O],它比绿矾或绿矾溶液更稳定。(稳定是指物质放置 在空气中不易发生各种化学反应而变质)
I.硫酸亚铁铵晶体的制备与检验
(1)某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都必须煮沸、冷却后再使用,这样处理蒸馏水的目的是_______ 。向 FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______ 、冷却结晶、过滤、洗涤和干燥后得到一 种浅蓝绿色的晶体。
(2)该小组同学继续设计实验证明所制得晶体的成分。
①如图所示实验的目的是_______ ,C 装置的作用是_______ 。
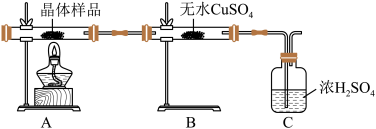
取少量晶体溶于水,得淡绿色待测液。
②取少量待测液,_______ (填操作与现象),证明所制得的晶体中有 Fe2+。
③取少量待测液,经其它实验证明晶体中有NH4+和SO42-
II.实验探究影响溶液中 Fe2+稳定性的因素
(3)配制 0.8 mol/L 的 FeSO4溶液(pH=4.5)和 0.8 mol/L 的(NH4)2Fe(SO4)2溶液(pH=4.0),各取 2 ml 上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加 2 滴 0.01mol/L 的 KSCN 溶液,15 分钟后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液;FeSO4溶液则出现淡黄色浑浊。
【资料 1】
①请用离子方程式解释 FeSO4溶液产生淡黄色浑浊的原因_______ 。
②讨论影响 Fe2+稳定性的因素,小组同学提出以下 3 种假设:
假设 1:其它条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中 Fe2+稳定性较好。
假设 2:其它条件相同时,在一定 pH 范围内,溶液 pH 越小 Fe2+稳定性越好。
假设 3:_______ 。
(4)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分 别控制溶液 A(0.2 mol/L NaCl)和溶液 B(0.1mol/L FeSO4)为不同的 pH,
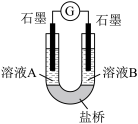
观察记录电流计读数,对假设 2 进行实验研究,实验结果如表所示。
【资料 2】原电池装置中,其它条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原 电池的电流越大。
【资料 3】常温下,0.1mol/L pH=1 的 FeSO4溶液比 pH=5 的 FeSO4溶液稳定性更好。 根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U 形管中左池的电极反应式____________ 。
②对比实验 1 和 2(或 3 和 4) ,在一定 pH 范围内,可得出的结论为____________ 。
③对比实验____________ 和____________ ,还可得出在一定pH 范围内溶液酸碱性变化对 O2氧化性强弱的影响因素。
④ 对【资料 3】实验事实的解释为____________ 。
I.硫酸亚铁铵晶体的制备与检验
(1)某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都必须煮沸、冷却后再使用,这样处理蒸馏水的目的是
(2)该小组同学继续设计实验证明所制得晶体的成分。
①如图所示实验的目的是

取少量晶体溶于水,得淡绿色待测液。
②取少量待测液,
③取少量待测液,经其它实验证明晶体中有NH4+和SO42-
II.实验探究影响溶液中 Fe2+稳定性的因素
(3)配制 0.8 mol/L 的 FeSO4溶液(pH=4.5)和 0.8 mol/L 的(NH4)2Fe(SO4)2溶液(pH=4.0),各取 2 ml 上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加 2 滴 0.01mol/L 的 KSCN 溶液,15 分钟后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液;FeSO4溶液则出现淡黄色浑浊。
【资料 1】
| 沉淀 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 7.6 | 2.7 |
| 完全沉淀pH | 9.6 | 3.7 |
②讨论影响 Fe2+稳定性的因素,小组同学提出以下 3 种假设:
假设 1:其它条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中 Fe2+稳定性较好。
假设 2:其它条件相同时,在一定 pH 范围内,溶液 pH 越小 Fe2+稳定性越好。
假设 3:
(4)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分 别控制溶液 A(0.2 mol/L NaCl)和溶液 B(0.1mol/L FeSO4)为不同的 pH,

观察记录电流计读数,对假设 2 进行实验研究,实验结果如表所示。
| 序号 | A:0.2mol·L-1NaCl | B:0.1mol·L-1FeSO4 | 电流计读数 |
| 实验1 | pH=1 | pH=5 | 8.4 |
| 实验2 | pH=1 | pH=1 | 6.5 |
| 实验3 | pH=6 | pH=5 | 7.8 |
| 实验4 | pH=6 | pH=1 | 5.5 |
【资料 3】常温下,0.1mol/L pH=1 的 FeSO4溶液比 pH=5 的 FeSO4溶液稳定性更好。 根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U 形管中左池的电极反应式
②对比实验 1 和 2(或 3 和 4) ,在一定 pH 范围内,可得出的结论为
③对比实验
④ 对【资料 3】实验事实的解释为
您最近一年使用:0次
2020-04-16更新
|
458次组卷
|
2卷引用:山东省济宁市嘉祥县第一中学2020届高三下学期第三次质量检测化学试题
8 . 交警检验司机是否酒驾时,通常使用酒精检测仪,学习小组分别对酒精检测仪的原理进行探究性学习。
(1)一种传统的酒精检测仪利用乙醇与酸性 溶液的反应进行检测,甲组同学进行模拟实验,向酸性
溶液的反应进行检测,甲组同学进行模拟实验,向酸性 溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现
溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现 在溶液中显绿色,该实验体现乙醇的
在溶液中显绿色,该实验体现乙醇的_______ (填“氧化性”或者“还原性”)
(2)目前常用的是燃料电池型呼气酒精检测仪,其工作原理如图所示,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。
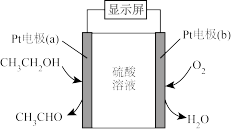
①负极电极反应式为_______ 。
②电池反应为_______ 。
(3)乙组同学设计如下装置(夹持装置省略)进一步探究 催化氧化反应。
催化氧化反应。
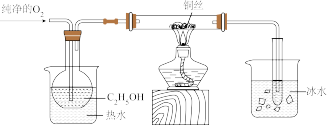
为检验反应产物,该小组同学分别取少量试管中的液体进行了如下实验,回答下列问题:已知:可以用检验葡萄糖的方法检验乙醛。
①热水浴的作用_______ 。
②实验b得出结论依据的现象是_______ 。
③实验a~c中的结论不合理的是_______ (填序号),原因是_______ 。
(1)一种传统的酒精检测仪利用乙醇与酸性
 溶液的反应进行检测,甲组同学进行模拟实验,向酸性
溶液的反应进行检测,甲组同学进行模拟实验,向酸性 溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现
溶液中加入乙醇,溶液由橙色变绿色,查阅资料发现 在溶液中显绿色,该实验体现乙醇的
在溶液中显绿色,该实验体现乙醇的(2)目前常用的是燃料电池型呼气酒精检测仪,其工作原理如图所示,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。

①负极电极反应式为
②电池反应为
(3)乙组同学设计如下装置(夹持装置省略)进一步探究
 催化氧化反应。
催化氧化反应。
为检验反应产物,该小组同学分别取少量试管中的液体进行了如下实验,回答下列问题:已知:可以用检验葡萄糖的方法检验乙醛。
| 实验序号 | 检验试剂和反应条件 | 现象 | 结论 |
| a | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| b | 新制 悬浊液,加热 悬浊液,加热 | _______ | 产物含有乙醛 |
| c | 浅红色含酚酞的 溶液 溶液 | 浅红色褪去 | 产物可能含有乙酸 |
①热水浴的作用
②实验b得出结论依据的现象是
③实验a~c中的结论不合理的是
您最近一年使用:0次
名校
9 . 某兴趣小组为探究浓硫酸与铜的反应,设计了如下装置。_______ 。
(2)为验证品红被 漂白的产物不稳定,简述操作步骤及现象
漂白的产物不稳定,简述操作步骤及现象_______ 。
(3)浸NaOH溶液的棉团作用是_______ 。
(4)为进一步探究 的还原性,将过量的
的还原性,将过量的 通入到200mL1.0mol/L的
通入到200mL1.0mol/L的 和过量
和过量 混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。 产生的原因进行探究(不考虑溶液中
产生的原因进行探究(不考虑溶液中 的影响)
的影响)
①查阅资料 不同浓度的 被还原的产物不同且产物不单一、不同pH时,
被还原的产物不同且产物不单一、不同pH时, 的氧化性不同。1.0mol/L的
的氧化性不同。1.0mol/L的 的
的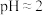 。
。
②提出猜想 猜想1: 被
被 氧化
氧化
猜想2: 在酸性条件下被
在酸性条件下被 氧化
氧化
猜想3:_______
③设计实验、验证猜想
限选实验试剂:0.01mol/LHCl、0.02mol/LHCl、3.0mol/LHNO3、6.0mol/LHNO3、3.0mol/LNaNO3、6.0mol/LNaNO3、0.1mol/LKSCN、 和
和 固体
固体
④交流讨论 小组同学认为,综合上述两个实验不足以证明猜想3成立。
⑤优化实验 若要证明猜想3成立,还要进行实验3。
实验3:_______ (只需提供设计思路,不需要写出具体操作步骤)。

(2)为验证品红被
 漂白的产物不稳定,简述操作步骤及现象
漂白的产物不稳定,简述操作步骤及现象(3)浸NaOH溶液的棉团作用是
(4)为进一步探究
 的还原性,将过量的
的还原性,将过量的 通入到200mL1.0mol/L的
通入到200mL1.0mol/L的 和过量
和过量 混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
 产生的原因进行探究(不考虑溶液中
产生的原因进行探究(不考虑溶液中 的影响)
的影响)①查阅资料 不同浓度的
 被还原的产物不同且产物不单一、不同pH时,
被还原的产物不同且产物不单一、不同pH时, 的氧化性不同。1.0mol/L的
的氧化性不同。1.0mol/L的 的
的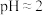 。
。②提出猜想 猜想1:
 被
被 氧化
氧化猜想2:
 在酸性条件下被
在酸性条件下被 氧化
氧化猜想3:
③设计实验、验证猜想
限选实验试剂:0.01mol/LHCl、0.02mol/LHCl、3.0mol/LHNO3、6.0mol/LHNO3、3.0mol/LNaNO3、6.0mol/LNaNO3、0.1mol/LKSCN、
 和
和 固体
固体| 实验步骤 | 实验现象和结论 |
| 实验1:取少量反应后的上层清液于试管中,滴入少量 | 出现 与 与 发生的离子方程式为 发生的离子方程式为 |
实验2:往图中的装置中加入100mL 固体,再通入过量 固体,再通入过量 。 。 | 出现白色沉淀,说明猜想2成立。 |
⑤优化实验 若要证明猜想3成立,还要进行实验3。
实验3:
您最近一年使用:0次
2022-04-29更新
|
1052次组卷
|
7卷引用:四川省泸州市古蔺县金兰高级中学校2022-2023学年高二下学期第一次月考化学试题
四川省泸州市古蔺县金兰高级中学校2022-2023学年高二下学期第一次月考化学试题2024届四川省攀枝花市第十五中学校高三上学期12月第7次半月考理科综合试题-高中化学广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题热点1实验方案设计(已下线)化学-2023年高考押题预测卷03(广东卷)(含考试版、全解全析、参考答案、答题卡)
名校
解题方法
10 . 某小组探究 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
【实验探究】
实验i:向装有0.5g 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:_______ 。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是_______ (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气的原因是_______ 。
(3)对比实验i和iii,为探究氨水对 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
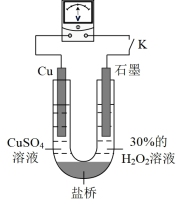
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:_______ 。
②利用该方法也可证明酸性增强可提高 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是_______ 。
(4)总结:物质氧化性和还原性变化的一般规律是_______ 。
(5)应用: 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因_______ 。
 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。【实验探究】
实验i:向装有0.5g
 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。(1)写出该反应的化学方程式:
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
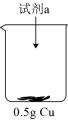 | ii | 20mL30% 与4mL 与4mL5mol/L  混合液 混合液 |  表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30% 与4mL 与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不溶物 表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对
 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:
②利用该方法也可证明酸性增强可提高
 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是(4)总结:物质氧化性和还原性变化的一般规律是
(5)应用:
 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因
您最近一年使用:0次
2022-06-03更新
|
544次组卷
|
4卷引用:北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题
北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题北京市和平街第一中学2021-2022学年高三下学期保温化学试题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)微专题 物质性质综合实验探究



