名校
1 . 氯气常用于自来水的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)写出该反应的化学方程式:_______ ,其中氧化剂和还原剂的物质的量比为_______ 。
(2)若0.1molMnO2和25mL12mol•L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为_______ (不考虑盐酸的挥发)
(3)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
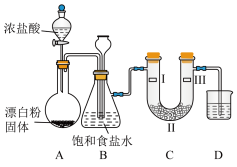
①从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是_______ 。
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:_______ 。
③装置C的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是_______ (填字母)。
④装置D中为NaOH溶液,其作用是_______ ,发生的反应的化学方程式为_______ 。
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中的还原产物是_______ (写化学式),反应中每生成1个ClO2分子,转移电子的数目为_______ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______ (填序号)。
A.O2 B.FeCl2 C.KI D.KMnO4
(1)写出该反应的化学方程式:
(2)若0.1molMnO2和25mL12mol•L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(3)若改用漂白粉与浓盐酸反应制备氯气,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。

①从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
②装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
③装置C的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是
| I | II | III | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中的还原产物是
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
您最近一年使用:0次
2023-10-28更新
|
272次组卷
|
2卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
2 . 下列氧化还原反应方程式,所标电子转移方向与数目不正确的是
A.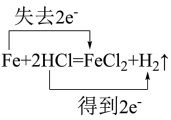 | B. |
C.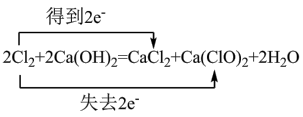 | D. |
您最近一年使用:0次
2023-10-25更新
|
658次组卷
|
34卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题【全国百强校】吉林省实验中学2017-2018学年高二下学期期末考试化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》 第二单元 化学物质及其变化单元测试 A卷河南省安阳市第二中学2018-2019学年高一上学期期中考试化学试题四川省邻水实验学校2018-2019学年高一上学期第三次月考化学试题【全国百强校】四川省成都市七中2018-2019学年高一(理科)上学期半期考试化学试题贵州省贵阳市第六中学2019—2020学年高一上学期期中考试化学试题江西省抚州市临川区第二中学2019-2020学年高一上学期第二次月考化学试题2020届高考化学知识点必练——电子转移的表示方法人教版(2019)高一必修第一册 第一章 物质及其变化 第三节 氧化还原反应 教材帮黑龙江省大庆市大庆中学2020-2021学年高一上学期10月月考化学试题吉林公主岭范家屯一中2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】28高一必修第一册(苏教2019)专题3 第一单元 氯气及氯的化合物1甘肃省张掖市第二中学2020-2021学年高一上学期期中考试化学试题陕西省宝鸡市金台区2021-2022学年高一上学期期中考试化学试题湖南省衡阳市田家炳实验中学2021-2022学年高一上学期期中考试化学试题云南省玉溪市峨山彝族自治县第一中学2021-2022学年高一下学期期中考试化学试题黑龙江省龙西北八校联合体2022-2023学年高一上学期第一次月考化学试题黑龙江省哈尔滨市第七十三中学校2022-2023学年高一上学期第一次月考化学试题陕西省西安市碑林区2022-2023学年高一上学期期中联考化学试题重庆南开中学2022-2023学年高一上学期期中考试化学试题山东省淄博市沂源县第二中学2022-2023学年高一上学期期中考试化学试题湖南省张家界市民族中学2022-2023学年高一上学期第一次月考化学试题北京市中国人民大学附属中学2018-2019学年高一上学期期中考试化学试题新疆维吾尔自治区和田地区洛浦县2022-2023学年高三上学期11月期中考试化学试题河北省石家庄市第二十二中学2023-2024学年高一上学期第一次月考化学试题北京中国人民大学附属中学2023-2024学年高一上学期期中考试化学试题甘肃省武威市凉州区2023-2024学年高一上学期期中考试化学试题山东省新泰市第一中学(弘文部)2023-2024学年高一上学期期中考试化学试题广西南宁市第二中学2023-2024学年高一上学期期中考试化学试题北京汇文中学2023-2024学年高一上学期期中考试化学试题云南省开远市第一中学校2023-2024学年高一上学期期中考试化学试题云南省宣威市东升实验中学2023-2024学年高一上学期11月月考化学试题
名校
解题方法
3 . 下列变化中,必须加入氧化剂才能实现的是
| A.C→CO2 | B.HNO3→NO2 |
| C.CaCO3→CaO | D.CuO→Cu |
您最近一年使用:0次
2023-10-24更新
|
281次组卷
|
3卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
4 . 下列叙述错误的是
| A.大量的钠着火时可以用沙子盖灭,少量的钠应保存在煤油中 |
| B.反应3NO2+H2O=2HNO3+NO中,水既不作氧化剂也不作还原剂 |
| C.将一小块钠投入CuSO4溶液中可置换出红色的固体 |
| D.Na2O在一定条件下能转化成Na2O2 |
您最近一年使用:0次
2023-10-24更新
|
458次组卷
|
3卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
名校
5 . 中华优秀传统文化对人类文明贡献巨大。下列文献的内容中,涉及氧化还原反应的是
| A.“青蒿一握,以水二升渍,绞取汁,尽服之”——《肘后备急方》 |
| B.“用浓酒和糟入甑,蒸令气上,用器承取滴露”——《本草纲目》 |
| C.“曾青得铁则化为铜”——《淮南万毕术》 |
| D.“每金七厘造方寸金一千片”——《天工开物》 |
您最近一年使用:0次
2023-10-23更新
|
295次组卷
|
5卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
6 . 下列物质的分类不正确的是
| A.冰和干冰都属于氧化物 | B. 和 和 都属于酸 都属于酸 |
| C.牛奶和空气都属于混合物 | D.纯碱和熟石灰都属于碱 |
您最近一年使用:0次
2023-10-13更新
|
315次组卷
|
4卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
名校
7 . 某化学兴趣小组利用下列装置制备亚硝酸钠( ),实验装置如图所示。
),实验装置如图所示。

已知:NO和 易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ;
;
回答下列问题:
(1)装置a的名称为_______ 。
(2)试配平装置A中反应的化学方程式:_______ 。
_______Cu+_______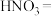 _______
_______ _______
_______ _______
_______
该反应中氧化剂与还原剂的个数比为_______ 。
(3)装置C中浓硫酸的作用是_______ 。
(4)反应开始前打开止水夹K,通入氮气的目的是_______ ;实验结束后,继续通入氮气的目的是_______ 。
(5)装置D中发生的反应为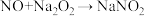 (未配平),每有1个NO参与反应时,转移
(未配平),每有1个NO参与反应时,转移_______ 个电子。
 ),实验装置如图所示。
),实验装置如图所示。
已知:NO和
 易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ;
;回答下列问题:
(1)装置a的名称为
(2)试配平装置A中反应的化学方程式:
_______Cu+_______
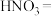 _______
_______ _______
_______ _______
_______该反应中氧化剂与还原剂的个数比为
(3)装置C中浓硫酸的作用是
(4)反应开始前打开止水夹K,通入氮气的目的是
(5)装置D中发生的反应为
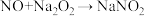 (未配平),每有1个NO参与反应时,转移
(未配平),每有1个NO参与反应时,转移
您最近一年使用:0次
2023-10-10更新
|
329次组卷
|
3卷引用:江西省吉安市井冈山市宁冈中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
8 . 赤铁矿的主要成分为Fe2O3,为测定赤铁矿矿样中铁的百分含量,有如下两种预处理方法:
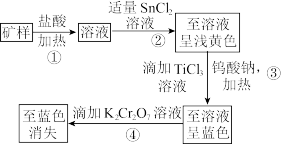
已知:①Sn、Hg、Ti在溶液中存在的形式有Sn2+、Sn4+、Hg2+、H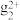 、Ti3+、TiO2+,且Sn2+能与K2Cr2O7反应,而Hg2+不能;氯化汞溶于水,氯化亚汞不溶于水(白色沉淀)。
、Ti3+、TiO2+,且Sn2+能与K2Cr2O7反应,而Hg2+不能;氯化汞溶于水,氯化亚汞不溶于水(白色沉淀)。
②钨酸钠(Na2WO4)可作指示剂,若W(Ⅵ)还原为W(Ⅴ),溶液将呈现蓝色。氧化性:Fe3+>W 。
。
(1)矿样与盐酸反应的主要化学方程式为___________ 。
(2)过程①发生反应的离子方程式为___________ ,过程②产生的沉淀是___________ (填化学式)。
(3)Na2WO4中W的化合价为___________ ,加入指示剂钨酸钠(Na2WO4)的作用是___________ 。
(4)现称取0.2 g矿样进行上述预处理后,加入H2SO4-H3PO4混酸溶液,以二苯胺磺酸钠为指示剂,用重铬酸钾标准溶液滴定,消耗0.0100 mol·L-1的K2Cr2O7标准溶液20.00 mL。
①配平滴定时发生反应的离子方程式: Fe2++
Fe2++ Cr2
Cr2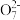 +
+ H+=
H+= Fe3++
Fe3++ Cr3++
Cr3++ H2O
H2O___________ 。
②原矿样中铁的百分含量为___________ ,若矿样预处理后溶液放置过久,对测定结果的影响是___________ (填“偏高”、“偏低”或“无影响”)。

已知:①Sn、Hg、Ti在溶液中存在的形式有Sn2+、Sn4+、Hg2+、H
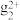 、Ti3+、TiO2+,且Sn2+能与K2Cr2O7反应,而Hg2+不能;氯化汞溶于水,氯化亚汞不溶于水(白色沉淀)。
、Ti3+、TiO2+,且Sn2+能与K2Cr2O7反应,而Hg2+不能;氯化汞溶于水,氯化亚汞不溶于水(白色沉淀)。②钨酸钠(Na2WO4)可作指示剂,若W(Ⅵ)还原为W(Ⅴ),溶液将呈现蓝色。氧化性:Fe3+>W
 。
。(1)矿样与盐酸反应的主要化学方程式为
(2)过程①发生反应的离子方程式为
(3)Na2WO4中W的化合价为
(4)现称取0.2 g矿样进行上述预处理后,加入H2SO4-H3PO4混酸溶液,以二苯胺磺酸钠为指示剂,用重铬酸钾标准溶液滴定,消耗0.0100 mol·L-1的K2Cr2O7标准溶液20.00 mL。
①配平滴定时发生反应的离子方程式:
 Fe2++
Fe2++ Cr2
Cr2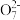 +
+ H+=
H+= Fe3++
Fe3++ Cr3++
Cr3++ H2O
H2O②原矿样中铁的百分含量为
您最近一年使用:0次
名校
解题方法
9 . 从元素化合价和物质类别两个维度学习、研究物质的性质及转化,是一种行之有效的方法。
(1)下图是氮元素的“价-类二维图”的部分信息。

①共价化合物A的化学式___________ (填“一定”或“不一定”)为NH3。
②图中氮的氧化物中,属于酸性氧化物的有___________ 。(用化学式表示)
③工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,写出其化学方程式:___________ 。
(2)目前我国锅炉烟气脱硝技术有新发现,科学家对O3氧化烟气脱硝同时制硝酸进行了实验研究,其生产硝酸的机理如下:
NO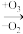 NO2
NO2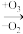 NO3
NO3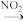 N2O5
N2O5 HNO3。
HNO3。
①NO3分子内存在两个过氧键,且氧均满足8电子稳定结构,NO3中N的化合价为___________ 。
②N2O5与O3作用也能生成NO3与氧气,根据反应前后同种元素价态相同,不参与氧化还原反应的原则,请分析反应N2O5+O3=2NO3+O2中,N2O5的作用是___________ (填“作氧化剂”、“作还原剂”或“既作氧化剂,又作还原剂”)。
③写出在有水存在时,O3与NO以物质的量之比3∶2完全反应的总化学方程式:___________ 。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___________ ,若反应中有0.3 mol 电子发生转移时,生成亚硝酸的质量为___________ g。
(1)下图是氮元素的“价-类二维图”的部分信息。

①共价化合物A的化学式
②图中氮的氧化物中,属于酸性氧化物的有
③工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,写出其化学方程式:
(2)目前我国锅炉烟气脱硝技术有新发现,科学家对O3氧化烟气脱硝同时制硝酸进行了实验研究,其生产硝酸的机理如下:
NO
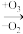 NO2
NO2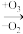 NO3
NO3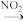 N2O5
N2O5 HNO3。
HNO3。①NO3分子内存在两个过氧键,且氧均满足8电子稳定结构,NO3中N的化合价为
②N2O5与O3作用也能生成NO3与氧气,根据反应前后同种元素价态相同,不参与氧化还原反应的原则,请分析反应N2O5+O3=2NO3+O2中,N2O5的作用是
③写出在有水存在时,O3与NO以物质的量之比3∶2完全反应的总化学方程式:
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 某化学兴趣小组为培养同学们对科学探究的兴趣,设计图1所示实验来探究HS 与Cu2+的反应:
与Cu2+的反应:
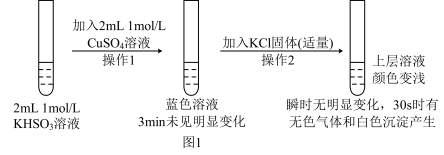
已知:氯化亚铜(CuCl)为白色立方结晶或白色粉末,难溶于水。
(1)将操作2后生成的无色气体通入氯化铁溶液中,___________ (填实验现象),说明该气体为SO2,发生的反应中,氧化剂与还原剂的物质的量之比为___________ 。
(2)操作2后生成的白色沉淀为___________ (填化学式),生成该沉淀和无色气体的反应的离子方程式为___________ 。
(3)根据氧化还原反应的规律,某同学推测操作2中涉及HS 与Cu2+的可逆反应正向进行的原因:外加Cl-导致Cu+的还原性弱于HS
与Cu2+的可逆反应正向进行的原因:外加Cl-导致Cu+的还原性弱于HS ,用图2所示装置(a、b均为石墨电极)进行实验验证。
,用图2所示装置(a、b均为石墨电极)进行实验验证。

①K闭合时,一段时间后指针几乎归零。
②向U形管右管添加___________ ,a电极为___________ 极,产生的现象证实了推测,现象是___________ 。
(4)基于(3)中实验,该同学进一步得出猜想:物质的氧化性和还原性与产物浓度有关,产物浓度越小,对应物质的氧化性或还原性越强。该同学用图2装置再次进行实验,以丰富验证该猜想。与(3)中实验对比,不同的操作是向U形管左管添加___________ 。
 与Cu2+的反应:
与Cu2+的反应:
已知:氯化亚铜(CuCl)为白色立方结晶或白色粉末,难溶于水。
(1)将操作2后生成的无色气体通入氯化铁溶液中,
(2)操作2后生成的白色沉淀为
(3)根据氧化还原反应的规律,某同学推测操作2中涉及HS
 与Cu2+的可逆反应正向进行的原因:外加Cl-导致Cu+的还原性弱于HS
与Cu2+的可逆反应正向进行的原因:外加Cl-导致Cu+的还原性弱于HS ,用图2所示装置(a、b均为石墨电极)进行实验验证。
,用图2所示装置(a、b均为石墨电极)进行实验验证。
①K闭合时,一段时间后指针几乎归零。
②向U形管右管添加
(4)基于(3)中实验,该同学进一步得出猜想:物质的氧化性和还原性与产物浓度有关,产物浓度越小,对应物质的氧化性或还原性越强。该同学用图2装置再次进行实验,以丰富验证该猜想。与(3)中实验对比,不同的操作是向U形管左管添加
您最近一年使用:0次



