解题方法
1 . MnO2可用于制取Cl2和O2。实验室制取纯净、干燥的Cl2的装置如下图。
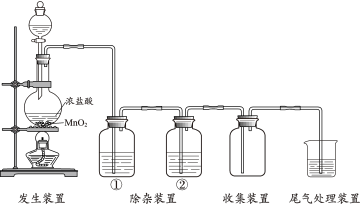
(1)实验室制取Cl2的化学方程式是___________ 。
(2)除杂装置①中的试剂是___________ 。
(3)实验室加热MnO2和KClO3的固体混合物制取O2,同时生成KCl,反应中MnO2是催化剂,化学方程式是___________ 。
(4)在(3)中得到的O2有刺激性气味,推测反应生成了Cl2,反应的化学方程式:2KClO3 + 2MnO2 K2Mn2O8 + Cl2↑+ O2↑。每生成1 mol O2,该反应共转移电子
K2Mn2O8 + Cl2↑+ O2↑。每生成1 mol O2,该反应共转移电子___________ mol。

(1)实验室制取Cl2的化学方程式是
(2)除杂装置①中的试剂是
(3)实验室加热MnO2和KClO3的固体混合物制取O2,同时生成KCl,反应中MnO2是催化剂,化学方程式是
(4)在(3)中得到的O2有刺激性气味,推测反应生成了Cl2,反应的化学方程式:2KClO3 + 2MnO2
 K2Mn2O8 + Cl2↑+ O2↑。每生成1 mol O2,该反应共转移电子
K2Mn2O8 + Cl2↑+ O2↑。每生成1 mol O2,该反应共转移电子
您最近一年使用:0次
2022-01-14更新
|
545次组卷
|
3卷引用:北京市西城区2021-2022学年高一上学期期末考试化学试题
2 . 阅读下面一段材料并回答问题。
维生素C,又称抗坏血酸,化学式为C6H8O6,是一种水溶性的有机化合物。
维生素C具有酸性,在酸性环境中稳定,遇氧气、热、光、碱性物质,特别是有氧化酶及痕量Cu2+、Fe3+等金属离子存在时,可促进其被氧化而破坏。人类不能自身合成维生素C,必须通过食物、药物等摄取,其广泛的食物来源为各类新鲜蔬果。
维生素C具有重要的生理功能,人体缺乏维生素C易引发坏血病、牙龈出血等。维生素C是一种常见的抗氧化剂,能够防止自由基对人体的伤害,从而增强人体抵抗力、延缓衰老等。此外维生素C还可以使Fe元素从+3价转化为+2价,提高肝脏对铁的利用率,从而治疗缺铁性贫血。若短期内服用过量的维生素C,会产生多尿、皮疹等副作用,长期服用过量的维生素C,可能导致草酸及尿酸结石。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)从物质分类看,维生素C属于无机化合物。___________
(2)维生素C具有重要的生理功能,应长期大量服用。___________
(3)维生素C具有抗氧化性是因其具有还原性。___________
(4)生吃新鲜蔬果利于补充维生素C.___________
维生素C,又称抗坏血酸,化学式为C6H8O6,是一种水溶性的有机化合物。
维生素C具有酸性,在酸性环境中稳定,遇氧气、热、光、碱性物质,特别是有氧化酶及痕量Cu2+、Fe3+等金属离子存在时,可促进其被氧化而破坏。人类不能自身合成维生素C,必须通过食物、药物等摄取,其广泛的食物来源为各类新鲜蔬果。
维生素C具有重要的生理功能,人体缺乏维生素C易引发坏血病、牙龈出血等。维生素C是一种常见的抗氧化剂,能够防止自由基对人体的伤害,从而增强人体抵抗力、延缓衰老等。此外维生素C还可以使Fe元素从+3价转化为+2价,提高肝脏对铁的利用率,从而治疗缺铁性贫血。若短期内服用过量的维生素C,会产生多尿、皮疹等副作用,长期服用过量的维生素C,可能导致草酸及尿酸结石。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)从物质分类看,维生素C属于无机化合物。
(2)维生素C具有重要的生理功能,应长期大量服用。
(3)维生素C具有抗氧化性是因其具有还原性。
(4)生吃新鲜蔬果利于补充维生素C.
您最近一年使用:0次
2022-01-14更新
|
244次组卷
|
2卷引用:北京市西城区2021-2022学年高一上学期期末考试化学试题
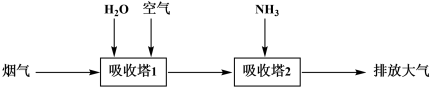
3 . 燃煤、炼钢等过程会产生含有SO2、NO的烟气,为了避免环境污染,研发了多种脱硫脱硝技术。
I活性炭脱硫脱硝技术_______ 。
(2)吸收塔2,在活性炭的催化作用下,烟气中的NO转化为无毒无害的气体排放到大气,该过程体现了NH3具有_______ (填“氧化性”或“还原性”)。
(3)吸收塔1中若SO2去除不彻底,进入吸收塔2,会降低NO的去除率,原因是_______ (写化学方程式)。
II络合吸收法脱硝技术
该技术有2种吸收NO的方法,涉及的反应如下:
方法1:Fe2++NO⇌[Fe(NO)]2+方法2:[FeY]2-+NO⇌[FeY(NO)]2-
已知:[FeY]2-是Fe2+与某有机化合物的阴离子(Y4-)形成的配合物
(4)①方法1,pH过高不利于Fe2+与NO反应,原因是_______ 。
②尽管生产[FeY]2-所需成本比Fe2+高,实际工业生产更多选用方法2吸收NO,可能的原因有_______ (至少写出2个不同角度的原因)。
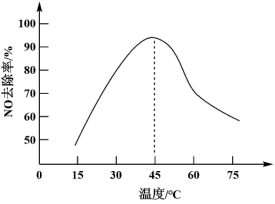
(5)研究温度对反应[FeY]2-(aq)+NO(g)⇌[FeY(NO)]2-(aq)ΔH<0的影响,在相同时间内,测得不同温度下,NO的去除率如图所示:_______ 。
(6)使用锌粉将1L吸收液中浓度为0.04mol·L-1[FeY(NO)]2-转化为[FeY]2-、N2和NH ,实现[FeY]2-的再生。若消耗锌粉0.03mol,测得NH
,实现[FeY]2-的再生。若消耗锌粉0.03mol,测得NH 浓度为0.004mol·L-1,则[FeY]2-的再生率为
浓度为0.004mol·L-1,则[FeY]2-的再生率为_______ 。
I活性炭脱硫脱硝技术
(2)吸收塔2,在活性炭的催化作用下,烟气中的NO转化为无毒无害的气体排放到大气,该过程体现了NH3具有
(3)吸收塔1中若SO2去除不彻底,进入吸收塔2,会降低NO的去除率,原因是
II络合吸收法脱硝技术
该技术有2种吸收NO的方法,涉及的反应如下:
方法1:Fe2++NO⇌[Fe(NO)]2+方法2:[FeY]2-+NO⇌[FeY(NO)]2-
已知:[FeY]2-是Fe2+与某有机化合物的阴离子(Y4-)形成的配合物
(4)①方法1,pH过高不利于Fe2+与NO反应,原因是
②尽管生产[FeY]2-所需成本比Fe2+高,实际工业生产更多选用方法2吸收NO,可能的原因有
(5)研究温度对反应[FeY]2-(aq)+NO(g)⇌[FeY(NO)]2-(aq)ΔH<0的影响,在相同时间内,测得不同温度下,NO的去除率如图所示:
(6)使用锌粉将1L吸收液中浓度为0.04mol·L-1[FeY(NO)]2-转化为[FeY]2-、N2和NH
 ,实现[FeY]2-的再生。若消耗锌粉0.03mol,测得NH
,实现[FeY]2-的再生。若消耗锌粉0.03mol,测得NH 浓度为0.004mol·L-1,则[FeY]2-的再生率为
浓度为0.004mol·L-1,则[FeY]2-的再生率为
您最近一年使用:0次
2022-01-14更新
|
182次组卷
|
2卷引用:北京市丰台区2021-2022学年高三上学期期末考试化学试题
名校
解题方法
4 . 我国的环境空气质量标准中对空气中SO2的浓度限值规定如下表所示。
研究人员测定受污染空气中SO2含量的实验方法如下:用NaOH溶液吸收2m3空气,用0.1mo·L-1硫酸调节pH,然后用I2溶液将其氧化,测得恰好完全反应时消耗I22.54mg。下列推断中,不正确 的是
| 标准等级 | 一级标准 | 二级标准 | 三级标准 |
| 浓度限值(mg·m-3) | 0~0.15 | 0.15~0.50 | 0.50~0.70 |
| A.恰好完全反应时消耗I2的物质的量为1×10-5mol |
| B.反应中转移电子的物质的量为2×10-5mol |
| C.被吸收的空气中SO2的质量为0.64mg |
| D.被测空气样品中SO2的浓度达到了三级标准 |
您最近一年使用:0次
2022-01-14更新
|
1178次组卷
|
7卷引用:北京市海淀区2021-2022学年高一上学期期末参考样题化学试题
名校
解题方法
5 . 自然界的氮循环包括以下过程。下列说法中,不正确 的是

| A.硝化过程中,含氮物质被氧化 |
| B.氨氧化过程中,亚硝态氮元素与铵态氮元素理论物质的量之比为3:4 |
C.N2→ 属于氮的固定,N2发生还原反应 属于氮的固定,N2发生还原反应 |
| D.土壤中Fe2+和Fe3+的存在有利于从与其接触的水体中除去氮元素 |
您最近一年使用:0次
2022-01-14更新
|
2966次组卷
|
22卷引用:北京市海淀区2021-2022学年高一上学期期末参考样题化学试题
北京市海淀区2021-2022学年高一上学期期末参考样题化学试题(已下线)北京市第四中学2021-2022学年高一下学期期中考试化学试题北京市第五十中学2022-2023学年高一下学期期中考试化学试题北京市第十五中学2023-2024学年高一下学期期中考试化学试题北京市怀柔区2023-2024学年第一中学高一上学期期末考试 化学 试题(已下线)章末培优 第5章 化工生产中的重要非金属元素-2021-2022学年高一化学课后培优练(人教版2019必修第二册)黑龙江省双鸭山市第一中学2021-2022学年高二下学期第一次月考化学试题福建省安溪县第一中学2021-2022学年高一下学期第一次月考化学试题山东省济宁市兖州区2021-2022学年高一下学期期中考试化学试题辽宁省辽南协作体2021-2022学年高一下学期期中考试化学试题湖北省重点高中智学联盟2021-2022学年高一下学期5月联考化学试题山东省临沂第一中学2021-2022学年高一下学期6月月考化学试题山西省运城市景胜中学2021-2022学年高一下学期3月月考化学试题新疆生产建设兵团第一师高级中学2022-2023学年高一下学期4月月考化学试题第五章 化工生产中的重要非金属元素(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册) 湖北省仙桃中学2022-2023学年高一上学期10月月考化学试题(已下线)考点巩固卷04 非金属及其化合物(4大考点60题)?-2024年高考化学一轮复习考点通关卷(新高考通用)云南省昆明市第三中学2023-2024学年高二上学期第一次综合测试化学试题宁夏石嘴山第三中学2023-2024学年高三上学期期中考试化学试题(已下线)第五章 化工生产中的重要非金属元素【单元测试B卷】云南省开远市第一中学校2023-2024学年高一下学期3月月考化学试题黑龙江省双鸭山市第一中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
6 . 氧化还原反应可拆分为氧化和还原两个“半反应”。某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是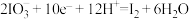 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验[硫酸与浓盐酸中 接近]。
接近]。
②甲是对比实验,目的是排除___________ 的干扰。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在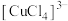 。从氧化还原性的角度分析丙中反应能够发生的原因:
。从氧化还原性的角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。 电极表面有
电极表面有 析出,右侧
析出,右侧 电极周围生成
电极周围生成 。
。
①该装置中右侧 电极作
电极作___________ (填“正”或“负”)极。
②对该原电池的电极反应和总反应的反应类型进行分析,谈谈对原电池工作原理的认识:___________ 。
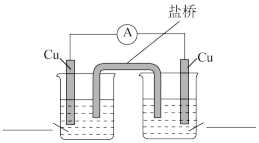
③结合上述实验思考,仅由以下实验用品能否设计成原电池。_____
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表
(选做下列a或b,若两个都作答,按a计分)
a.若不能,说明原因。
b.若能,在如下装置图中填写烧杯中的试剂,并标出电子的移动方向。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
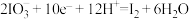 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验[硫酸与浓盐酸中
 接近]。
接近]。| 装置 | 序号 | 试管内药品 | 现象 |
| 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
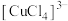 。从氧化还原性的角度分析丙中反应能够发生的原因:
。从氧化还原性的角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
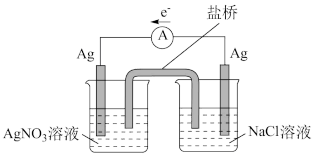
 电极表面有
电极表面有 析出,右侧
析出,右侧 电极周围生成
电极周围生成 。
。①该装置中右侧
 电极作
电极作②对该原电池的电极反应和总反应的反应类型进行分析,谈谈对原电池工作原理的认识:
③结合上述实验思考,仅由以下实验用品能否设计成原电池。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若不能,说明原因。
b.若能,在如下装置图中填写烧杯中的试剂,并标出电子的移动方向。
您最近一年使用:0次
2022-01-14更新
|
541次组卷
|
2卷引用:北京市东城区2021-2022学年高三上学期期末统一检测化学试题
名校
解题方法
7 . 某小组同学分别探究FeCl2溶液、FeCl3溶液的性质。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于___________ ,因此可以与某些碱反应。
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现___________ 性。
(3)预测FeCl2具有还原性,预测依据是___________ ,因此可以与酸性KMnO4溶液反应。
(4)进行如下实验操作:
①i中的现象是___________ ,用化学方程式表示产生该现象的原因:___________ 、___________ 。
②ii中反应的离子方程式是___________ 。
③iii中的现象是___________ 。
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②___________ , 为证实该反应中Fe2+确实被氧化,需要在反应后的溶液中加入试剂___________ ,观察到现象___________ 。
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
(6)iv中反应的离子方程式是___________ 。
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是___________ 。
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到___________ 现象,得出结论:假设b成立。
(9)进一步预测SCN-可能被转化为SO ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象___________ 。
I.探究FeCl2溶液的性质。
(1)从物质类别角度判断FeCl2属于
(2)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现
(3)预测FeCl2具有还原性,预测依据是
(4)进行如下实验操作:
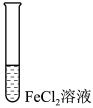 | 序号 | 操作 |
| i | 滴加NaOH溶液 | |
| ii | 加入少量锌粉 | |
| iii | 滴加酸性KMnO4溶液 |
②ii中反应的离子方程式是
③iii中的现象是
(5)某同学认为iii中现象并不能证明Fe2+具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象、②
II.探究FeCl3溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
| 操作 | 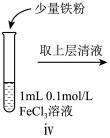 |  | 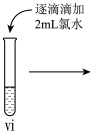 |
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色, 而后红色褪去 |
(7)vi 中滴加氯水过程中,氯水反应的离子方程式是
III.小组同学探究vi中褪色原因,提出两种假设: a.铁离子被转化,b. SCN被转化。
(8)分别向褪色后的溶液中滴加0.1 mol/L FeCl3溶液和KSCN溶液各1滴,观察到
(9)进一步预测SCN-可能被转化为SO
 ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象
您最近一年使用:0次
2022-01-12更新
|
734次组卷
|
5卷引用:北京市昌平区2021-2022学年高一上学期期末考试化学试题
北京市昌平区2021-2022学年高一上学期期末考试化学试题 (已下线)3.1.2 铁盐和亚铁盐-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)广东省广州市第二中学2022-2023学年高一上学期12月月考化学试题9.2.1反应的合理选择(课后)-2019苏教版必修2课前课中课后河南省郑州市第七高级中学2023-2024学年高一上学期12月考试化学试题
8 . 下图是氮在自然界中的循环示意图(部分)。___________ 。实验室用NH4Cl和___________ 反应(写化学式)也可以制备得到氨。
(2)N2在闪电、雨水等作用下转化为HNO3需经历多步反应,写出其中由NO2转化为HNO3的化学方程式___________ 。
(3)写出由氨转化为硝酸铵的化学方程式___________ 。
(4)处理含NH 废水的一种方法如下图所示。
废水的一种方法如下图所示。
NH
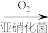 NO
NO
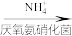 N2
N2
①该工艺中被氧化的微粒是___________ 。
②在上述工艺中,若氧气浓度过高时,NO 会被氧化成NO
会被氧化成NO 。可以通过以下工艺提高氮的脱除率。
。可以通过以下工艺提高氮的脱除率。___________ 。

(2)N2在闪电、雨水等作用下转化为HNO3需经历多步反应,写出其中由NO2转化为HNO3的化学方程式
(3)写出由氨转化为硝酸铵的化学方程式
(4)处理含NH
 废水的一种方法如下图所示。
废水的一种方法如下图所示。NH

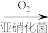 NO
NO
 N2
N2①该工艺中被氧化的微粒是
②在上述工艺中,若氧气浓度过高时,NO
 会被氧化成NO
会被氧化成NO 。可以通过以下工艺提高氮的脱除率。
。可以通过以下工艺提高氮的脱除率。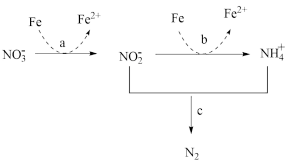
您最近一年使用:0次
名校
9 . 研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
I.以下是硫元素形成的部分物质的价类二维图及相互转化的部分信息。
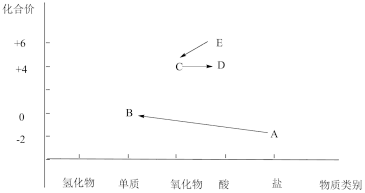
(1)A是一种钠盐,它的电离方程式是___________ 。加入氯水,可完成从A →B的转化,氯水起到的作用是___________ 。
(2)D的化学式是___________ ,写出C →D的化学方程式___________ 。
(3)写出E →C的化学方程式___________ 。
II.双碱法脱除烟气中SO2的过程如下图所示。
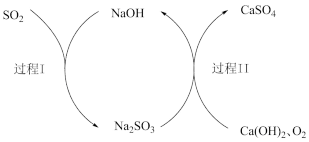
(4)过程I的化学方程式是___________ ,该反应中,含S元素物质发生了类别间的转化,具体来说是___________ 类物质向___________ 类物质的转化。
(5)过程II中含硫元素物质发生了___________ 反应 (填“氧化”或者“还原”),反应中氧化剂是___________ 。 写出该反应的化学方程式___________ 。
(6)该过程中可以循环利用的物质是___________ 。
I.以下是硫元素形成的部分物质的价类二维图及相互转化的部分信息。

(1)A是一种钠盐,它的电离方程式是
(2)D的化学式是
(3)写出E →C的化学方程式
II.双碱法脱除烟气中SO2的过程如下图所示。

(4)过程I的化学方程式是
(5)过程II中含硫元素物质发生了
(6)该过程中可以循环利用的物质是
您最近一年使用:0次
2022-01-12更新
|
213次组卷
|
2卷引用:北京市昌平区2021-2022学年高一上学期期末考试化学试题
解题方法
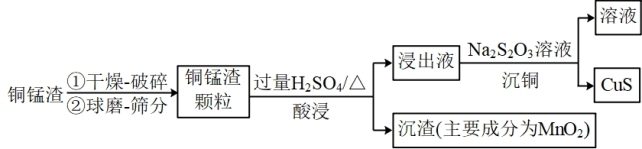
10 . 在回收铜锰渣中的金属资源的流程中,实现铜离子的高效分离是流程的关键。如图是从某铜锰渣(主要成分为Mn3O4、CuMn2O4、ZnMn2O4)中沉铜的流程。
已知:①Na2S2O3+H2O Na2SO4+H2S
Na2SO4+H2S
②3种金属硫化物溶度积
以上为18−25℃的数据,单位省略
(1)上述流程中,破碎、加热等措施的目的是______ 。
(2)酸浸过程中Mn3O4(可看做MnO·Mn2O3)发生了自身氧化还原反应,化学方程式是______ 。
(3)浸出液中存在的离子主要有Mn2+、______ 。
(4)测得某条件下酸浸过程中,铜、锌、锰的浸出率分别为98.14%、98.55%、24.51%,锰浸出率低的原因是______ 。
(5)沉铜过程中发生了反应CuSO4+H2S=CuS↓+H2SO4,该反应的发生不符合“强酸制弱酸”原理,请解释该反应可以发生的原因______ 。
(6)实验证明,只要铜离子过量,MnS、ZnS就会转化为CuS,写出ZnS转化为CuS的离子方程式______ 。

已知:①Na2S2O3+H2O
 Na2SO4+H2S
Na2SO4+H2S②3种金属硫化物溶度积
金属硫化物 | MnS | CuS | ZnS |
溶度积(Ksp) | 2.5×10-13 | 1.3×10-36 | 1.6×10-24 |
(1)上述流程中,破碎、加热等措施的目的是
(2)酸浸过程中Mn3O4(可看做MnO·Mn2O3)发生了自身氧化还原反应,化学方程式是
(3)浸出液中存在的离子主要有Mn2+、
(4)测得某条件下酸浸过程中,铜、锌、锰的浸出率分别为98.14%、98.55%、24.51%,锰浸出率低的原因是
(5)沉铜过程中发生了反应CuSO4+H2S=CuS↓+H2SO4,该反应的发生不符合“强酸制弱酸”原理,请解释该反应可以发生的原因
(6)实验证明,只要铜离子过量,MnS、ZnS就会转化为CuS,写出ZnS转化为CuS的离子方程式
您最近一年使用:0次