解题方法
1 . 以辉锑矿(主要成分为 ,含少量
,含少量 、CuO、
、CuO、 等)为原料制备金属锑的工艺流程如图所示。
等)为原料制备金属锑的工艺流程如图所示。 之外,还含有
之外,还含有 、
、 、
、 等。
等。
下列说法错误的是
 ,含少量
,含少量 、CuO、
、CuO、 等)为原料制备金属锑的工艺流程如图所示。
等)为原料制备金属锑的工艺流程如图所示。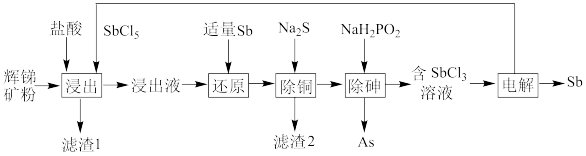
 之外,还含有
之外,还含有 、
、 、
、 等。
等。下列说法错误的是
| A.“还原”过程加适量Sb目的是更好地循环利用Sb元素 |
B.“除铜”时,不宜加过多的 ,是为了防止生成 ,是为了防止生成 或产生有毒物质 或产生有毒物质 |
C.“除砷”时有 生成,该反应每生产2molAs,消耗 生成,该反应每生产2molAs,消耗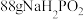 |
| D.“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2 |
您最近一年使用:0次
2 . 回答下列问题。
(1)向含有NaOH和 的混合溶液中缓缓通入
的混合溶液中缓缓通入 直到过量。其现象为开始出现沉淀,后来沉淀逐渐溶解。请按照先后顺序写出相应反应的化学方程式:
直到过量。其现象为开始出现沉淀,后来沉淀逐渐溶解。请按照先后顺序写出相应反应的化学方程式:
①___________ ;
②___________ ;
③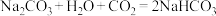 ;
;
④___________ 。
(2)高氯酸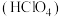 是最强酸。现有一种不常见的氯的化合物叫作高氯酸氯,其分子中氯的质量分数为0.526,且每个分子中含有4个氧原子。
是最强酸。现有一种不常见的氯的化合物叫作高氯酸氯,其分子中氯的质量分数为0.526,且每个分子中含有4个氧原子。
①高氯酸氯的化学式为___________ ,物质类别可归为___________ 。
②高氯酸氯在室温下即发生分解,形成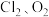 和另一种氯的氧化物。已知该反应的化学方程式中3种产物的化学计量数相同。请写出该分解反应的化学方程式:
和另一种氯的氧化物。已知该反应的化学方程式中3种产物的化学计量数相同。请写出该分解反应的化学方程式:___________ 。
(3)医药上可用石膏来固定骨折部位。石膏有熟石膏(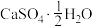 ,一种白色粉末)和生石膏(
,一种白色粉末)和生石膏( ,一种坚硬的固体)两种,固定骨折的石膏是
,一种坚硬的固体)两种,固定骨折的石膏是___________ (填化学式)。固定时发生反应的化学方程式为___________ 。
(4)CO与 溶液反应产生黑色金属钯粉末(反应中有水参加),用此来检测CO对环境的污染情况,此反应的化学方程式为
溶液反应产生黑色金属钯粉末(反应中有水参加),用此来检测CO对环境的污染情况,此反应的化学方程式为___________ ,反应中可能看到的现象是___________ 。
(1)向含有NaOH和
 的混合溶液中缓缓通入
的混合溶液中缓缓通入 直到过量。其现象为开始出现沉淀,后来沉淀逐渐溶解。请按照先后顺序写出相应反应的化学方程式:
直到过量。其现象为开始出现沉淀,后来沉淀逐渐溶解。请按照先后顺序写出相应反应的化学方程式:①
②
③
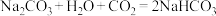 ;
;④
(2)高氯酸
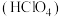 是最强酸。现有一种不常见的氯的化合物叫作高氯酸氯,其分子中氯的质量分数为0.526,且每个分子中含有4个氧原子。
是最强酸。现有一种不常见的氯的化合物叫作高氯酸氯,其分子中氯的质量分数为0.526,且每个分子中含有4个氧原子。①高氯酸氯的化学式为
②高氯酸氯在室温下即发生分解,形成
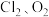 和另一种氯的氧化物。已知该反应的化学方程式中3种产物的化学计量数相同。请写出该分解反应的化学方程式:
和另一种氯的氧化物。已知该反应的化学方程式中3种产物的化学计量数相同。请写出该分解反应的化学方程式:(3)医药上可用石膏来固定骨折部位。石膏有熟石膏(
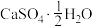 ,一种白色粉末)和生石膏(
,一种白色粉末)和生石膏( ,一种坚硬的固体)两种,固定骨折的石膏是
,一种坚硬的固体)两种,固定骨折的石膏是(4)CO与
 溶液反应产生黑色金属钯粉末(反应中有水参加),用此来检测CO对环境的污染情况,此反应的化学方程式为
溶液反应产生黑色金属钯粉末(反应中有水参加),用此来检测CO对环境的污染情况,此反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过如下实验流程制得:
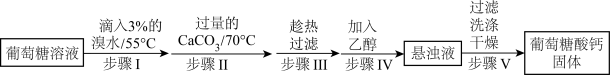
已知:a.反应原理: 。
。
b.相关物质的溶解性如下表:
c.相关物质的酸性:氢溴酸>葡萄糖酸>碳酸。
回答下列问题:
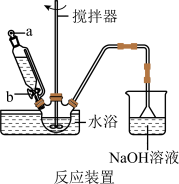
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是___________ ,恒压滴液漏斗使用时需要打开的活塞或玻璃塞是___________ (填“a”“b”或“a和b”)。烧杯中 溶液水浴的作用是
溶液水浴的作用是___________ 。
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
(3)步骤Ⅱ中加入过量的 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为___________ 。加入过量的 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是___________ 。
(4)洗涤操作中最合适的洗涤剂是___________ (填序号),理由是___________ 。
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:___________ (填序号,操作步骤不可重复使用)。
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出
④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液

已知:a.反应原理:
 。
。b.相关物质的溶解性如下表:
| 物质的名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 极易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 |
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是
 溶液水浴的作用是
溶液水浴的作用是
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
A.新制 悬浊液 悬浊液 | B.酸性 溶液 溶液 |
C. /葡萄糖氧化酶 /葡萄糖氧化酶 | D. 溶液 溶液 |
(3)步骤Ⅱ中加入过量的
 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是(4)洗涤操作中最合适的洗涤剂是
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入
 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入
 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
您最近一年使用:0次
名校
解题方法
4 . 酸性高锰酸钾氧化H2O2的离子方程式为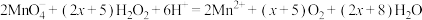 。与该反应有关的说法正确的是
。与该反应有关的说法正确的是
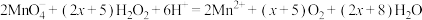 。与该反应有关的说法正确的是
。与该反应有关的说法正确的是A.H2O2的球棍模型为 |
B.O2的电子式为: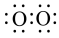 |
C.基态Mn2+价电子的轨道表示式为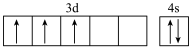 |
D.标准状况下收集到56LO2时,最多消耗 |
您最近一年使用:0次
2024-03-27更新
|
874次组卷
|
3卷引用:山东省济南市2023-2024学年高三下学期3月模拟(一模)考试化学试题
解题方法
5 . 硫酸盐还原菌( )会腐蚀许多金属及合金。模拟
)会腐蚀许多金属及合金。模拟 诱导腐蚀碳素钢发生厌氧电化学腐蚀实验,实验后发现碳素钢表面覆盖物成分是硫化物(主要含
诱导腐蚀碳素钢发生厌氧电化学腐蚀实验,实验后发现碳素钢表面覆盖物成分是硫化物(主要含 ),腐蚀机理如图所示。下列说法正确的是
),腐蚀机理如图所示。下列说法正确的是
 )会腐蚀许多金属及合金。模拟
)会腐蚀许多金属及合金。模拟 诱导腐蚀碳素钢发生厌氧电化学腐蚀实验,实验后发现碳素钢表面覆盖物成分是硫化物(主要含
诱导腐蚀碳素钢发生厌氧电化学腐蚀实验,实验后发现碳素钢表面覆盖物成分是硫化物(主要含 ),腐蚀机理如图所示。下列说法正确的是
),腐蚀机理如图所示。下列说法正确的是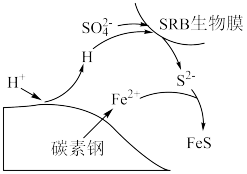
A.碳素钢厌氧腐蚀过程中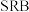 做还原剂 做还原剂 |
B.温度越高,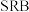 诱导碳素钢厌氧腐蚀速率越快 诱导碳素钢厌氧腐蚀速率越快 |
C.碳作负极,电极反应为: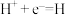 |
D.该实验生成 的总反应: 的总反应: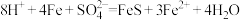 |
您最近一年使用:0次
2024-03-26更新
|
471次组卷
|
4卷引用:2024届四川省大数据学考联盟高三第一次质量检测理科综合试题-高中化学
2024届四川省大数据学考联盟高三第一次质量检测理科综合试题-高中化学(已下线)通关练09 重温“两池”原理及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题04?化学反应机理、历程、能垒图分析(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
6 . 综合利用软锰矿(主要含 ,还有少量
,还有少量 、
、 、MgO、CaO、
、MgO、CaO、 )和硫铁矿(主要含
)和硫铁矿(主要含 )回收
)回收 的工艺流程如图所示:
的工艺流程如图所示:
请回答下列问题:
(1)“酸浸”时将矿石粉碎,主要目的是___________ 。
(2)浸渣1中除 和S外,还有
和S外,还有___________ (填化学式)。S是 分别与
分别与 、
、 反应产生的,其中
反应产生的,其中 与
与 反应的离子方程式为
反应的离子方程式为___________
(3)当离子浓度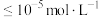 时,可视为沉淀完全,则“除铁铝”时应控制
时,可视为沉淀完全,则“除铁铝”时应控制
___________ (保留两位有效数字)。
(4)“氟化除杂”时除钙的离子反应的平衡常数
___________ (保留两位有效数字)。“转化”时发生反应的离子方程式为___________ 。
(5)氟化钙的晶胞结构如图所示: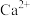 周围最近且距离相等的
周围最近且距离相等的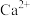 个数为
个数为___________ ,若晶体密度为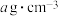 ,用
,用 表示阿伏加德罗常数的值,则晶体中
表示阿伏加德罗常数的值,则晶体中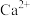 与
与 间的最近距离为
间的最近距离为___________ cm(用含 、
、 的代数式表示)。
的代数式表示)。
 ,还有少量
,还有少量 、
、 、MgO、CaO、
、MgO、CaO、 )和硫铁矿(主要含
)和硫铁矿(主要含 )回收
)回收 的工艺流程如图所示:
的工艺流程如图所示:
| 物质 |  | 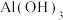 |  |  |  |  |  |
 |  | 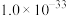 |  | 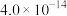 | 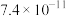 | 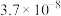 | 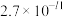 |
(1)“酸浸”时将矿石粉碎,主要目的是
(2)浸渣1中除
 和S外,还有
和S外,还有 分别与
分别与 、
、 反应产生的,其中
反应产生的,其中 与
与 反应的离子方程式为
反应的离子方程式为(3)当离子浓度
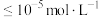 时,可视为沉淀完全,则“除铁铝”时应控制
时,可视为沉淀完全,则“除铁铝”时应控制
(4)“氟化除杂”时除钙的离子反应的平衡常数

(5)氟化钙的晶胞结构如图所示:
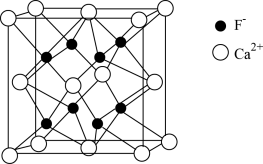
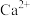 周围最近且距离相等的
周围最近且距离相等的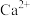 个数为
个数为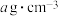 ,用
,用 表示阿伏加德罗常数的值,则晶体中
表示阿伏加德罗常数的值,则晶体中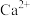 与
与 间的最近距离为
间的最近距离为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-03-26更新
|
387次组卷
|
3卷引用:2024届河南省焦作市普通高中高三上学期第一次模拟考试理科综合试题-高中化学
2024届河南省焦作市普通高中高三上学期第一次模拟考试理科综合试题-高中化学(已下线)压轴题11?无机化工流程综合分析(6大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届河南省禹州市高级中学高三下学期综合考试(1)理综试题-高中化学
7 . 为了减少污染和合理使用资源,某厂计划与氯碱厂、甲醇厂进行联合生产。设计的联合生产的工艺流程如图所示(FeTiO3中Ti为+4价)。下列叙述正确的是
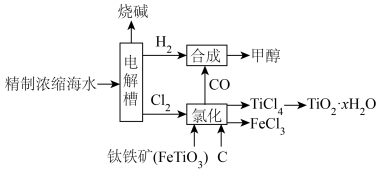
| A.在电解槽中阳极常用铁作电极材料 |
| B.“氯化”反应中氧化剂与CO的物质的量之比为7∶6 |
| C.“合成”甲醇的反应不符合绿色化学中的原子经济性原则 |
| D.利用TiCl4水解制TiO2·xH2O时,应加强热以促进水解 |
您最近一年使用:0次
名校
8 . 为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。后者常采用 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是(
,下列说法不正确的是( 为阿伏加德罗常数)
为阿伏加德罗常数)
 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是(
,下列说法不正确的是( 为阿伏加德罗常数)
为阿伏加德罗常数)| A.氧化产物与还原产物的质量比为3∶4 | B.生成 水转移电子的数目为 水转移电子的数目为 |
C.可使用 溶液吸收氮氧化物 溶液吸收氮氧化物 | D.氮氧化物的排放可形成酸雨 |
您最近一年使用:0次
解题方法
9 . NaBH4是常用络合型氢化物,常温下为白色结晶粉末,具有吸湿性,在干燥空气中可以稳定存在,溶于水、液氨、胺类等。制备方法:
步骤1酯化 反应装置内按化学计量加入H3BO3和CH3OH,在54℃回流2h之后,开始收集B(OCH3)3(硼酸三甲酯)与CH3OH的共沸物,控制温度54℃~55℃。共沸液经硫酸酸洗后进行精馏,得到硼酸三甲酯
步骤2氢化 将金属钠分散于石蜡油中,通入氢气合成氢化钠
步骤3缩合 硼酸三甲酯和氢化钠在石蜡油介质中反应合成硼氢化钠,将物料冷却至100℃以下,进行离心分离得到硼氢化钠滤饼粗品。
步骤4水解 将上述硼氢化钠滤饼粗品置于容器中加水,发生反应NaOCH3+H2O=NaOH+CH3OH;将此水溶液离心分离,清液送入分层器,静置1h后分层。得到硼氢化钠碱性水溶液。
(1)已知电负性B<H,硼氢化钠与水反应生成NaBO2,反应的化学方程式为______ 。
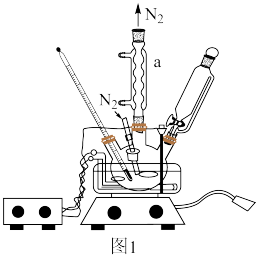
(2)步骤1中,硫酸的作用_______ ,步骤3可在如图1所示装置中进行,仪器a的名称______ ,反应进行前通入氮气的目的是_______ ,步骤4中,硼氢化钠能够稳定存在的原因______ 。
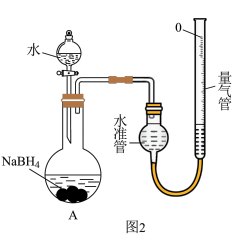
(3)NaBH4溶液浓度可采用如下方法测定(装置如图2所示):25℃,常压下,用移液管移取2.00mL的)NaBH4溶液于烧瓶中,记录量气管起始体积读数V1mL,加入液体,反应结束后调整量气管,记录读数为V2mL。NaBH4的浓度为______ (用含V1、V2的代数式表达)。
注:25℃,常压下气体摩尔体积约为24.5L•mol-1。______ (填“偏大”、“偏小”或“无影响”),需要将量气管慢慢______ 移动(填“向上”或“向下”)。
步骤1酯化 反应装置内按化学计量加入H3BO3和CH3OH,在54℃回流2h之后,开始收集B(OCH3)3(硼酸三甲酯)与CH3OH的共沸物,控制温度54℃~55℃。共沸液经硫酸酸洗后进行精馏,得到硼酸三甲酯
步骤2氢化 将金属钠分散于石蜡油中,通入氢气合成氢化钠
步骤3缩合 硼酸三甲酯和氢化钠在石蜡油介质中反应合成硼氢化钠,将物料冷却至100℃以下,进行离心分离得到硼氢化钠滤饼粗品。
步骤4水解 将上述硼氢化钠滤饼粗品置于容器中加水,发生反应NaOCH3+H2O=NaOH+CH3OH;将此水溶液离心分离,清液送入分层器,静置1h后分层。得到硼氢化钠碱性水溶液。
| pH值 | t/℃ | ||||
| 0 | 25 | 50 | 75 | 100 | |
| 8 | 3.0×10-3 | 4.3×10-5 | 6.0×10-5 | 8.5×10-6 | 1.2×10-6 |
| 10 | 3.0×10-1 | 4.3×10-2 | 6.0×10-3 | 8.5×10-4 | 1.2×10-4 |
| 12 | 3.0×101 | 4.3×100 | 6.0×10-1 | 8.5×10-2 | 1.2×10-2 |
| 14 | 3.0×103 | 4.3×102 | 6.0×101 | 8.5×100 | 1.2×100 |
(1)已知电负性B<H,硼氢化钠与水反应生成NaBO2,反应的化学方程式为
(2)步骤1中,硫酸的作用
(3)NaBH4溶液浓度可采用如下方法测定(装置如图2所示):25℃,常压下,用移液管移取2.00mL的)NaBH4溶液于烧瓶中,记录量气管起始体积读数V1mL,加入液体,反应结束后调整量气管,记录读数为V2mL。NaBH4的浓度为
注:25℃,常压下气体摩尔体积约为24.5L•mol-1。
您最近一年使用:0次
解题方法
10 .  和
和 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向 中加入足量稀硫酸时发生反应
中加入足量稀硫酸时发生反应 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 和
和 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向 中加入足量稀硫酸时发生反应
中加入足量稀硫酸时发生反应 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A. 和足量稀硫酸反应时,每产生 和足量稀硫酸反应时,每产生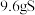 时,转移 时,转移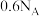 个电子 个电子 |
B.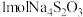 固体中共含有 固体中共含有 个离子 个离子 |
C. 与 与 的水溶液均显碱性 的水溶液均显碱性 |
D.向 中加入足量稀硫酸会有 中加入足量稀硫酸会有 产生,被氧化与被还原的原子数相等 产生,被氧化与被还原的原子数相等 |
您最近一年使用:0次



