解题方法
1 . 固态化合物CaCu2O3有如下转化:
(1)用化学式表示A的组成___________ ,写出溶液D中主要的阳离子___________ 。
(2)下列说法正确的是___________。
(3)已知高铜酸钠(NaCuO2)是一种黑色难溶于水的固体,具有强氧化性,但在中性或碱性溶液下稳定,可在NaOH溶液中用NaClO氧化Cu(OH)2制得。
①写出制备NaCuO2的离子方程式___________ 。
②制备的高铜酸钠中可能含有Cu(OH)2,设计实验证明Cu(OH)2是否存在___________ 。

(1)用化学式表示A的组成
(2)下列说法正确的是___________。
| A.反应Ⅰ中NH3体现氧化性 |
B.反应Ⅱ的现象说明稳定性: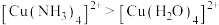 |
| C.气体混合物B的组成为N2、NH3 |
| D.固体G与水反应可以得到NH3 |
(3)已知高铜酸钠(NaCuO2)是一种黑色难溶于水的固体,具有强氧化性,但在中性或碱性溶液下稳定,可在NaOH溶液中用NaClO氧化Cu(OH)2制得。
①写出制备NaCuO2的离子方程式
②制备的高铜酸钠中可能含有Cu(OH)2,设计实验证明Cu(OH)2是否存在
您最近一年使用:0次
解题方法
2 . 根据实验目的设计方案并进行实验,观察到相关现象,方案设计或结论不正确 的是
| 选项 | 实验目的 | 方案设计 | 现象 | 结论 |
| A | 探究 与 与 水解程度的大小 水解程度的大小 | 分别测定 的 的 和 和 溶液 溶液 | 前者 小 小 |  水解程度小于 水解程度小于 |
| B | 探究 、 、 结合 结合 的能力 的能力 | 向 溶液依次滴加足量 溶液依次滴加足量 溶液、几滴 溶液、几滴 溶液 溶液 | 加入 后无明显变化,加入 后无明显变化,加入 溶液变红 溶液变红 | 结合 能力: 能力: |
| C | 探究 对 对 氧化性的影响 氧化性的影响 | 用 调节相同浓度 调节相同浓度 、 、 和 和 溶液的 溶液的 ,测量氧化反应所需最低 ,测量氧化反应所需最低 | 最低 顺序: 顺序: |  浓度越大, 浓度越大, 氧化性越强 氧化性越强 |
| D | 比较 与 与 结合 结合 能力 能力 | 将等浓度等体积的 溶液和 溶液和 溶液混合 溶液混合 | 产生白色沉淀 | 结合 能力: 能力: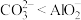 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-10更新
|
481次组卷
|
3卷引用:浙江省杭州市2024届高三下学期二模化学试题
浙江省杭州市2024届高三下学期二模化学试题浙江省2024届高三下学期5月选考适应性考试化学试题(已下线)压轴题09 微型化学实验设计与评价(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
名校
解题方法
3 . 工业上常以天青石(主要成分为SrSO4,含少量BaSO4)为原料制取SrCl2·6H2O,生产流程如下:
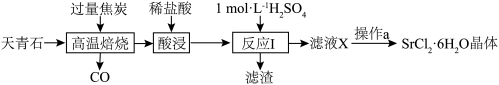
A.高温焙烧时,若0.2molSrSO4完全反应转移了1.6mol电子,该反应化学方程式为SrSO4+4C SrS+4CO↑ SrS+4CO↑ |
| B.反应Ⅰ中,应使用过量的H2SO4来提高锶元素的利用率 |
| C.为除去SrCl2·6H2O晶体表面杂质,可使用无水乙醇洗涤 |
| D.为得到无水SrCl2,可直接加热SrCl2·6H2O脱去结晶水制得 |
您最近一年使用:0次
2024-04-04更新
|
56次组卷
|
2卷引用:浙江省湖州中学2023-2024学年高二下学期第二次阶段检测化学试卷
4 . 近来中国隐形战机歼-20换装试飞成功,大大壮我军威。这得益于师昌绪等科学家开发的由新型无机非金属材料制成的新型发动机,热效率高、寿命长。这类材料中研究较多的是化合物G。化合物G的相对分子质量为140,含有硅元素,其质量分数为40%,另含有元素Y。化合物E(含两种元素)与 反应制得G和HCl。
反应制得G和HCl。
(1)G化学式为___________ 。
(2)写出E与 反应的化学方程式:
反应的化学方程式:___________ 。
(3)粉末状G能够与氧气在高温下反应,所得产物中有一种是空气的主要成分,另一种是氧化物,该过程的化学方程式为___________ 。
 反应制得G和HCl。
反应制得G和HCl。(1)G化学式为
(2)写出E与
 反应的化学方程式:
反应的化学方程式:(3)粉末状G能够与氧气在高温下反应,所得产物中有一种是空气的主要成分,另一种是氧化物,该过程的化学方程式为
您最近一年使用:0次
5 . 按要求完成下列化学方程式:
(1)铁丝在氧气中燃烧的产物能溶于稀盐酸,试写出反应的化学方程式___________ 。
(2)“神舟五号”火箭的动力来源是联氨 和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式
和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式___________ 。
(3)已知 和
和 都是易分解的二元弱酸,且
都是易分解的二元弱酸,且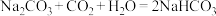 。试写出将过量
。试写出将过量 通入到少量NaOH溶液中反应的化学方程式
通入到少量NaOH溶液中反应的化学方程式___________ 。
(4)已知硫和氧的性质相似,对应化合物的性质也相似,且 (硫代碳酸钠),试写出
(硫代碳酸钠),试写出 和
和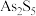 反应的化学方程式
反应的化学方程式___________ 。
(1)铁丝在氧气中燃烧的产物能溶于稀盐酸,试写出反应的化学方程式
(2)“神舟五号”火箭的动力来源是联氨
 和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式
和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式(3)已知
 和
和 都是易分解的二元弱酸,且
都是易分解的二元弱酸,且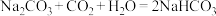 。试写出将过量
。试写出将过量 通入到少量NaOH溶液中反应的化学方程式
通入到少量NaOH溶液中反应的化学方程式(4)已知硫和氧的性质相似,对应化合物的性质也相似,且
 (硫代碳酸钠),试写出
(硫代碳酸钠),试写出 和
和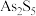 反应的化学方程式
反应的化学方程式
您最近一年使用:0次
名校
6 . 请回答:
(1)Na的原子结构示意图是________________ ;MgCl2电子式是___________________ 。
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有________________ 性。
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是________________ 。
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是________________ ;此反应的离子方程式是________________ 。然后在溶液中再加入足量的铁粉,现象是________________ ,此时反应的离子方程式是________________ 。
(1)Na的原子结构示意图是
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是
您最近一年使用:0次
名校
解题方法
7 . 已知难溶性化合物 的化学式为
的化学式为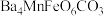 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。
(1) 高温下在
高温下在 气流中的反应
气流中的反应________ 氧化还原反应(填“属于”或“不属于”), 中钡元素的化合价为
中钡元素的化合价为________ 。
(2)步骤Ⅳ可以进行的原因除了生成 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因________ 。
(3)下列说法正确的是________。
(4)固体 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式________ 。
(5)设计实验检验混合气体A(除 外)的成份
外)的成份________ 。
 的化学式为
的化学式为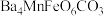 ,对
,对 进行如下实验,部分产物已经略去。
进行如下实验,部分产物已经略去。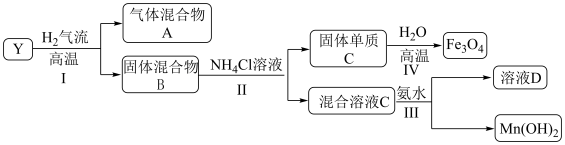
 中的金属元素在该实验条件下不能与
中的金属元素在该实验条件下不能与 产生配合物。
产生配合物。(1)
 高温下在
高温下在 气流中的反应
气流中的反应 中钡元素的化合价为
中钡元素的化合价为(2)步骤Ⅳ可以进行的原因除了生成
 降低体系的能量之外,从化学平衡的角度解释能够发生的原因
降低体系的能量之外,从化学平衡的角度解释能够发生的原因(3)下列说法正确的是________。
A.溶液D中阳离子只有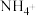 |
| B.若磁铁能吸引反应Ⅳ的剩余固体,则证明铁有剩余 |
| C.步骤Ⅱ中的氯化铵溶液也可以用盐酸代替 |
D.依据步骤Ⅲ可知碱性强弱 |
(4)固体
 在一定条件下也可以与
在一定条件下也可以与 溶液反应,写出反应的离子方程式
溶液反应,写出反应的离子方程式(5)设计实验检验混合气体A(除
 外)的成份
外)的成份
您最近一年使用:0次
名校
8 . 为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。后者常采用 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是(
,下列说法不正确的是( 为阿伏加德罗常数)
为阿伏加德罗常数)
 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是(
,下列说法不正确的是( 为阿伏加德罗常数)
为阿伏加德罗常数)| A.氧化产物与还原产物的质量比为3∶4 | B.生成 水转移电子的数目为 水转移电子的数目为 |
C.可使用 溶液吸收氮氧化物 溶液吸收氮氧化物 | D.氮氧化物的排放可形成酸雨 |
您最近一年使用:0次
名校
解题方法
9 .  和
和 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向 中加入足量稀硫酸时发生反应
中加入足量稀硫酸时发生反应 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 和
和 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向
均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为混盐)。已知向 中加入足量稀硫酸时发生反应
中加入足量稀硫酸时发生反应 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A. 和足量稀硫酸反应时,每产生 和足量稀硫酸反应时,每产生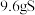 时,转移 时,转移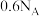 个电子 个电子 |
B.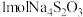 固体中共含有 固体中共含有 个离子 个离子 |
C. 与 与 的水溶液均显碱性 的水溶液均显碱性 |
D.向 中加入足量稀硫酸会有 中加入足量稀硫酸会有 产生,被氧化与被还原的原子数相等 产生,被氧化与被还原的原子数相等 |
您最近一年使用:0次
2024-03-21更新
|
527次组卷
|
4卷引用:浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题
浙江省宁波市镇海中学2023-2024学年高二下学期期末考试化学试题 山东省泰安市2024届高三一模检测化学试题(已下线)压轴题02 氧化还原反应的概念及规律(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
10 . 通过电化学将 转化为有机物、开发利用清洁能源都是实现“双碳”目标的重要途径。请回答:
转化为有机物、开发利用清洁能源都是实现“双碳”目标的重要途径。请回答:
(1)某研究小组采用单原子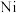 和纳米
和纳米 作串联催化剂,通过电解法将
作串联催化剂,通过电解法将 最终转化为乙烯,装置示意图如图1所示。惰性电极a上催化剂纳米
最终转化为乙烯,装置示意图如图1所示。惰性电极a上催化剂纳米 处的电极反应式为
处的电极反应式为__________ 。 ,主要反应如下:
,主要反应如下:
反应Ⅰ: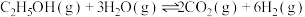
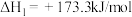
反应Ⅱ:

反应Ⅲ: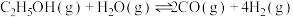

①
__________  。
。
②保持压强为 ,按
,按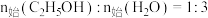 投料,发生反应,测得平衡时
投料,发生反应,测得平衡时 和
和 的选择性[例如
的选择性[例如 的选择性
的选择性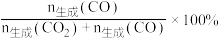 ]及
]及 的产率[
的产率[ 产率
产率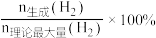 ]随温度T的变化关系如图2所示。
]随温度T的变化关系如图2所示。
下列说法正确的是__________ 。
A.曲线a表示平衡时 的选择性
的选择性
B.乙醇的平衡转化率随温度的升高一直增大
C.300℃后曲线b随温度升高而降低的原因是催化剂在高温下活性下降
D.降低水醇比[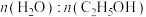 ]有助于提高
]有助于提高 的选择性
的选择性
③500℃、100kPa条件下,反应Ⅱ中用平衡分压表示的平衡常数
__________ 。
(3)第三个研究小组研究 还原
还原 获得能源
获得能源 。恒压、750℃条件下,
。恒压、750℃条件下, 和
和 按物质的量之比1:3投料,经如下流程实现
按物质的量之比1:3投料,经如下流程实现 高效转化。
高效转化。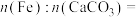
__________ 。
②若 和
和 按物质的量之比1:1投料,会导致过程ⅱ、ⅲ循环无法持续进行,请解释原因(结合第①问数据进行说明)
按物质的量之比1:1投料,会导致过程ⅱ、ⅲ循环无法持续进行,请解释原因(结合第①问数据进行说明)__________ 。
 转化为有机物、开发利用清洁能源都是实现“双碳”目标的重要途径。请回答:
转化为有机物、开发利用清洁能源都是实现“双碳”目标的重要途径。请回答:(1)某研究小组采用单原子
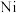 和纳米
和纳米 作串联催化剂,通过电解法将
作串联催化剂,通过电解法将 最终转化为乙烯,装置示意图如图1所示。惰性电极a上催化剂纳米
最终转化为乙烯,装置示意图如图1所示。惰性电极a上催化剂纳米 处的电极反应式为
处的电极反应式为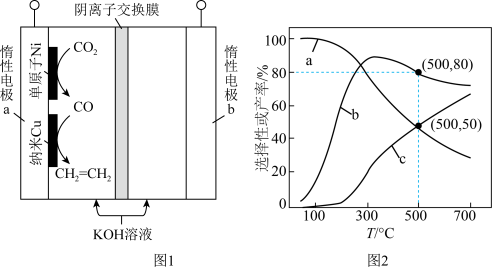
 ,主要反应如下:
,主要反应如下:反应Ⅰ:
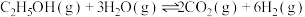
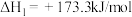
反应Ⅱ:


反应Ⅲ:
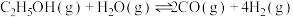

①

 。
。②保持压强为
 ,按
,按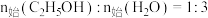 投料,发生反应,测得平衡时
投料,发生反应,测得平衡时 和
和 的选择性[例如
的选择性[例如 的选择性
的选择性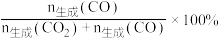 ]及
]及 的产率[
的产率[ 产率
产率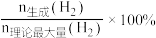 ]随温度T的变化关系如图2所示。
]随温度T的变化关系如图2所示。下列说法正确的是
A.曲线a表示平衡时
 的选择性
的选择性B.乙醇的平衡转化率随温度的升高一直增大
C.300℃后曲线b随温度升高而降低的原因是催化剂在高温下活性下降
D.降低水醇比[
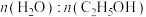 ]有助于提高
]有助于提高 的选择性
的选择性③500℃、100kPa条件下,反应Ⅱ中用平衡分压表示的平衡常数

(3)第三个研究小组研究
 还原
还原 获得能源
获得能源 。恒压、750℃条件下,
。恒压、750℃条件下, 和
和 按物质的量之比1:3投料,经如下流程实现
按物质的量之比1:3投料,经如下流程实现 高效转化。
高效转化。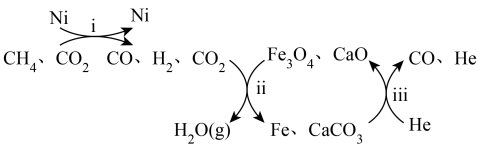
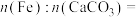
②若
 和
和 按物质的量之比1:1投料,会导致过程ⅱ、ⅲ循环无法持续进行,请解释原因(结合第①问数据进行说明)
按物质的量之比1:1投料,会导致过程ⅱ、ⅲ循环无法持续进行,请解释原因(结合第①问数据进行说明)
您最近一年使用:0次



