解题方法
1 . Ⅰ.实验室用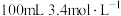 的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中
的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中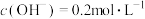 ,
, 和
和 的物质的量浓度之比为
的物质的量浓度之比为 。(不考虑反应前后溶液的体积变化)。
。(不考虑反应前后溶液的体积变化)。
(1)吸收氯气所消耗的氢氧化钠物质的量为__________ 。
(2)被氧化与被还原的氯气的物质的量之比为__________ 。
Ⅱ.无水 与
与 作用会生成
作用会生成 。现有
。现有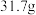 无水
无水 ,吸收
,吸收 后变成
后变成 ,试回答下列问题:
,试回答下列问题:
(3) 中
中
__________ 。
(4) 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到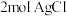 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为__________ 。
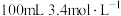 的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中
的氢氧化钠溶液吸收多余的氯气。测得吸收后的溶液中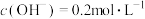 ,
, 和
和 的物质的量浓度之比为
的物质的量浓度之比为 。(不考虑反应前后溶液的体积变化)。
。(不考虑反应前后溶液的体积变化)。(1)吸收氯气所消耗的氢氧化钠物质的量为
(2)被氧化与被还原的氯气的物质的量之比为
Ⅱ.无水
 与
与 作用会生成
作用会生成 。现有
。现有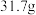 无水
无水 ,吸收
,吸收 后变成
后变成 ,试回答下列问题:
,试回答下列问题:(3)
 中
中
(4)
 为配合物,其中
为配合物,其中 的配位数为6,经测定
的配位数为6,经测定 该配合物和足量
该配合物和足量 溶液反应得到
溶液反应得到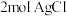 沉淀,则该配合物的化学式可表示为
沉淀,则该配合物的化学式可表示为
您最近一年使用:0次
解题方法
2 . 下图是氯的“价类二维图”,请根据所学回答下列问题:

(1)已知A、H均为一元酸,写出A、H的化学式:___________ 、___________ 。
(2)写出B物质的一种用途:___________ 。
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:___________ 。
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的___________ 倍(已知两种消毒剂均被还原为 )。
)。

(1)已知A、H均为一元酸,写出A、H的化学式:
(2)写出B物质的一种用途:
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的
 )。
)。
您最近一年使用:0次
名校
解题方法
3 . 工业上以NH3为原料按如下流程制取化合物A。 反应生成Cl-
反应生成Cl-
请回答:
(1)写出NH3催化氧化生成NO的化学方程式________ 。
(2)等物质的量的HNO3与ClF反应除生成A外,另一种产物为HF。
①电子衍射研究表明,气态HF中存在环状六聚体(HF)6,而其他卤素的气态氢化物却不存在,气态HF中存在环状六聚体(HF)6的原因是_____ 。
②下列说法正确的是_____ 。
A.尾气的主要成分是NO,可用NaOH溶液直接吸收 B.ClF中的Cl呈零价
C.化合物A具有强氧化性 D.TiCl4与A反应能生成Ti(NO3)4
(3)①设计实验验证化合物A中含有Cl元素___________ 。
②写出实验过程中涉及的反应方程式___________ 。

 反应生成Cl-
反应生成Cl-请回答:
(1)写出NH3催化氧化生成NO的化学方程式
(2)等物质的量的HNO3与ClF反应除生成A外,另一种产物为HF。
①电子衍射研究表明,气态HF中存在环状六聚体(HF)6,而其他卤素的气态氢化物却不存在,气态HF中存在环状六聚体(HF)6的原因是
②下列说法正确的是
A.尾气的主要成分是NO,可用NaOH溶液直接吸收 B.ClF中的Cl呈零价
C.化合物A具有强氧化性 D.TiCl4与A反应能生成Ti(NO3)4
(3)①设计实验验证化合物A中含有Cl元素
②写出实验过程中涉及的反应方程式
您最近一年使用:0次
名校
解题方法
4 . 下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。 可被其它更易被吸附的阴离子替代)对
可被其它更易被吸附的阴离子替代)对 有很强的交换吸附能力;②步骤“交换吸附”发生的反应:
有很强的交换吸附能力;②步骤“交换吸附”发生的反应: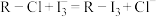 。
。
请回答:
(1)写出海带浸出液被氧化生成粗碘水过程中的反应方程式:__________ 。
(2)下列说法正确的是__________。
(3)“氧化”过程不能加入过量 ,原因是
,原因是__________ 。
(4)流程中的中间产物 可在淀粉指示剂下与酸化的过氧化氢反应,现象为蓝色—无色—蓝色—无色的重复现象,称为“碘钟实验”,写出a过程的离子方程式。
可在淀粉指示剂下与酸化的过氧化氢反应,现象为蓝色—无色—蓝色—无色的重复现象,称为“碘钟实验”,写出a过程的离子方程式。
a.蓝色出现,并伴有大量气泡:__________ ;
b.蓝色消失:
(5)设计实验方案验证氧化过程得到粗碘水中碘元素除 外可能的存在形式。(不考虑其它杂质阴离子)
外可能的存在形式。(不考虑其它杂质阴离子)__________ 。
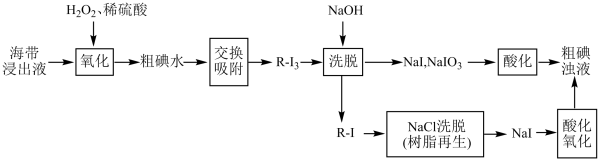
 可被其它更易被吸附的阴离子替代)对
可被其它更易被吸附的阴离子替代)对 有很强的交换吸附能力;②步骤“交换吸附”发生的反应:
有很强的交换吸附能力;②步骤“交换吸附”发生的反应: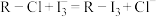 。
。请回答:
(1)写出海带浸出液被氧化生成粗碘水过程中的反应方程式:
(2)下列说法正确的是__________。
A.已知 的VSEPR模型为 的VSEPR模型为 ,推测 ,推测 为sp杂化 为sp杂化 |
B.可用KI溶液提取 中的碘单质 中的碘单质 |
C.该制备流程中“洗脱”、“酸化”、“ 洗脱”均涉及到氧化还原反应 洗脱”均涉及到氧化还原反应 |
D.“酸化氧化”过程若选择 为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则 为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则 与 与 的物质的量比应不少于 的物质的量比应不少于 |
(3)“氧化”过程不能加入过量
 ,原因是
,原因是(4)流程中的中间产物
 可在淀粉指示剂下与酸化的过氧化氢反应,现象为蓝色—无色—蓝色—无色的重复现象,称为“碘钟实验”,写出a过程的离子方程式。
可在淀粉指示剂下与酸化的过氧化氢反应,现象为蓝色—无色—蓝色—无色的重复现象,称为“碘钟实验”,写出a过程的离子方程式。a.蓝色出现,并伴有大量气泡:
b.蓝色消失:

(5)设计实验方案验证氧化过程得到粗碘水中碘元素除
 外可能的存在形式。(不考虑其它杂质阴离子)
外可能的存在形式。(不考虑其它杂质阴离子)
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)已知活泼金属可以与水反应,如 ↑,而单质硅(
↑,而单质硅( )通常不与水反应,但单质硅能够溶解在
)通常不与水反应,但单质硅能够溶解在 溶液中并产生H2。请写出该反应可能的化学方程式
溶液中并产生H2。请写出该反应可能的化学方程式___________ 。
(2)已知 在常温无氧条件下可以分解产生
在常温无氧条件下可以分解产生 和一种气体单质,请写出可能的化学方程式
和一种气体单质,请写出可能的化学方程式___________ 。
(3)CuCl2溶液呈绿色的原因可认为是CuCl2溶解后生成了个数比 的两种离子,其中一种是蓝色的
的两种离子,其中一种是蓝色的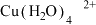 ,另一种离子显黄色,请写出该离子可能的化学式
,另一种离子显黄色,请写出该离子可能的化学式___________ 。
(4)尿素 是一种常见的氮肥,在较高温度下可以与水反应生成两种常见的气体,请写出可能的化学方程式
是一种常见的氮肥,在较高温度下可以与水反应生成两种常见的气体,请写出可能的化学方程式___________ 。
(1)已知活泼金属可以与水反应,如
 ↑,而单质硅(
↑,而单质硅( )通常不与水反应,但单质硅能够溶解在
)通常不与水反应,但单质硅能够溶解在 溶液中并产生H2。请写出该反应可能的化学方程式
溶液中并产生H2。请写出该反应可能的化学方程式(2)已知
 在常温无氧条件下可以分解产生
在常温无氧条件下可以分解产生 和一种气体单质,请写出可能的化学方程式
和一种气体单质,请写出可能的化学方程式(3)CuCl2溶液呈绿色的原因可认为是CuCl2溶解后生成了个数比
 的两种离子,其中一种是蓝色的
的两种离子,其中一种是蓝色的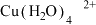 ,另一种离子显黄色,请写出该离子可能的化学式
,另一种离子显黄色,请写出该离子可能的化学式(4)尿素
 是一种常见的氮肥,在较高温度下可以与水反应生成两种常见的气体,请写出可能的化学方程式
是一种常见的氮肥,在较高温度下可以与水反应生成两种常见的气体,请写出可能的化学方程式
您最近一年使用:0次
6 . 物质结构决定物质性质。已知氢元素原子的核电荷数为1。试分析:
(1) 是一种离子化合物,应读作
是一种离子化合物,应读作_______ 。它与盐酸反应生成一种盐和一种可燃性气体,其化学方程式为_______ 。已知反应物中具有氧化性的物质,发生还原反应后,元素化合价降低。请判断上述反应中,反应物_______ (填化学式)具有氧化性。
(2)氢原子可以和很多原子组成10电子或18电子的微粒。请写出氢原子与其他一种原子形成的五核(五个原子)10电子微粒且带正荷的化学式:_______ ;也请写出氢原子与其他一种原子形成的六核(六个原子)18电子微粒的分子式:_______ 。
(1)
 是一种离子化合物,应读作
是一种离子化合物,应读作(2)氢原子可以和很多原子组成10电子或18电子的微粒。请写出氢原子与其他一种原子形成的五核(五个原子)10电子微粒且带正荷的化学式:
您最近一年使用:0次
名校
7 . 回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)高温下铝粉与氧化铁的反应可用来焊接钢轨。置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。写出该反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)高温下铝粉与氧化铁的反应可用来焊接钢轨。置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。写出该反应的化学方程式,并用单线桥表示电子转移的方向和数目
您最近一年使用:0次
名校
解题方法
8 . 利用表面含有油脂的废旧的铁屑制备Fe3O4粒子,流程如下:
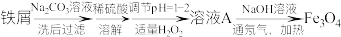
已知: 易与水反应(水解反应),pH=2.7时开始沉淀,pH=3.7沉淀完全。
易与水反应(水解反应),pH=2.7时开始沉淀,pH=3.7沉淀完全。
回答下列问题:
(1)Na2CO3溶液的作用是___________ 。
(2)调节pH为1—2的目的是___________ 。
(3)控制H2O2用量的原因是___________ 。
(4)溶液A中的阳离子是___________ ,检验溶液A中阳离子(除Fe元素外形成的阳离子)的具体操作是___________ 。
(5)溶液A到Fe3O4的离子方程式是___________ 。
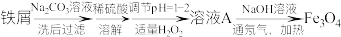
已知:
 易与水反应(水解反应),pH=2.7时开始沉淀,pH=3.7沉淀完全。
易与水反应(水解反应),pH=2.7时开始沉淀,pH=3.7沉淀完全。回答下列问题:
(1)Na2CO3溶液的作用是
(2)调节pH为1—2的目的是
(3)控制H2O2用量的原因是
(4)溶液A中的阳离子是
(5)溶液A到Fe3O4的离子方程式是
您最近一年使用:0次
9 . 某研究性学习小组设计了如图所示的实验,以此来验证氯、溴、碘三种卤素单质的氧化性顺序。图中A、B、C分别是浸有饱和溴化钠溶液、饱和碘化钾溶液、冷水的棉球,烧杯D中盛有氢氧化钠溶液。实验时,打开止水夹从左端导管口缓慢通入氯气片刻,关闭止水夹停通氯气再对B棉球进行加热。
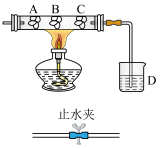
导管右侧插入玻璃管左侧橡胶塞
请利用下表提供的信息,结合所学知识,完成下列问题:
(1)棉球A的现象:_______ 。
(2)棉球B上反应的离子方程式:_______ 。
(3)棉球C的现象:_______ 。
(4)氢氧化钠溶液的作用是_______ ,写出其中一反应的离子方程式:_______ 。
(5)由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:_______ 、_______ 。

导管右侧插入玻璃管左侧橡胶塞
请利用下表提供的信息,结合所学知识,完成下列问题:
| 卤素单质 | 颜色和状态 | 蒸气颜色 | 在水中的溶解度 | 水溶液的颜色 | 熔点/℃ | 沸点/℃ |
 | 黄绿色气体 | / | 在一定量水中溶解的溶质的物质的量逐渐减少 | 淡黄绿色 |  |  |
 | 深红棕色液体 | 红棕色 | 橙色 | 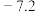 | 58.78 | |
 | 紫黑色固体 | 紫色 | 黄褐色 | 113.5 | 184.4 |
(1)棉球A的现象:
(2)棉球B上反应的离子方程式:
(3)棉球C的现象:
(4)氢氧化钠溶液的作用是
(5)由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:
您最近一年使用:0次
10 . 中医药典记载木耳具有“和血养营”功效。某实验小组称取一定量黑木耳以检验黑木耳中含有铁元素、并测定铁元素含量。实验过程如下:

Ⅰ.定性检验
(1)“灼烧”中用于盛装黑木耳的仪器是________ 。
(2)甲同学往“酸浸”所得溶液中加入高锰酸钾,发现溶液的紫红色褪去,因此得出“此酸浸溶液中含 ”的结论。乙同学不赞同甲同学的观点,乙同学的理由是
”的结论。乙同学不赞同甲同学的观点,乙同学的理由是________ 。
Ⅱ.定量分析1——高锰酸钾滴定法
(3)取一定量待测液,利用盐酸羟胺(在溶液中可完全电离出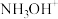 与
与 )将溶液中
)将溶液中 还原为
还原为 ,同时产生一种无污染的气体,该反应的离子方程式为
,同时产生一种无污染的气体,该反应的离子方程式为________ ;再利用酸性高锰酸钾溶液氧化 ,根据消耗的高锰酸钾溶液的体积以计算铁元素含量。
,根据消耗的高锰酸钾溶液的体积以计算铁元素含量。
(4)配制一定物质的量浓度的高锰酸钾溶液时,下列操作会使铁元素含量测量值偏高的是________。
Ⅲ.定量分析2——吸光度法
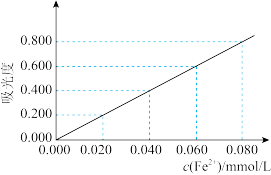
(5)取10mL待测液,利用吸光度法测得其吸光度为0.600(吸光度与 的浓度关系如下图所示)。
的浓度关系如下图所示)。
该黑木耳中铁元素的含量(溶液密度为 )=
)=________ (mg/100g)。

Ⅰ.定性检验
(1)“灼烧”中用于盛装黑木耳的仪器是
(2)甲同学往“酸浸”所得溶液中加入高锰酸钾,发现溶液的紫红色褪去,因此得出“此酸浸溶液中含
 ”的结论。乙同学不赞同甲同学的观点,乙同学的理由是
”的结论。乙同学不赞同甲同学的观点,乙同学的理由是Ⅱ.定量分析1——高锰酸钾滴定法
(3)取一定量待测液,利用盐酸羟胺(在溶液中可完全电离出
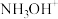 与
与 )将溶液中
)将溶液中 还原为
还原为 ,同时产生一种无污染的气体,该反应的离子方程式为
,同时产生一种无污染的气体,该反应的离子方程式为 ,根据消耗的高锰酸钾溶液的体积以计算铁元素含量。
,根据消耗的高锰酸钾溶液的体积以计算铁元素含量。(4)配制一定物质的量浓度的高锰酸钾溶液时,下列操作会使铁元素含量测量值偏高的是________。
| A.没有进行洗涤操作 |
| B.定容时俯视容量瓶的刻度线 |
| C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线 |
| D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制 |
Ⅲ.定量分析2——吸光度法
(5)取10mL待测液,利用吸光度法测得其吸光度为0.600(吸光度与
 的浓度关系如下图所示)。
的浓度关系如下图所示)。该黑木耳中铁元素的含量(溶液密度为
 )=
)=
您最近一年使用:0次



