1 . 下图是氯元素的“价-类”二维图,回答下列问题。

(1)氯元素在周期表中的位置为________ ,上述物质中氯元素只具有还原性的是________ 。
(2)上述物质中NaClO的是“84”消毒液的有效成分,若与洁厕灵(主要成分HCl)混用,会产生有毒气体,若标准状况下产生22.4L气体,转移的电子数为________ 。
(3)利用 可制取“84”消毒液,实验室制取
可制取“84”消毒液,实验室制取 的离子方程式为
的离子方程式为________ 。
(4)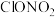 可与水反应生成两种酸,请写出对应化学方程式
可与水反应生成两种酸,请写出对应化学方程式________ 。

(1)氯元素在周期表中的位置为
(2)上述物质中NaClO的是“84”消毒液的有效成分,若与洁厕灵(主要成分HCl)混用,会产生有毒气体,若标准状况下产生22.4L气体,转移的电子数为
(3)利用
 可制取“84”消毒液,实验室制取
可制取“84”消毒液,实验室制取 的离子方程式为
的离子方程式为(4)
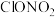 可与水反应生成两种酸,请写出对应化学方程式
可与水反应生成两种酸,请写出对应化学方程式
您最近一年使用:0次
2 . 按要求填空。
(1)2016年IUPAC将第117号元素命名为Ts,则中子数为176的Ts的核素符号是________ 。
(2)漂粉精可做漂白棉、麻、纸张的漂白剂,也可用于游泳池等场所的消毒剂,其主要成分是________ 。
(3)目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应,生成 和
和 。指出上述反应中的氧化剂与氧化产物的物质的量之比
。指出上述反应中的氧化剂与氧化产物的物质的量之比________ 。
(4)现有NaCl、 ,和
,和 三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与
三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与 反应的离子方程式
反应的离子方程式________ 。
(1)2016年IUPAC将第117号元素命名为Ts,则中子数为176的Ts的核素符号是
(2)漂粉精可做漂白棉、麻、纸张的漂白剂,也可用于游泳池等场所的消毒剂,其主要成分是
(3)目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应,生成
 和
和 。指出上述反应中的氧化剂与氧化产物的物质的量之比
。指出上述反应中的氧化剂与氧化产物的物质的量之比(4)现有NaCl、
 ,和
,和 三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与
三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组拟按如下步骤合成铁系催化剂的中间体[Fe(CO)2Cl2]: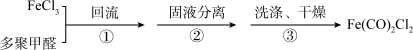
其中步骤①实验装置如图所示:
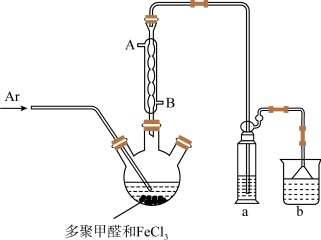
已知:
(I)多聚甲醛为(CH2O)n(n=6~100),当n<12的多聚甲醛可溶于水,当n≥12则不溶于水;加酸或160~200°C加热时会解聚。
(Ⅰ)[Fe(CO)2Cl2]遇氧气、水都会反应,其中Fe的化合价为+2价。
(Ⅱ)SnCl2有强还原性,可被弱氧化剂HgCl2氧化:2HgCl2+SnCl2=Hg2Cl2↓+SnCl4。
请回答:
(1)步骤③产物干燥后仍需放置在干燥器中,以下称为干燥器的是_______。
(2)操作步骤②时仍需在氩气氛围下完成,理由是_______ 。
(3)写出生成[Fe(CO)2Cl2]的化学反应方程式_______ 。
(4)仪器a中盛放的试剂为_______ ,装置b的作用是_______ 。
(5)测定产品纯度时,先称取一定量[Fe(CO)2Cl2],经多步处理并转化为Fe2+后,再用KMnO4标准溶液(用Na2C2O4标准溶液标定)滴定其含量。从下列选项中选出合理的操作并排序:_______ 。
c→ →a→ → →f
a.将准确称量的[Fe(CO)2Cl2]溶解于水
b.准确称量Na2C2O4并配制一定物质的量浓度的溶液,进行滴定
c.将制备的KMnO4溶液加热煮沸,冷却后滤去MnO2
d.用HgCl2除过量的SnCl2,滤去沉淀
e.加入足量SnCl2进行还原
f.用Na2C2O4标准溶液标定后的KMnO4溶液进行滴定
下列情况会导致测量结果偏大的是_______ 。
A.[Fe(CO)2Cl2]产品含少量多聚甲醛杂质
B.过量的SnCl2未被除尽
C.[Fe(CO)2Cl2]产品部分氧化或潮解
D.配好的KMnO4标准溶液久置后使用

其中步骤①实验装置如图所示:

已知:
(I)多聚甲醛为(CH2O)n(n=6~100),当n<12的多聚甲醛可溶于水,当n≥12则不溶于水;加酸或160~200°C加热时会解聚。
(Ⅰ)[Fe(CO)2Cl2]遇氧气、水都会反应,其中Fe的化合价为+2价。
(Ⅱ)SnCl2有强还原性,可被弱氧化剂HgCl2氧化:2HgCl2+SnCl2=Hg2Cl2↓+SnCl4。
请回答:
(1)步骤③产物干燥后仍需放置在干燥器中,以下称为干燥器的是_______。
A.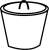 | B. | C.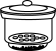 | D. |
(2)操作步骤②时仍需在氩气氛围下完成,理由是
(3)写出生成[Fe(CO)2Cl2]的化学反应方程式
(4)仪器a中盛放的试剂为
(5)测定产品纯度时,先称取一定量[Fe(CO)2Cl2],经多步处理并转化为Fe2+后,再用KMnO4标准溶液(用Na2C2O4标准溶液标定)滴定其含量。从下列选项中选出合理的操作并排序:
c→ →a→ → →f
a.将准确称量的[Fe(CO)2Cl2]溶解于水
b.准确称量Na2C2O4并配制一定物质的量浓度的溶液,进行滴定
c.将制备的KMnO4溶液加热煮沸,冷却后滤去MnO2
d.用HgCl2除过量的SnCl2,滤去沉淀
e.加入足量SnCl2进行还原
f.用Na2C2O4标准溶液标定后的KMnO4溶液进行滴定
下列情况会导致测量结果偏大的是
A.[Fe(CO)2Cl2]产品含少量多聚甲醛杂质
B.过量的SnCl2未被除尽
C.[Fe(CO)2Cl2]产品部分氧化或潮解
D.配好的KMnO4标准溶液久置后使用
您最近一年使用:0次
名校
4 . 亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
请回答:
(1)NOCl的电子式为_______ ,化合物X的结构简式为_______ 。
(2)下列说法正确的是_______。
(3)已知浓盐酸和浓硝酸混合配制王水时也会产生亚硝酰氯,写出该反应的化学方程式_______ 。
(4)设计实验验证化合物X中含有Cl元素_______ ;写出实验过程中涉及的反应方程式_______ 。
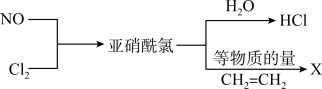
请回答:
(1)NOCl的电子式为
(2)下列说法正确的是_______。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为V形 |
C.化合物X的沸点低于氯乙酰胺( ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
(3)已知浓盐酸和浓硝酸混合配制王水时也会产生亚硝酰氯,写出该反应的化学方程式
(4)设计实验验证化合物X中含有Cl元素
您最近一年使用:0次
5 . 为探究一种矿石(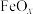 )的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用
)的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用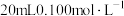 的
的 溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的
溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的 还原,得固体1.120g。请回答:
还原,得固体1.120g。请回答:
(1)实验用稀硫酸溶解矿石而不用盐酸,原因是___________ (用文字或用方程式表述均可)。
(2)矿石的化学组成为___________ 。
(3)若无“另取1.504g样品用足量的 还原,得固体1.120g”的数据,能否求得该矿石的组成:
还原,得固体1.120g”的数据,能否求得该矿石的组成:___________ (填“能”或“否”)。
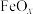 )的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用
)的组成,已知矿石不含其他杂质,铁元素呈+2、+3价,氧元素为-2价。称取1.504g样品用足量的稀硫酸溶解,所得溶液用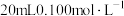 的
的 溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的
溶液恰好使+2价铁元素氧化为+3价,同时Cr元素被还原为+3价。另取1.504g样品用足量的 还原,得固体1.120g。请回答:
还原,得固体1.120g。请回答:(1)实验用稀硫酸溶解矿石而不用盐酸,原因是
(2)矿石的化学组成为
(3)若无“另取1.504g样品用足量的
 还原,得固体1.120g”的数据,能否求得该矿石的组成:
还原,得固体1.120g”的数据,能否求得该矿石的组成:
您最近一年使用:0次
6 . 请按要求填空。
(1)写出磁性氧化铁的化学式:___________ 。
(2)碘水与 溶液混合,生成了
溶液混合,生成了 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(3)溴水与 溶液反应有淡黄色AgBr沉淀生成,写出反应的离子方程式:
溶液反应有淡黄色AgBr沉淀生成,写出反应的离子方程式:________ 。
(4)已知在一定温度下,溴与NaOH溶液反应,产物中NaBrO与 的物质的量之比为3:1,写出反应的化学方程式:
的物质的量之比为3:1,写出反应的化学方程式:___________ 。
(1)写出磁性氧化铁的化学式:
(2)碘水与
 溶液混合,生成了
溶液混合,生成了 ,写出反应的离子方程式:
,写出反应的离子方程式:(3)溴水与
 溶液反应有淡黄色AgBr沉淀生成,写出反应的离子方程式:
溶液反应有淡黄色AgBr沉淀生成,写出反应的离子方程式:(4)已知在一定温度下,溴与NaOH溶液反应,产物中NaBrO与
 的物质的量之比为3:1,写出反应的化学方程式:
的物质的量之比为3:1,写出反应的化学方程式:
您最近一年使用:0次
解题方法
7 . 食用盐中常加入碘酸钾以实现补碘,工业上有多种方法制备碘酸钾,其中一种采用 氧化法:
氧化法: ,下列有关说法
,下列有关说法不正确 的是
 氧化法:
氧化法: ,下列有关说法
,下列有关说法A. 是还原产物 是还原产物 |
B.氧化性: |
| C.当反应中转移10mol电子,此时生成22.4L氯气 |
D.通过该反应相关物质的氧化性强弱可知:能用 与 与 反应来制取 反应来制取 |
您最近一年使用:0次
解题方法
8 . 用下列装置制备 溶液,装置B中放入
溶液,装置B中放入 溶液。(部分夹持装置已省略)
溶液。(部分夹持装置已省略)
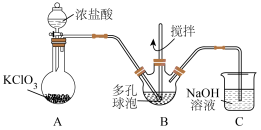
请回答下列问题:
(1)多孔球泡的作用是___________ 。
(2)NaOH溶液的作用是___________ 。
(3)装置B中反应的离子方程式为___________ 。
(4)装置A可制备 ,写出反应的化学方程式,并用单线桥法标出电子转移方向和数目:
,写出反应的化学方程式,并用单线桥法标出电子转移方向和数目:___________ 。
(5)当 发生反应时,被氧化的
发生反应时,被氧化的 的物质的量为
的物质的量为___________ mol。
 溶液,装置B中放入
溶液,装置B中放入 溶液。(部分夹持装置已省略)
溶液。(部分夹持装置已省略)
请回答下列问题:
(1)多孔球泡的作用是
(2)NaOH溶液的作用是
(3)装置B中反应的离子方程式为
(4)装置A可制备
 ,写出反应的化学方程式,并用单线桥法标出电子转移方向和数目:
,写出反应的化学方程式,并用单线桥法标出电子转移方向和数目:(5)当
 发生反应时,被氧化的
发生反应时,被氧化的 的物质的量为
的物质的量为
您最近一年使用:0次
解题方法
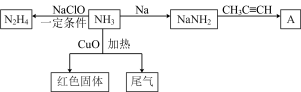
9 . 氨气用途非常广泛,以下是氨气的部分转化关系图。
②随着杂化轨道中s成分的增加,电子云更靠近原子核,核对电子的吸引力增强
(1) 又称联氨,不如氨气稳定,还原性强于氨气,与
又称联氨,不如氨气稳定,还原性强于氨气,与 反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。
反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。
①写出 用于火箭推进剂反应的化学方程式
用于火箭推进剂反应的化学方程式___________ 。
②从分子结构角度分析, 不如氨气稳定的原因是
不如氨气稳定的原因是___________ 。
(2)下列说法正确的是___________。
(3)结合已知信息,写出生成A的化学方程式___________ 。
(4)实验中在加热条件下通入过量的 与CuO反应,设计实验验证尾气中比较活泼的两种气体
与CuO反应,设计实验验证尾气中比较活泼的两种气体___________ 。

②随着杂化轨道中s成分的增加,电子云更靠近原子核,核对电子的吸引力增强
(1)
 又称联氨,不如氨气稳定,还原性强于氨气,与
又称联氨,不如氨气稳定,还原性强于氨气,与 反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。
反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。①写出
 用于火箭推进剂反应的化学方程式
用于火箭推进剂反应的化学方程式②从分子结构角度分析,
 不如氨气稳定的原因是
不如氨气稳定的原因是(2)下列说法正确的是___________。
A.以上转化关系中 只表现出还原性 只表现出还原性 |
| B.若CuO无剩余,红色固体的组分可能有三种情况 |
| C.制备氨基钠需在无水、无氧环境中进行 |
D.为了增加 的产量,往往加入过量的NaClO 的产量,往往加入过量的NaClO |
(3)结合已知信息,写出生成A的化学方程式
(4)实验中在加热条件下通入过量的
 与CuO反应,设计实验验证尾气中比较活泼的两种气体
与CuO反应,设计实验验证尾气中比较活泼的两种气体
您最近一年使用:0次
解题方法
10 . 一水硫酸四氨合铜(Ⅱ)的化学式为 是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:不正确 的是
 是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
A.操作I中发生的主要反应为: |
| B.操作II中趁热过滤除去的是难溶性杂质和氢氧化铁 |
| C.操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式 |
| D.设计操作IV的目的是为了提高乙醇的利用率 |
您最近一年使用:0次



