1 . 第十三届全国人民代表大会第四次会议政府工作报告指出“要扎实做好碳达峰、碳中和各项工作”,绿色氢能和液态阳光甲醇可助力完成碳中和目标。下列说法正确的是
A. 属于电解质 属于电解质 |
B.用焦炭与 反应是未来较好获取氢能的方法 反应是未来较好获取氢能的方法 |
C. 与 与 反应,每生成1mol 反应,每生成1mol 时转移4mol电子 时转移4mol电子 |
| D.植树造林、节能减排等有利于实现碳中和 |
您最近一年使用:0次
2021-05-20更新
|
611次组卷
|
7卷引用:考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)
(已下线)考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省永州市省重点中学2021届高三5月联考化学试题河北省沧州市2021届高考第二次模拟考试化学试题辽宁省朝阳市2021届高三第四次模拟考试化学试题(已下线)考点10 碳、硅及其无机非金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 硅及其无机非金属材料-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点12 硅及其无机非金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
解题方法
2 . 某兴趣小组对化合物X开展探究实验。

其中:X由5种短周期主族元素组成;B在标况下的密度为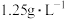 ;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)
;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)
请回答:
(1)组成X的元素除了Na、O外还有_______ (填元素符号),X的化学式是_______ 。
(2)X与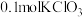 发生的反应的化学方程式是
发生的反应的化学方程式是_______ 。
(3)少量C与足量 反应也产生G,该反应的离子方程式是
反应也产生G,该反应的离子方程式是_______ 。
(4) ,F、H的阴离子相同,反应后所得溶液呈酸性,原因是
,F、H的阴离子相同,反应后所得溶液呈酸性,原因是_______ 。
(5)已知C与A加热可制备得到一种气体,请设计实验探究该气体的组成:_______ (已知该气体只有两种元素组成)。

其中:X由5种短周期主族元素组成;B在标况下的密度为
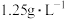 ;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)
;A的焰色反应是紫色;所有物质都是纯净物。(气体体积已折算为标况下的体积)请回答:
(1)组成X的元素除了Na、O外还有
(2)X与
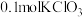 发生的反应的化学方程式是
发生的反应的化学方程式是(3)少量C与足量
 反应也产生G,该反应的离子方程式是
反应也产生G,该反应的离子方程式是(4)
 ,F、H的阴离子相同,反应后所得溶液呈酸性,原因是
,F、H的阴离子相同,反应后所得溶液呈酸性,原因是(5)已知C与A加热可制备得到一种气体,请设计实验探究该气体的组成:
您最近一年使用:0次
3 . 一定条件下双氧水与某浓度的硫酸反应过程如图所示,下列说法正确的是
HO—OH HO—OSO3H(过一硫酸)
HO—OSO3H(过一硫酸) HO3SO—OSO3H(过二硫酸)
HO3SO—OSO3H(过二硫酸)
HO—OH
 HO—OSO3H(过一硫酸)
HO—OSO3H(过一硫酸) HO3SO—OSO3H(过二硫酸)
HO3SO—OSO3H(过二硫酸)| A.生成过硫酸反应过程因硫酸的羟基被取代而呈中性 |
| B.可以用硝酸钡溶液鉴别过一硫酸和过二硫酸 |
| C.过一硫酸与过二硫酸均可做漂白剂,温度越高,漂白性越强 |
| D.等物质的量的过一硫酸与过二硫酸消耗FeSO4的量相等 |
您最近一年使用:0次
解题方法
4 . 某小组以软锰矿、闪锌矿为原料,尝试在铁钉表面镀锌及制取高纯 。流程如下:
。流程如下:

已知:①矿粉的主要成分是 、ZnS,还含有少量FeS、CuS、
、ZnS,还含有少量FeS、CuS、 等。
等。
②酸浸时反应之一: 。该生产过程中,
。该生产过程中, 与
与 不反应。
不反应。
③ 的氧化性与溶液pH有关。
的氧化性与溶液pH有关。
请回答:
(1)滤渣中加NaOH溶液可分离铁和铝,化学方程式是___________ 。
(2)下列说法正确的是___________ (填字母)。
A.可从步骤③的滤渣中回收S B.步骤⑤, 可换成
可换成
C.步骤⑥,阳极材料可选择Fe D.多次过滤分离,可提高矿石利用价值
(3)除杂时先加 后加
后加 ,原因是
,原因是___________ 。
(4)小组同学欲用下列步骤测定铁钉表面镀层的锌的质量。请选出正确操作并排序(实验只进行一次,操作不重复):
称取一定质量的铁钉,放入烧杯中→(___________)→(___________)→(___________)→(___________)→(___________),_______________
a.加过量浓硫酸
b.加过量稀硫酸
c.置于坩埚中,小火烘干
d.置于石棉网上,小火烘干
e.取出,用蒸馏水洗涤
f.搅拌,至气泡速率突然减小
g.用电子天平称量
h.用托盘天平称量
(5)测定 产品的纯度:将
产品的纯度:将 固体研细,称取一定质量的产品至锥形瓶中,依次加入过量
固体研细,称取一定质量的产品至锥形瓶中,依次加入过量 固体、足量稀
固体、足量稀 ,振荡至充分反应,再用
,振荡至充分反应,再用 标准溶液滴定剩余
标准溶液滴定剩余 至终点。
至终点。
①下列关于实验过程的说法,正确的是___________ (填字母)。
A.先在滤纸上称量好 粉末,再倒入锥形瓶
粉末,再倒入锥形瓶
B.配制 溶液时宜在棕色容量瓶中进行
溶液时宜在棕色容量瓶中进行
C.“振荡至充分反应”时,锥形瓶须加塞密封
D.滴定时的指示剂是
E.滴定终点后仰视读数,会导致 纯度偏大
纯度偏大
②读取滴定管中 溶液的示数时,因溶液颜色的干扰,凹液面最低点无法准确定位,此时可改为读取
溶液的示数时,因溶液颜色的干扰,凹液面最低点无法准确定位,此时可改为读取___________ 处的示数。
(6)电解时的总化学方程式为___________ 。
 。流程如下:
。流程如下:
已知:①矿粉的主要成分是
 、ZnS,还含有少量FeS、CuS、
、ZnS,还含有少量FeS、CuS、 等。
等。②酸浸时反应之一:
 。该生产过程中,
。该生产过程中, 与
与 不反应。
不反应。③
 的氧化性与溶液pH有关。
的氧化性与溶液pH有关。请回答:
(1)滤渣中加NaOH溶液可分离铁和铝,化学方程式是
(2)下列说法正确的是
A.可从步骤③的滤渣中回收S B.步骤⑤,
 可换成
可换成
C.步骤⑥,阳极材料可选择Fe D.多次过滤分离,可提高矿石利用价值
(3)除杂时先加
 后加
后加 ,原因是
,原因是(4)小组同学欲用下列步骤测定铁钉表面镀层的锌的质量。请选出正确操作并排序(实验只进行一次,操作不重复):
称取一定质量的铁钉,放入烧杯中→(___________)→(___________)→(___________)→(___________)→(___________),
a.加过量浓硫酸
b.加过量稀硫酸
c.置于坩埚中,小火烘干
d.置于石棉网上,小火烘干
e.取出,用蒸馏水洗涤
f.搅拌,至气泡速率突然减小
g.用电子天平称量
h.用托盘天平称量
(5)测定
 产品的纯度:将
产品的纯度:将 固体研细,称取一定质量的产品至锥形瓶中,依次加入过量
固体研细,称取一定质量的产品至锥形瓶中,依次加入过量 固体、足量稀
固体、足量稀 ,振荡至充分反应,再用
,振荡至充分反应,再用 标准溶液滴定剩余
标准溶液滴定剩余 至终点。
至终点。①下列关于实验过程的说法,正确的是
A.先在滤纸上称量好
 粉末,再倒入锥形瓶
粉末,再倒入锥形瓶B.配制
 溶液时宜在棕色容量瓶中进行
溶液时宜在棕色容量瓶中进行C.“振荡至充分反应”时,锥形瓶须加塞密封
D.滴定时的指示剂是

E.滴定终点后仰视读数,会导致
 纯度偏大
纯度偏大②读取滴定管中
 溶液的示数时,因溶液颜色的干扰,凹液面最低点无法准确定位,此时可改为读取
溶液的示数时,因溶液颜色的干扰,凹液面最低点无法准确定位,此时可改为读取(6)电解时的总化学方程式为
您最近一年使用:0次
名校
5 . 根据物质的组成、结构等信息可以预测其性质或用途。下列预测中,明显不合理 的是
A.根据化合价预测,高铜酸钠(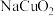 )与 )与 可生成硫酸盐 可生成硫酸盐 |
B.根据组成预测,铝酸三钙(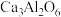 )溶于足量盐酸,生成白色沉淀 )溶于足量盐酸,生成白色沉淀 |
| C.根据在周期表中位置预测,单质砷(第ⅤA族)是重要的半导体材料 |
D.根据结构预测,葡萄糖[ ]溶液中加入新制氢氧化铜,溶液呈绛蓝色 ]溶液中加入新制氢氧化铜,溶液呈绛蓝色 |
您最近一年使用:0次
2021-05-10更新
|
524次组卷
|
3卷引用:浙江省金华十校2021届高三4月模拟考试化学试题
浙江省金华十校2021届高三4月模拟考试化学试题浙江省杭州学军中学2021-2022学年高三上学期12月适应性考试化学试题(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(精练)-2022年高考化学一轮复习讲练测
名校
解题方法
6 . 某含结晶水的盐A是制备负载型活性铁催化剂的主要原料,由五种常见元素组成,M(A)<500 g·mol−1。某兴趣小组对盐A进行了实验探究,流程如下:
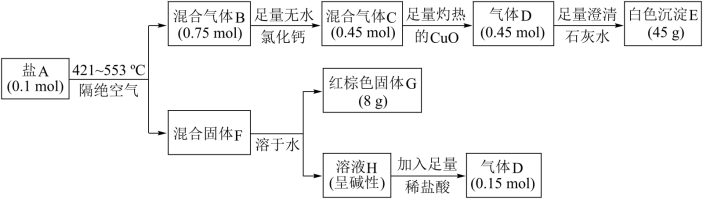
已知:①混合气体C转化为气体D时,质量增加了4.8 g;②溶液H为单一溶质,且不与氢氧化钾反应,焰色反应呈紫色。请回答:
(1)盐A除Fe、H、O以外的两种元素是_____ 。(填元素符号)
(2)混合气体C的组成成分_____ (填化学式)
(3)盐A在421~553℃下分解生成混合气体B和混合固体F的化学方程式:_____ 。
(4)盐A中加入足量稀硫酸,可得到一种二元弱酸,且该弱酸可以被酸性高锰酸钾溶液氧化生成气体D,试写出该弱酸被氧化的离子方程式:_______ 。
(5)某兴趣小组用混合气体C还原少量CuO粉末,使CuO完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:_______ 。(已知:Cu2O+2H+=Cu2++Cu+H2O)

已知:①混合气体C转化为气体D时,质量增加了4.8 g;②溶液H为单一溶质,且不与氢氧化钾反应,焰色反应呈紫色。请回答:
(1)盐A除Fe、H、O以外的两种元素是
(2)混合气体C的组成成分
(3)盐A在421~553℃下分解生成混合气体B和混合固体F的化学方程式:
(4)盐A中加入足量稀硫酸,可得到一种二元弱酸,且该弱酸可以被酸性高锰酸钾溶液氧化生成气体D,试写出该弱酸被氧化的离子方程式:
(5)某兴趣小组用混合气体C还原少量CuO粉末,使CuO完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
您最近一年使用:0次
2021-05-08更新
|
324次组卷
|
3卷引用:浙江省温州市2021届普通高中高考5月适应性测试(三模)化学试题
浙江省温州市2021届普通高中高考5月适应性测试(三模)化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)江西省景德镇市第一中学2021-2022学年高一上学期期中18班化学试题
解题方法
7 . 如图所示化合物是合成纳米管原料之一,W、X、Z、Y是原子半径逐渐减小的短周期元素,且原子序数均为奇数,Z元素无正化合价,W与Z同周期。则下列叙述正确的是


| A.液态XY3气化过程中需要破坏X和Y之间的共价键 |
| B.X的氧化物对应水化物一定为强酸 |
| C.Y元素与Na形成的二元化合物与水反应属于非氧化还原反应 |
| D.与W同主族短周期元素形成的单质可以与氢氧化钠溶液反应产生氢气 |
您最近一年使用:0次
8 . 超氧化钾(KO2)在加热条件下可以将CuO氧化成Cu(III)的化合物,化学方程式如下:2CuO+2KO2 O2↑+2KCuO2,则下列说法正确的是
O2↑+2KCuO2,则下列说法正确的是
 O2↑+2KCuO2,则下列说法正确的是
O2↑+2KCuO2,则下列说法正确的是| A.该反应中化合价升高的元素只有Cu |
| B.KCuO2既是氧化产物,又是还原产物 |
| C.当反应中转移的电子数为0.2NA时,则有0.2 mol CuO被氧化 |
| D.标准状况下,生成3.36 LO2时,被还原的超氧化钾(KO2)为0.3 mol |
您最近一年使用:0次
名校
解题方法
9 . 将38.4gCu和Fe2O3混合固体投入100mL稀硫酸中,经过充分反应后固体无剩余,向其中加入NaOH溶液至不再有沉淀生成,经过滤、洗涤、干燥和在空气中灼烧至恒重(不计损失),得到CuO和Fe2O3固体的总质量为40.0g。下列判断错误的是
| A.Cu的质量为6.4g |
| B.整个过程中转移电子的物质的量为0.4NA |
| C.加入NaOH的物质的量恰好是H2SO4的物质的量2倍 |
| D.固体恰好溶解时CuSO4的物质的量浓度为1mol/L |
您最近一年使用:0次
解题方法
10 . 由三种元素组成的化合物X,按如下流程进行实验。气体A是由气体E和气体F组成的混合物,溶液B可被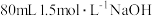 溶液恰好中和。
溶液恰好中和。

请回答:
(1)组成X的三种元素是___________ (真元素符号),X的化学式是___________ 。
(2)步骤I发生反应的离子方程式是___________ 。
(3)Mg在气体E中剧烈燃烧生成两种固体化合物,该反应的化学方程式是___________ 。
(4)步骤II,为使铜片进一步溶解,可向反应后的混合物中加入___________ (填序号)。
①稀 ②
② ③
③ ④
④
(5)将体积比为 的气体E和
的气体E和 的混合气体通入水中制得Y的浓溶液。该浓溶液与Cu反应得到绿色溶液,有同学认为溶液呈绿色是因为溶有气体E,设计实验方案证明
的混合气体通入水中制得Y的浓溶液。该浓溶液与Cu反应得到绿色溶液,有同学认为溶液呈绿色是因为溶有气体E,设计实验方案证明___________ 。
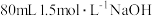 溶液恰好中和。
溶液恰好中和。
请回答:
(1)组成X的三种元素是
(2)步骤I发生反应的离子方程式是
(3)Mg在气体E中剧烈燃烧生成两种固体化合物,该反应的化学方程式是
(4)步骤II,为使铜片进一步溶解,可向反应后的混合物中加入
①稀
 ②
② ③
③ ④
④
(5)将体积比为
 的气体E和
的气体E和 的混合气体通入水中制得Y的浓溶液。该浓溶液与Cu反应得到绿色溶液,有同学认为溶液呈绿色是因为溶有气体E,设计实验方案证明
的混合气体通入水中制得Y的浓溶液。该浓溶液与Cu反应得到绿色溶液,有同学认为溶液呈绿色是因为溶有气体E,设计实验方案证明
您最近一年使用:0次



