1 . 原电池是将化学能转化为电能的装置,某兴趣小组利用数据采集器和传感器等仪器对原电池进行实验探究。
I.能量变化探究
将上表的现象和结论补充完整
(1)_____________
(2)__________ 、__________
II.原电池电压影响因素的测定
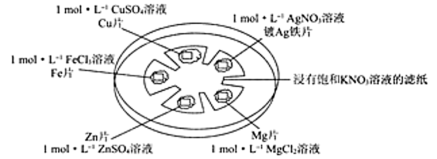
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。
(3)准确配制一定物质的量浓度的溶液时,操作X应在__________ (填字母)之间。
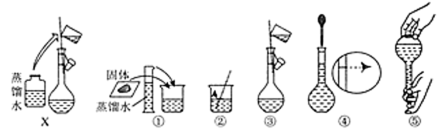
A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为_________________ 。
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表__________ (填“正”或“负”)极,预测表中Ag和Zn相连接时,测得电压的数值a可能的范围为____________ ;Fe和Mg相连接时,Z极的电极反应式为__________ ,Y极的电极反应式为____________ 。
I.能量变化探究
| 实验操作 | 数据及图象 | 现象与结论 |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,向其中加入1g镁粉 | 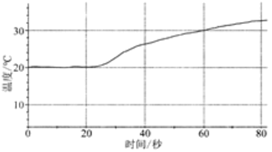 | (1)反应过程中,化学能直接转化为 能; |
| 将60mL1mol/LCuSO4溶液置于100mL烧杯中,平行插入铜片和镁片,与电流传感器形成闭合回路 | 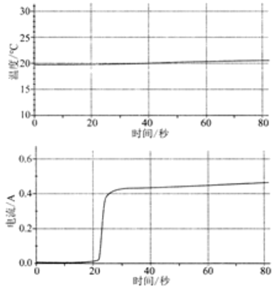 | (2)体系温度变化很小,原因是 ;反应过程中,镁片和铜片的质量变化分别为: ; |
(1)
(2)
II.原电池电压影响因素的测定
如图所示,在培养皿中进行微型实验,用浸有饱和KNO3溶液的滤纸充当盐桥,在滤纸间隔位置放置金属片,并滴三滴相应溶液,用电压传感器的两个探头分别与不同的金属表面接触形成闭合回路,测定电压。

(3)准确配制一定物质的量浓度的溶液时,操作X应在

A.②③ B.③④ C.④⑤
(4)以上五种金属的活动性由活泼到不活泼的顺序为
(5)实验条件下,连接不同金属片时所得数据见下表,表中Y极代表
| Y极 | Z极 | 测得电压/V |
| Ag | Fe | 1.009 |
| Ag | Zn | a |
| Ag | Mg | 2.114 |
| Fe | Zn | 0.473 |
| Fe | Mg | 1.111 |
| Zn | Mg | 0.636 |
您最近一年使用:0次
解题方法
2 . 实验小组的同学们将三种金属按照下表的装置进行实验。回答问题:
(1)装置甲中铁极的电极反应式是____________ ,溶液中H+向_____ 极移动(填“正”或“负”)。
(2)装置乙中铜极发生____________ (填“氧化”或“还原”)反应。
(3)装置丙中M极为______ (填“正极”或“负极”),一段时间后溶液的酸性_____________ (填“增强”“减弱”或“不变”)。
(4)Fe、Cu、M中金属活动性最强的是_____________ 。
| 序号 | 甲 | 乙 | 丙 |
| 装置 |  | 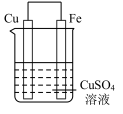 | 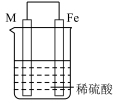 |
| 现象 | 溶液变为浅绿色,Cu极产生大量气泡 | Cu极的质量增加 | M极的质量减少 |
(1)装置甲中铁极的电极反应式是
(2)装置乙中铜极发生
(3)装置丙中M极为
(4)Fe、Cu、M中金属活动性最强的是
您最近一年使用:0次
2020-08-08更新
|
115次组卷
|
3卷引用:青海省西宁市2019-2020学年高一下学期期末调研测试化学试题
解题方法
3 . 如图所示装置:
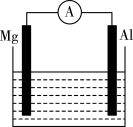
(1)若烧杯中溶液为稀硫酸,则观察到的现象为________ 。两极反应式为:正极________ ;负极________ 。该装置将________ 能转化为________ 能,原电池中的H+向______ (Mg、Al)极移动。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________ ,带_______ (正、负)电;总反应方程式为________ 。

(1)若烧杯中溶液为稀硫酸,则观察到的现象为
(2)若烧杯中溶液为氢氧化钠溶液,则负极为
您最近一年使用:0次
解题方法
4 . 已知可逆反应: 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
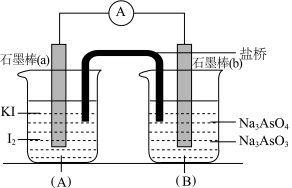
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:____________________________________ 。
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为____________________________________ 。
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为____________________________________ 。
 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为
您最近一年使用:0次
5 . (1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1molN2中的 键需要吸收
键需要吸收 能量;破坏
能量;破坏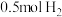 中的
中的 键需要吸收
键需要吸收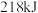 能量;形成
能量;形成 中的
中的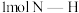 键能释放
键能释放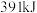 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
①________________  ,②
,②____________________  。
。

(2)用A、B、C、D四种金属按如表所示的装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为__________________ 。
②装置乙中正极的电极反应式为________________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是________ 。
(3)一定温度下,在体积为 的恒容密闭容器中充入
的恒容密闭容器中充入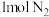 和
和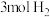 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
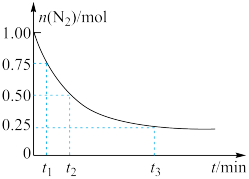
从开始反应到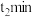 ,用
,用 表示的化学反应速率为
表示的化学反应速率为_________ 。
 键需要吸收
键需要吸收 能量;破坏
能量;破坏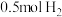 中的
中的 键需要吸收
键需要吸收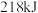 能量;形成
能量;形成 中的
中的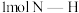 键能释放
键能释放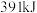 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。①
 ,②
,② 。
。
(2)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 |  甲 |  乙 |  丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为
 的恒容密闭容器中充入
的恒容密闭容器中充入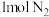 和
和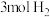 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
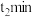 ,用
,用 表示的化学反应速率为
表示的化学反应速率为
您最近一年使用:0次
2020-09-24更新
|
676次组卷
|
3卷引用:鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 章末综合检测卷
名校
解题方法
6 . “水”电池是一种利用淡水与海水之间含盐量差别进行发电的电池,其总反应为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,如图以“水”电池为电源电解酸性FeCl2溶液,X电极附近溶液先变黄,下列有关分析不正确的是( )
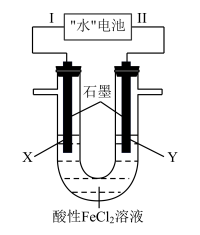

| A.该装置只涉及两种能量之间的转化 |
| B.在线路中安装电压调节装置,可通过现象判断Fe2+和Cl-的还原性强弱 |
| C.“水”电池内Na+不断向正极移动 |
| D.Ⅱ为负极,其电极反应式为Ag+Cl--e-=AgCl |
您最近一年使用:0次
2020-07-08更新
|
75次组卷
|
3卷引用:安徽省太和第一中学2019-2020学年高一下学期期末考试化学试题
名校
解题方法
7 . 由下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Co2O3中滴加浓盐酸 | 产生黄绿色气体 | 氧化性:Cl2>Co2O3 |
| B | 在镁、铝为电极,氢氧化钠为电解质的原电池装置 | 镁表面有气泡 | 金属活动性:Al>Mg |
| C | 测定等物质的量浓度的NaCl与Na2CO3溶液的pH | 后者较大 | 非金属性:Cl>C |
| D | 将10 mL 2 mol/L的KI溶液与1 mL 1 mol/L FeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题(用符号A、B、C、D回答下列问题)
(1)装置甲中负极 为___ 。装置丙中负极 为__ 。
(2)装置乙中正极 的电极反应式是___ 。
(3)四种金属活泼性由强到弱 的顺序是___ 。
| 装置 |  甲 甲 |  乙 乙 |  丙 丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题(用符号A、B、C、D回答下列问题)
(1)装置甲中
(2)装置乙中
(3)四种金属活泼性
您最近一年使用:0次
解题方法
9 . 由下列实验操作和现象得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Co2O3中滴加浓盐酸 | 产生黄绿色气体 | 氧化性:Cl2<Co2O3 |
| B | 在镁、铝为电极,氢氧化钠为电解质的原电池装置 | 镁表面有气泡 | 金属活动性:Al>Mg |
| C | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟 | X可能是浓盐酸 |
| D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN溶液 | 溶液颜色变红 | KI与FeCl3的反应具有可逆性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-09-24更新
|
175次组卷
|
2卷引用:湖北省龙泉中学、荆州中学、宜昌一中2021届高三9月联考化学试题
名校
解题方法
10 . 对右图所示的装置中实验现象的描述正确的是
| 选项 | a电极 | b电极 | X溶液 | 实验现象 | 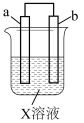 |
| A | 石墨 | 石墨 | CuCl2溶液 | a极质量增加,b极放出无色气体 | |
| B | Cu | Fe | KNO3溶液 | a极质量增加,b极放出无色气体 | |
| C | 石墨 | Fe |  溶液 溶液 | a极质量增加,b极质量减小 | |
| D | 石墨 | Zn | HCl溶液 | a放出无色气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



