名校
解题方法
1 . 请回答下列问题:
(1)铅酸蓄电池是一种可充电电池,其总反应式为Pb+PbO2+2H2SO4 2PbSO4+2H2O,原电池负极的电极反应式为
2PbSO4+2H2O,原电池负极的电极反应式为_______ ,正极附近溶液的pH_______ (填“增大”、“不变”或“减小”)。
(2)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ ,写出正极的电极反应式_______ 。若开始时两极质量相等,当导线中通过0.2mol电子时,两个电极的质量差为_______ 。
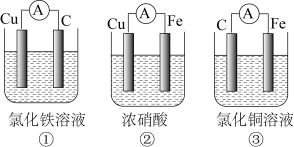
(3)乙醇燃料电池技术方面获得新突破,乙醇(CH3CH2OH)燃料电池的工作原理如图所示。
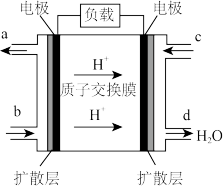
①该电池工作时,c入口处对应的电极为_______ (填“正”或“负”)极,b处入口的物质为_______
②工作一段时间后,当2.3 g乙醇完全反应生成CO2时,外电路中通过的电子数目为_______ 。
(1)铅酸蓄电池是一种可充电电池,其总反应式为Pb+PbO2+2H2SO4
 2PbSO4+2H2O,原电池负极的电极反应式为
2PbSO4+2H2O,原电池负极的电极反应式为(2)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
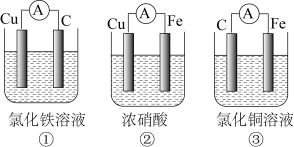
(3)乙醇燃料电池技术方面获得新突破,乙醇(CH3CH2OH)燃料电池的工作原理如图所示。

①该电池工作时,c入口处对应的电极为
②工作一段时间后,当2.3 g乙醇完全反应生成CO2时,外电路中通过的电子数目为
您最近一年使用:0次
2022-11-02更新
|
537次组卷
|
2卷引用:重庆市璧山来凤中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
2 . 化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,而许多能量的利用与化学反应中的能量变化密切相关。
I.完成下列问题
(1)H2(g) +Cl2(g)=2HCl(g)的反应过程如图所示:
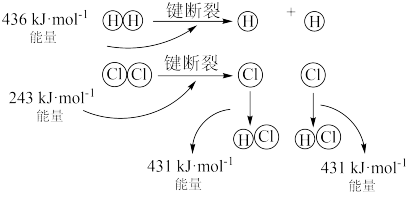
该反应为_______ (填“放热”或“吸热”)反应,其吸收或放出的热量为_______ 。
(2)下列变化中属于吸热反应的是_______ (填序号)。
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④生石灰与水反应生成熟石灰
⑤CO2 +C 2CO
2CO
⑥Ba(OH)2·8H2O与固体NH4Cl混合
⑦C+ H2O(g)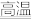 CO+ H2
CO+ H2
⑧Al与盐酸反应
(3)某化学反应中,设反应物的总能量为E1,生成物的总能量为E2。
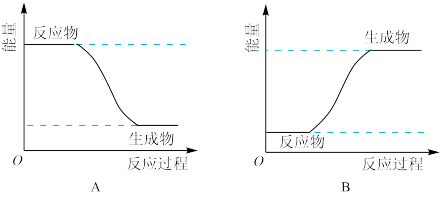
若E1>E2,则该反应可用图_______ (填“A”或“B")表示。
Ⅱ.回答下列问题
(4)为了验证Fe2+与Cu2+的氧化性强弱,如图装置能达到实验目的的是_______ (填装置序号),其正极的电极反应式为_______ ;若构建该原电池时两个电极的质量相等,当导线中通过0.4mol电子时,两个电极的质量差为_______ g。
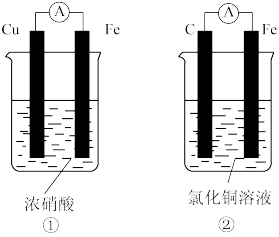
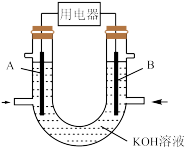
将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则_______ (填“A”或“B”)处电极入口通CH4,其电极反应式为_______ 。
I.完成下列问题
(1)H2(g) +Cl2(g)=2HCl(g)的反应过程如图所示:

该反应为
(2)下列变化中属于吸热反应的是
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④生石灰与水反应生成熟石灰
⑤CO2 +C
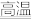 2CO
2CO⑥Ba(OH)2·8H2O与固体NH4Cl混合
⑦C+ H2O(g)
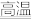 CO+ H2
CO+ H2⑧Al与盐酸反应
(3)某化学反应中,设反应物的总能量为E1,生成物的总能量为E2。

若E1>E2,则该反应可用图
Ⅱ.回答下列问题
(4)为了验证Fe2+与Cu2+的氧化性强弱,如图装置能达到实验目的的是

将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得OH-定向移向A电极,则

您最近一年使用:0次
名校
解题方法
3 . 下列实验装置和操作能达到实验目的或者对实验装置中的现象描述正确的是
A.+测定化学反应速率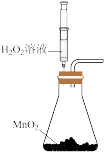 | B.锌被腐蚀、铜片上有气泡产生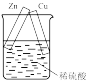 | C.探究不同催化剂对反应速率的影响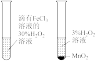 | D.组装原电池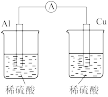 |
您最近一年使用:0次
2018-09-06更新
|
197次组卷
|
2卷引用:2018-2019学年苏教版高中化学必修二:专题综合测评2 化学反应与能量转化
4 . 用如图所示装置进行相应实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 | 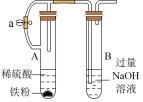 |  | 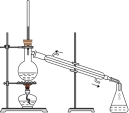 | 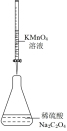 |
| 目的 | 制取 沉淀 沉淀 | 将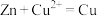 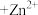 设计成原电池装置 设计成原电池装置 | 分离苯和硝基苯 | 测定 溶液的物质的量浓度 溶液的物质的量浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-18更新
|
1279次组卷
|
4卷引用:湖北省2022届高三5月联考化学试题
湖北省2022届高三5月联考化学试题(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题 吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题
5 . 利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体积已转换为标准状况。下列说法正确的是
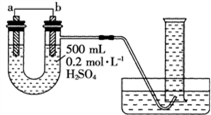

| A.a电极的电极材料是铜 |
| B.如果将稀硫酸换为CuSO4溶液,则不能达到实验目的 |
| C.锌与稀硫酸反应时放出的热量对实验测定不产生影响 |
| D.若量筒中收集到aLH2,则电解质溶液中通过了a/11.2mol电子 |
您最近一年使用:0次
2017-06-13更新
|
305次组卷
|
3卷引用:甘肃省天水市第一中学2016-2017学年高一下学期第二次月考(B卷)化学试题
名校
6 . I.为了探究原电池的工作原理,某研究性学习小组进行了如下实验。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
Ⅱ.化学反应 的能量变化如图所示。
的能量变化如图所示。_______ (填“能”或“不能”)将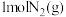 和
和 全部转化为
全部转化为 。
。
(4)该反应属于_______ (填“吸热”或“放热”)反应。
(5)一定量的 和
和 充分反应生成
充分反应生成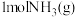 时,释放
时,释放_______  能量。
能量。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。

A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向

D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
A.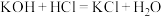 |
B. |
C. |
D.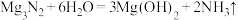 |
Ⅱ.化学反应
 的能量变化如图所示。
的能量变化如图所示。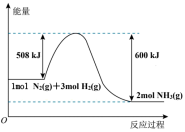
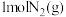 和
和 全部转化为
全部转化为 。
。(4)该反应属于
(5)一定量的
 和
和 充分反应生成
充分反应生成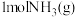 时,释放
时,释放 能量。
能量。
您最近一年使用:0次
名校
解题方法
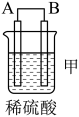
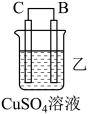
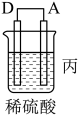
7 . 化学能还可以转化为电能,由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)外电路中电流由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)外电路中电流由
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
8 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
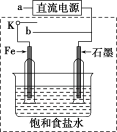
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
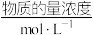 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近一年使用:0次
解题方法
9 . 如图是牺牲阳极法保护金属的实验装置图,烧杯内为经过酸化的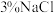 溶液。
溶液。
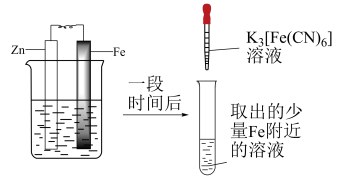
下列关于该装置的叙述错误的是
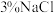 溶液。
溶液。
下列关于该装置的叙述错误的是
| A.铁作正极被保护 |
B.将 换成 换成 ,也可以保护铁不被腐蚀 ,也可以保护铁不被腐蚀 |
C.向试管中加入 溶液,无明显现象 溶液,无明显现象 |
D.正极反应式为 |
您最近一年使用:0次
名校
解题方法
10 . 人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_______(填字母,下同)。
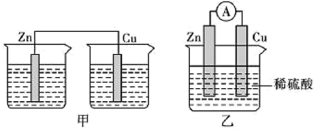
(2)为了探究原电池的工作原理,某研究性学习小组进行了如下实验。分别按图1中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
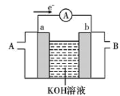
(3)某氢氧燃料电池装置如图所示,a、b均为惰性电极。_______ (填“A”或“B”)口通入。
②负极上的电极反应式为_______ ,当电路中转移 电子时,理论上负极通入的气体在标准状况下的体积为
电子时,理论上负极通入的气体在标准状况下的体积为_______ L。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_______(填字母,下同)。
A. 与 与 反应 反应 | B.氢氧化钠与稀盐酸反应 |
C.灼热的炭与 反应 反应 | D. 与 与 燃烧反应 燃烧反应 |
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(3)某氢氧燃料电池装置如图所示,a、b均为惰性电极。
②负极上的电极反应式为
 电子时,理论上负极通入的气体在标准状况下的体积为
电子时,理论上负极通入的气体在标准状况下的体积为
您最近一年使用:0次