解题方法
1 . 图为某化学兴趣小组探究不同条件下化学能转变为电能的装置。根据原电池原理回答问题:
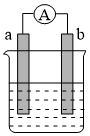
(1)若电极a为Zn、电极b为Cu、电解质溶液为稀硫酸,该装置工作时,Cu电极上的可以看到的现象___ ,SO 向
向____ 极(填a或b)移动,正极的电极反应式为___ 。
(2)若电极a为Fe、电极b为Ag、电解质溶液为硝酸银,该原电池工作时,原电池的负极材料为___ ,电子沿导线向___ (填a/b)移动。
(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2)请将此反应设计成原电池,该原电池负极的电极材料为___ ,正极的电极材料为____ ,电解质溶液为___ ,负极的电极反应式为___ 。

(1)若电极a为Zn、电极b为Cu、电解质溶液为稀硫酸,该装置工作时,Cu电极上的可以看到的现象
 向
向(2)若电极a为Fe、电极b为Ag、电解质溶液为硝酸银,该原电池工作时,原电池的负极材料为
(3)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2)请将此反应设计成原电池,该原电池负极的电极材料为
您最近一年使用:0次
解题方法
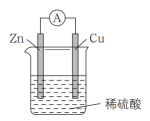
2 . 实验室中,学生利用下图装置制作一个简单燃料电池。步骤如下:

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到_______ 。
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的_______ (填“正极”或“负极”),该石墨表面的电极方程式是_______ 。
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与_______ (填“左”或“右”)侧的石墨棒连接的导线相连。
(4)出现_______ 的现象,证明该燃料电池制作成功。燃料电池正极的电极方程式是_______ 。

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与
(4)出现
您最近一年使用:0次
3 . 原电池是直接把化学能转化为电能的装置。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)____ ;稀硫酸的作用是________ 。
a.负极反应物 b.负极材料 c.正极反应物
d.正极材料 e.离子导体 f.电子导体
(2) ①在Cu-Zn原电池中,Zn片上发生________ 反应(填“氧化”或“还原”)。Cu片上发生的电极反应为________ 。
②外电路中电子流向_____ 极;内电路溶液中SO 移向
移向___ 极。
③能证明化学能转化为电能的实验现象为________ 。
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是__ 。

(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将________ ,并通过能导电的物质形成闭合回路,产生电流。
(1)如图所示:按照构成原电池的基本要素来看,Zn的作用是(填字母,下同)

a.负极反应物 b.负极材料 c.正极反应物
d.正极材料 e.离子导体 f.电子导体
(2) ①在Cu-Zn原电池中,Zn片上发生
②外电路中电子流向
 移向
移向③能证明化学能转化为电能的实验现象为
(3)某原电池的总反应为Zn+Cu2+=Cu+Zn2+,该原电池正确的组成是

(4)从化学的角度分析,原电池装置产生电流的原因是:原电池可将
您最近一年使用:0次
解题方法
4 . 课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
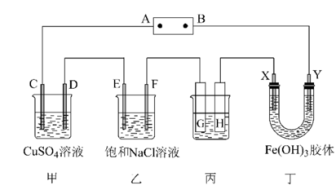
(1)电源A极的名称是___________ 。
(2)甲装置中在两极分别滴加紫色石蕊溶液,有现象的是___________ (填电极符号)。
(3)如果收集乙装置中产生的气体,两种气体的体积比是___________ 。
(4)欲用丙装置给铜镀银,G应该是___________ (填“铜”或“银”),电镀液的主要成分是___________ (填化学式)。
(5)若丙装置的两极产生气体的质量比为1∶8,则丙中的溶液可以为___________ (填化学式)。

(1)电源A极的名称是
(2)甲装置中在两极分别滴加紫色石蕊溶液,有现象的是
(3)如果收集乙装置中产生的气体,两种气体的体积比是
(4)欲用丙装置给铜镀银,G应该是
(5)若丙装置的两极产生气体的质量比为1∶8,则丙中的溶液可以为
您最近一年使用:0次
5 . 根据如图所示的装置,完成下列各空。
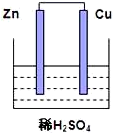
(1)该装置中的总反应式为___________ 。
(2)溶液中的H+移向___________ (填“Cu片”或“Zn片”)
(3)Zn电极的反应式为___________ ,发生 ___________ 反应,(填“氧化”或“还原”)
(4)Cu片为原电池的___________ 极(填“正”或“负”),现象为___________ 。

(1)该装置中的总反应式为
(2)溶液中的H+移向
(3)Zn电极的反应式为
(4)Cu片为原电池的
您最近一年使用:0次
名校
6 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置乙中正极的电极反应式是_______ 。
(2)四种金属活动性由强到弱的顺序是_______ 。
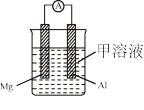
(3)Mg、Al设计成如图所示原电池装置:若电解液为盐酸,正极的电极反应为___ 。若电解液为氢氧化钠溶液,负极的电极反应为___ 。
| 装置 | 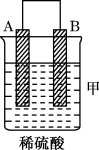 | 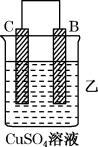 | 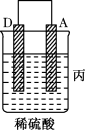 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置乙中正极的电极反应式是
(2)四种金属活动性由强到弱的顺序是
(3)Mg、Al设计成如图所示原电池装置:若电解液为盐酸,正极的电极反应为

您最近一年使用:0次
名校
解题方法
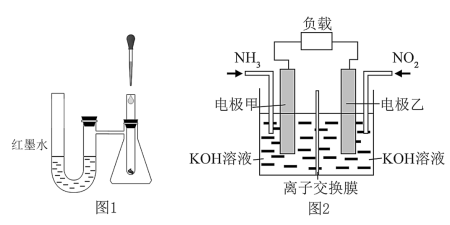
7 . (1)为了探究化学反应的热效应,某兴趣小组采用如图1所示装置进行实验:将稀盐酸滴入装入铁粉的试管中,U形管内的现象为_____ ,发生的反应是_____ (填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是_______ (填字母)。
A.盐酸与碳酸氢钠的反应B.CaCO3的分解反应
C.食物的缓慢氧化D.Ba(OH)2•8H2O和NH4Cl的反应
E.H2和Cl2的反应
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为_____ 。
A.铝片、铝片B.铜片、铜片C.铝片、铜片D.铜片、铝片
(3)雾霾中含有氮的氧化物,利用反应NO2+NH3→N2+H2O(未配平)制作如图2所示的电池,用以消除氮氧化物的污染。电极甲是_____ 极,电池工作时,OH-定向移向______ 电极(填“甲”或“乙”),写出负极电极反应式:_____ ,若一段时间内测得外电路中有1.2mol电子通过,则负极比正极产生的气体多____ L(标准状况下)。
A.盐酸与碳酸氢钠的反应B.CaCO3的分解反应
C.食物的缓慢氧化D.Ba(OH)2•8H2O和NH4Cl的反应
E.H2和Cl2的反应

(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铝片B.铜片、铜片C.铝片、铜片D.铜片、铝片
(3)雾霾中含有氮的氧化物,利用反应NO2+NH3→N2+H2O(未配平)制作如图2所示的电池,用以消除氮氧化物的污染。电极甲是
您最近一年使用:0次
8 . 由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)装置乙溶液中C电极反应:_______ ;外电路中电子由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 | 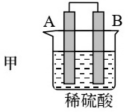 | 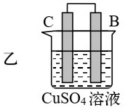 | 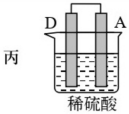 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)装置乙溶液中C电极反应:
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
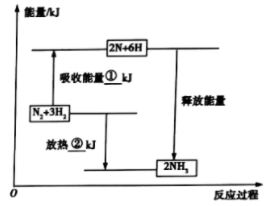
9 . (1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1mol氮气中的化学键需要吸收946kJ能量;破坏0.5mol氢气中的 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
①______ kJ,②_____ kJ。
(2)由A、B、C、D四种金属按如表所示装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为_______________ 。
②装置乙中正极的电极反应式为_______________ 。
③装置丙中溶液的pH_________ (填“变大”“变小”或“不变”)
④四种金属的活动性由强到弱的顺序是____________ 。
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: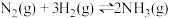 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
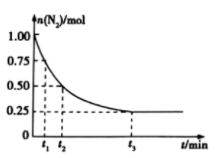
从开始反应到 min,氮气的平均反应速率为
min,氮气的平均反应速率为_________ 。
 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。①

(2)由A、B、C、D四种金属按如表所示装置进行实验。
| 装置 | 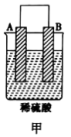 | 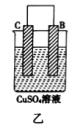 | 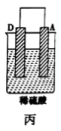 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol
 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: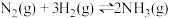 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
 min,氮气的平均反应速率为
min,氮气的平均反应速率为
您最近一年使用:0次
名校
解题方法
10 . 电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。
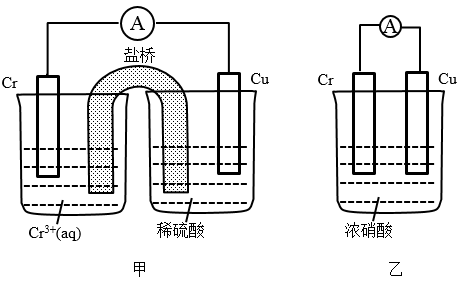
(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜__ (填“强”或“弱”);由装置乙知常温下铬在浓硝酸中出现__ 现象。
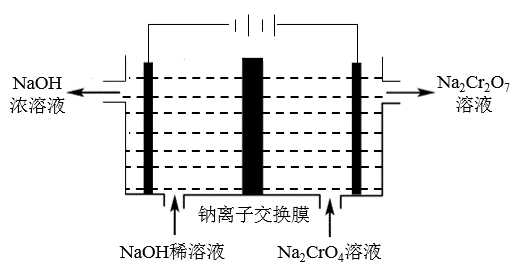
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为__ 。
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为__ 。阴极上Cr2O 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为__ ;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=___ 。
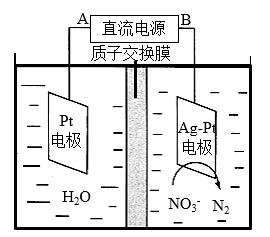
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为___ g。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为

(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O
 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为

您最近一年使用:0次



