名校
1 . 短周期元素X和Y,可组成化合物XY3。当X的原子序数为a时,Y的原子序数可能是:①a+2,②a+4,③a+8,④a+12,⑤a-6,其中正确的组合是
| A.①② | B.①②③ | C.①②③⑤ | D.①②④⑤ |
您最近一年使用:0次
2017-04-14更新
|
679次组卷
|
3卷引用:2016-2017学年四川省成都市九校高一下学期期中联考化学试卷
2 . Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,Q元素的原子最外层电子数是其内层电子数的2倍,W、Z原子最外层电子数相同,Z的核电荷数是W的2倍,元素Y的合金是日常生活中使用最广泛的金属材料之一、下列说法正确的是
| A.简单离子半径的大小顺序:rX>rY>rZ>rW |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.Z元素氢化物的沸点高于W元素氢化物的沸点 |
| D.X、Y、Z最高价氧化物的水化物之间两两不能发生反应 |
您最近一年使用:0次
3 . 镁、钡是位于同一主族的活泼的金属元素。
回答下列问题:
(1)镁在元素周期表中的位置是:______________ ;钡位于周期表第六周期,钡原子最外层电子的电子排布式是:________ 。
(2)铝也是一种活泼金属,铝的金属性比钡的_____ (填“强”或“弱”)。工业上可用如下方法制取钡:2Al+4BaO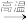 3Ba↑+BaO·Al2O3,该法制钡的主要原因是
3Ba↑+BaO·Al2O3,该法制钡的主要原因是______ (选填选项)
a.高温时Al的活泼性大于Ba b.高温时BaO·Al2O3比Al2O3稳定
c.Ba的沸点比Al的低 d.高温有利于BaO分解
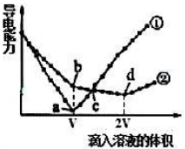
两个烧杯分别盛有VmL、c mol/L的Ba(OH)2溶液,分别向其中滴入c mol/L的H2SO4 和NaHSO4溶液,两烧杯中溶液导电能力随滴入溶液体积的变化分别如下图中①、②所示。
(3)写出Ba(OH)2溶液与H2SO4恰好反应的离子方程式:___________ 。
(4)写出b点溶液中大量存在的阴离子的电子式:_________ 。
(5)a、b、c、d点溶液呈中性的是____________________ 。
回答下列问题:
(1)镁在元素周期表中的位置是:
(2)铝也是一种活泼金属,铝的金属性比钡的
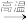 3Ba↑+BaO·Al2O3,该法制钡的主要原因是
3Ba↑+BaO·Al2O3,该法制钡的主要原因是a.高温时Al的活泼性大于Ba b.高温时BaO·Al2O3比Al2O3稳定
c.Ba的沸点比Al的低 d.高温有利于BaO分解
两个烧杯分别盛有VmL、c mol/L的Ba(OH)2溶液,分别向其中滴入c mol/L的H2SO4 和NaHSO4溶液,两烧杯中溶液导电能力随滴入溶液体积的变化分别如下图中①、②所示。
(3)写出Ba(OH)2溶液与H2SO4恰好反应的离子方程式:
(4)写出b点溶液中大量存在的阴离子的电子式:
(5)a、b、c、d点溶液呈中性的是
您最近一年使用:0次
名校
4 . 已知短周期元素的离子,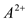 ,
, ,
, ,
,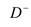 都具有相同的电子层结构,则下列叙述正确的是
都具有相同的电子层结构,则下列叙述正确的是
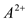 ,
, ,
, ,
,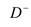 都具有相同的电子层结构,则下列叙述正确的是
都具有相同的电子层结构,则下列叙述正确的是| A.原子半径A>B>D>C | B.原子序数D>C>B>A |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
您最近一年使用:0次
2017-04-05更新
|
1507次组卷
|
2卷引用:2016-2017学年山东省济南第一中学高一3月阶段性考试化学试卷
名校
5 . 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
_________ 与盐酸反应最剧烈;________ 与盐酸反应的速度最慢;_________ 与盐酸反应产生的气体最多。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由___________ 。
II. 利用如图装置可验证同主族元素非金属性的变化规律。
(3)仪器B的名称为________ ,干燥管D的作用为_______ 。
(4)若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_______ 溶液吸收尾气。
(5)若要证明非金属性C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液_____ (填现象),即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有________ 溶液的洗气瓶除去。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由
II. 利用如图装置可验证同主族元素非金属性的变化规律。
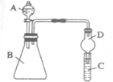
(3)仪器B的名称为
(4)若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近一年使用:0次
2017-04-01更新
|
586次组卷
|
2卷引用:2016-2017学年山东省枣庄市第八中学北校区高一下学期第一次月考化学试卷
6 . (I)俄美科学家联合小组宣布合成出114号元素(FI)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中位于第______ 周期,_____ 族,属于金属元素还是非金属元素?____
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式________ 。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为__________ 。
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为___________ 。
(3)元素⑩的单质与⑦的氢化物高温下反应的化学方程式为___________ 。
(III)判断以下叙述正确的是__________ 。
部分短周期元素的原子半径及主要化合价
A. L2+、R2-的核外电子数相等
B. 单质与稀盐酸反应的速率L<Q
C. M与T形成的化合物一定具有两性
D. 氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中位于第
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
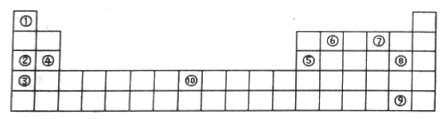
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为
(3)元素⑩的单质与⑦的氢化物高温下反应的化学方程式为
(III)判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A. L2+、R2-的核外电子数相等
B. 单质与稀盐酸反应的速率L<Q
C. M与T形成的化合物一定具有两性
D. 氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
7 . 下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)______ ,离子半径最小的是____ (写元素符号)。
(2)J的简单离子的结构示意图__________ 。
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)____ 。
(4)比较G、H两元素的最高价氧化物对应水化物的酸性______ (写化学式,下同)。比较C、G两元素的气态氢化物稳定性_________ 。
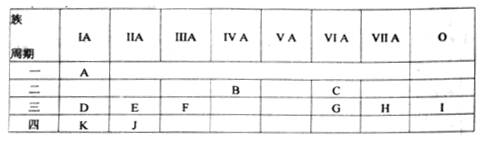
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)
(2)J的简单离子的结构示意图
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)
(4)比较G、H两元素的最高价氧化物对应水化物的酸性
您最近一年使用:0次
8 . X、Y、Z是一种短周期元素,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生右下图转化关系.其中R为10电子分子,是一种常见的无机溶剂。下列说法中不正确的是
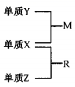
| A.X元素位于周期表中第16列 |
| B.X、Y、Z元素两两之间均能形成原子个数比为l:1的化合物 |
| C.X、Y、Z元素形成的单质均具有强还原性 |
| D.R的沸点高于M的沸点 |
您最近一年使用:0次
2017-03-31更新
|
1387次组卷
|
4卷引用:2017届河南省郑州、平顶山、濮阳市高三第二次质量预测(二模)理综化学试卷
名校
9 . A为ⅡA主族元素,B为ⅢA主族元素,A、B同周期,其原子序数分别为M,N,甲乙为同一主族相邻元素,其原子序数分别为X、Y。则下列选项中的两个关系式均正确的是:
| A.N=M+10 Y=X+2 | B.N=M+11 Y=X+4 | C.N=M+25 Y=X+8 | D.N=M+10 Y=X+18 |
您最近一年使用:0次
名校
10 . 已知W、X、Y、Z为短周期元素,原子序数依次增大。W、Z同主族,X、Y、Z同周期,其中只有X为金属元素。下列说法一定正确的是
| A.简单离子半径:W > X |
| B.含氧酸的酸性:W > Z |
| C.气态氢化物的稳定性:W < Y |
| D.若W与X原子序数差为5,则形成化合物的化学式为X3W2 |
您最近一年使用:0次
2017-03-27更新
|
889次组卷
|
3卷引用:2017届山东省济南市高三第一次模拟考试理科综合化学试卷



