名校
解题方法
1 . 海洋中蕴含着丰富的资源,海水中 的含量约为67mg/L,海洋植物如海带、海藻中含有丰富的碘元素(以
的含量约为67mg/L,海洋植物如海带、海藻中含有丰富的碘元素(以 的形式存在),实验室里从海藻中提取碘的流程如图所示。
的形式存在),实验室里从海藻中提取碘的流程如图所示。___________ 中进行,操作②后得到“浸取液”的操作是___________ 。
(2)操作③中发生反应的离子方程式为___________ ﹔该操作温度不宜过高的原因是___________ 。
(3)操作⑥是 ,
, 与45%的
与45%的 溶液反应,写出该反应的离子方程式:
溶液反应,写出该反应的离子方程式:___________ 。
(4)碘盐中添加 ,可以预防甲状腺肿。碘酸钾的某种制取工艺流程如图所示。
,可以预防甲状腺肿。碘酸钾的某种制取工艺流程如图所示。___________ 。
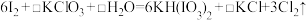
②X的化学式为___________ 。
③测定产品纯度:称取wg产品溶于蒸馏水,滴加适量稀硫酸,加入 溶液恰好完全反应,发生反应:
溶液恰好完全反应,发生反应: (未配平)。根据上述数据,测得产品中碘元素质量分数为
(未配平)。根据上述数据,测得产品中碘元素质量分数为___________ (用含w,c、V的表达式表示)。
 的含量约为67mg/L,海洋植物如海带、海藻中含有丰富的碘元素(以
的含量约为67mg/L,海洋植物如海带、海藻中含有丰富的碘元素(以 的形式存在),实验室里从海藻中提取碘的流程如图所示。
的形式存在),实验室里从海藻中提取碘的流程如图所示。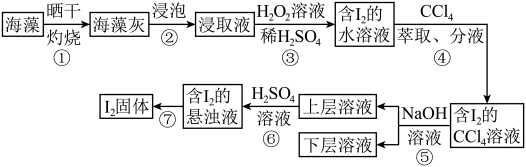
(2)操作③中发生反应的离子方程式为
(3)操作⑥是
 ,
, 与45%的
与45%的 溶液反应,写出该反应的离子方程式:
溶液反应,写出该反应的离子方程式:(4)碘盐中添加
 ,可以预防甲状腺肿。碘酸钾的某种制取工艺流程如图所示。
,可以预防甲状腺肿。碘酸钾的某种制取工艺流程如图所示。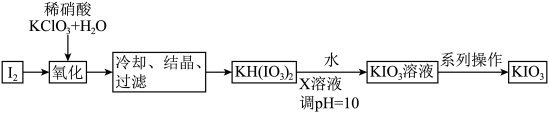
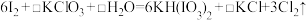
②X的化学式为
③测定产品纯度:称取wg产品溶于蒸馏水,滴加适量稀硫酸,加入
 溶液恰好完全反应,发生反应:
溶液恰好完全反应,发生反应: (未配平)。根据上述数据,测得产品中碘元素质量分数为
(未配平)。根据上述数据,测得产品中碘元素质量分数为
您最近一年使用:0次
2024-07-30更新
|
65次组卷
|
2卷引用:河南省郑州市中牟县2023-2024学年高一下学期期末考试化学试题
名校
解题方法
2 . 碘单质及其化合物具有重要应用。下列说法正确的是
A.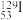 与 与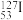 互为同位素 互为同位素 | B.碘单质及其化合物能使淀粉溶液变蓝 |
C.从海带中提取 的过程只发生物理变化 的过程只发生物理变化 | D.氯和碘是同族元素,HI比 稳定 稳定 |
您最近一年使用:0次
名校
3 . 实验室里进行碘的提取,①向盛有KI(aq)的试管中加入少许CCl4后滴加氯水,振荡、静置后,CCl4层变成紫色。②分离出CCl4层,③继续向其中滴加新制氯水,充分振荡,CCl4层会逐渐变浅,最后变成无色。上层水溶液也呈无色。
(1)写出CCl4层由无色变成紫色的化学方程式:_______ 。
(2)分离出CCl4层使用的实验仪器匙:_______ 。
(3)取最终上层水溶液,滴加淀粉溶液,溶液不变蓝,说明:________ 。再经实验测定,最终碘元素以HIO3形式存在,请写出③反应的化学方程式并配平:_______ 。若使用新制氯水和淀粉溶液,请写出检验溶液中含有I-的实验过程:_______ 。
(4)向用硫酸酸化的NaI溶液中中逐滴加入NaBrO3溶液,当加入2.6molNaBrO3时,测得反应后溶液中溴元素和碘元素的存在形式及物质的量如表。
请根据氧化还原反应中化合价升高和降低的总数相等的原则,通过计算判断反应后的溶液中是否存在IO ?
?_______ 。若存在,则IO 的物质的最是多少
的物质的最是多少_______ ?写出计算过程。
(1)写出CCl4层由无色变成紫色的化学方程式:
(2)分离出CCl4层使用的实验仪器匙:
(3)取最终上层水溶液,滴加淀粉溶液,溶液不变蓝,说明:
(4)向用硫酸酸化的NaI溶液中中逐滴加入NaBrO3溶液,当加入2.6molNaBrO3时,测得反应后溶液中溴元素和碘元素的存在形式及物质的量如表。
| 粒子 | I2 | Br2 | IO |
| n/mol | 0.5 | 1.3 | 未知 |
 ?
? 的物质的最是多少
的物质的最是多少
您最近一年使用:0次
解题方法
4 . 下列化学实验装置、操作使用合理的是
 |  | 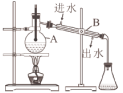 | 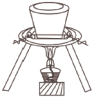 |
| A.用标准氢氧化钠溶液滴定稀硫酸溶液 | B.用氯仿作萃取剂分离溴水 | C.用蒸馏的方法分离乙酸和乙醇 | D.海水制碘实验,海带成灰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 2022年6月8日是世界海洋日,主题为“保护海洋生态系统,人与自然和谐共生”。下列有关说法错误的是
| A.海水晒盐属于物理变化 |
B.海水中的 可用四氯化碳直接萃取得到 可用四氯化碳直接萃取得到 |
C.海带中富含 ,从海带中获得碘单质一定涉及氧化还原反应 ,从海带中获得碘单质一定涉及氧化还原反应 |
D.海水中富含 ,可以通过沉淀法将海水中的镁离子分离出来 ,可以通过沉淀法将海水中的镁离子分离出来 |
您最近一年使用:0次
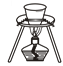
6 . 下列关于自然资源开发利用的说法中错误的是

| A.工业生产镁的过程为:海水→氢氧化镁→氧化镁→金属镁 |
| B.煤的干馏、煤的气化与石油的催化重整均属于化学变化 |
| C.从海带中提取碘时,利用图所示装置灼烧海带碎片 |
| D.利用可再生资源作反应物符合绿色化学的要求 |
您最近一年使用:0次
名校
解题方法
7 . 海水是一个巨大的化学资源宝库。请回答下列问题:
Ⅰ.从海带中提取碘单质
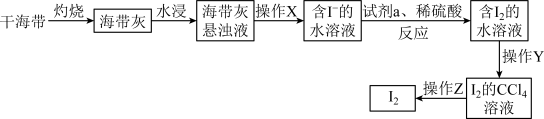
(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、_____ ,“操作X”的名称为_____ 。
(2)若试剂 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为_____ ,氧化性:
_____ (填“>”或“<”) 。
。
(3)“操作Y”为萃取分液,萃取后分液时,转移 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是_____ 。
Ⅱ.海水提溴:海水→海水淡化→ 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴
(4)“空气吹出”体现了溴的_____ 性,该步骤的目的是_____ 。
(5)若“吸收”步骤使用浓的 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为_____ 。若反应后得到 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,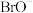 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比_____ 。
Ⅰ.从海带中提取碘单质

(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、
(2)若试剂
 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为
 。
。(3)“操作Y”为萃取分液,萃取后分液时,转移
 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是Ⅱ.海水提溴:海水→海水淡化→
 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴(4)“空气吹出”体现了溴的
(5)若“吸收”步骤使用浓的
 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,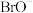 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
您最近一年使用:0次
8 . 从海带中提取碘的简单流程如下:
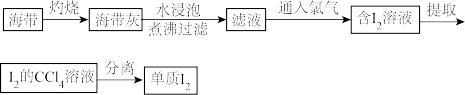
(1)灼烧时应在什么仪器中进行:________ 。
(2)滤液中通入氯气得到含I2溶液,写出反应的离子方程式________ ;氯气通常可用________ 试剂替代。
(3)如何检验通入氯气后所得溶液中含有I2:________ 。

(1)灼烧时应在什么仪器中进行:
(2)滤液中通入氯气得到含I2溶液,写出反应的离子方程式
(3)如何检验通入氯气后所得溶液中含有I2:
您最近一年使用:0次
名校
解题方法
9 . 碘是国防、工业、农业、医药等部门和行业所依赖的重要原料。下图是某厂家设计的海带提碘流程图:
(1)步骤①是将海带进行灼烧,应该选择的仪器为______ (填字母),其名称为______ 。_______ 。
(3)步骤③发生反应的离子方程式为______ 。
(4)设计步骤④⑤⑥的目的是_______ 。
(5)步骤③中实际消耗的 比理论多,其原因是
比理论多,其原因是______ (用化学方程式表示)。
(6)步骤⑥滴入少量浓硫酸后发生反应的离子方程式为 ,每生成
,每生成 ,时转移的电子数目为
,时转移的电子数目为______ ;与直接滴加稀硫酸相比,这里用浓硫酸的好处是_______ (填一条)。
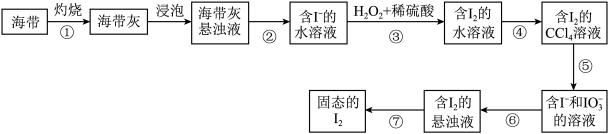
(1)步骤①是将海带进行灼烧,应该选择的仪器为
(3)步骤③发生反应的离子方程式为
(4)设计步骤④⑤⑥的目的是
(5)步骤③中实际消耗的
 比理论多,其原因是
比理论多,其原因是(6)步骤⑥滴入少量浓硫酸后发生反应的离子方程式为
 ,每生成
,每生成 ,时转移的电子数目为
,时转移的电子数目为
您最近一年使用:0次
2024-07-06更新
|
44次组卷
|
2卷引用:湖南省部分学校2023-2024学年高一下学期7月期末联考化学试题
名校
10 . I.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得镁、溴等重要的化工产品。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和___________ 。离子交换法净化水的过程如图所示。下列说法正确的是___________ (填序号)。
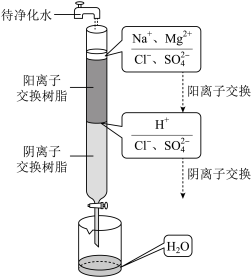
A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
(2)工业上通过 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是___________ 。制备溴时通入热空气可以吹出溴,是利用了溴的___________ 。
Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
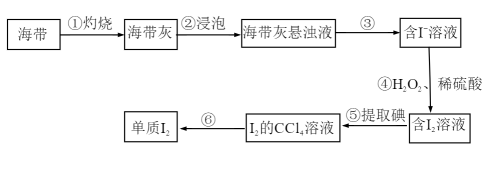
(3)实验步骤①不会用到下列仪器中的___________ (填字母)
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是___________
(5)步骤④中反应的离子方程式为___________
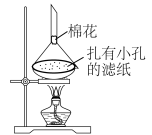
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理________ ;棉花的作用是________ 。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和

A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有
 被除去
被除去C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:

(2)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(3)实验步骤①不会用到下列仪器中的
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理

您最近一年使用:0次



