解题方法
1 . 碘是生物必需的一种微量元素,海带、海藻等食物含碘量最为丰富.某小组通过实验提取并测定干海带中碘的含量.回答下列问题:
Ⅰ.从海带中提取碘.该小组同学按如图实验流程进行实验:______ (填仪器名称)。______ (用离子方程式表示)。
Ⅱ.滴定法测海带中碘的含量。
用 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: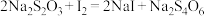 ,
,
(3)用酸式滴定管量取 的水溶液时常需要排出气泡,操作是
的水溶液时常需要排出气泡,操作是__________ 。
(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。
猜想1:碘离子被______ 氧化;
猜想2:碘离子被步骤iii中过量的 氧化;
氧化;
②验证猜想
③查阅资料 小组同学认为可能是反应速率不同造成的, 氧化
氧化 的速率
的速率______ (填“快于”或“慢于”) 还原
还原 的速率,导致待测液反复变为蓝色。
的速率,导致待测液反复变为蓝色。
④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案____________ 。
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL
 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为______ mg/g(保留2位有效数字)。
Ⅰ.从海带中提取碘.该小组同学按如图实验流程进行实验:

Ⅱ.滴定法测海带中碘的含量。
用
 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: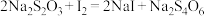 ,
,(3)用酸式滴定管量取
 的水溶液时常需要排出气泡,操作是
的水溶液时常需要排出气泡,操作是(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。

猜想1:碘离子被
猜想2:碘离子被步骤iii中过量的
 氧化;
氧化;②验证猜想
| 序号 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量原海带浸出液,加入硫酸酸化,再滴加几滴淀粉溶液,鼓入空气 | 待测液始终保持无色 | 猜想1不成立 |
| 2 | 将2mL KI溶液、2滴 KI溶液、2滴  溶液、2滴淀粉溶液和1滴 溶液、2滴淀粉溶液和1滴  溶液混合配制待测液,用 溶液混合配制待测液,用 溶液滴定 溶液滴定 | 猜想2不成立 |
 氧化
氧化 的速率
的速率 还原
还原 的速率,导致待测液反复变为蓝色。
的速率,导致待测液反复变为蓝色。④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL

 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为
您最近一年使用:0次
2024-04-16更新
|
633次组卷
|
2卷引用:广东省佛山市2024届高三教学质量检测(一)化学试题
2 . 化学与生活、生产、能源及环境等密切相关。下列说法正确的是
| A.向浸泡过海带灰的水中滴入淀粉溶液有蓝色出现 |
| B.“天宫二号”空间实验室的硅电池板将光能直接转换为电能 |
| C.由植物及其废弃物制成的燃料乙醇属于不可再生能源 |
| D.用Na2S作还原剂可除去污水中的Cu2+和Hg2+ |
您最近一年使用:0次
名校
解题方法
3 . 下列劳动项目与所述的化学知识不相符的是
| 选项 | 劳动项目 | 化学知识 |
| A | 传统工艺:手工制作陶瓷 | CaCO3是陶瓷主要成分 |
| B | 学农活动:使用复合肥料培育植物 | 复合肥含N、P、K三种元素中的两种或三种 |
| C | 自主探究:海带提碘 | 通过灼烧将有机碘转化为碘离子 |
| D | 家务劳动:烹煮鱼时加入少量料酒和食醋可以去腥提鲜 | 食醋与料酒发生酯化反应,增加香味 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-08-24更新
|
661次组卷
|
3卷引用:广东省深圳市光明区高级中学2022届高三模拟测试(一)化学试题
4 . 下列原理或方法不能达到相应目的或现象的是
| 选项 | 目的或现象 | 原理或方法 |
| A | 去除汽车尾气中NO和CO | 催化转化: |
| B | 利用海带提取碘 | 经灼烧、溶解、过滤、氧化和萃取富集碘元素 |
| C | 维持血液的pH为7.35~7.45 | 血浆中 和 和 的浓度保持动态平衡 的浓度保持动态平衡 |
| D | 消除蚂蚁叮咬引起的皮肤不适 | 可涂抹饱和 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 海洋资源的利用具有非常广阔的前景。
I.从海水中提取溴的过程如下:

(1)步骤“氧化”中已获得Br2.步骤“吸收”中又将Br2反应为Br-,其目的为_______ 。
(2)热空气吹出Br2,利用了溴的_______。
(3)步骤“吸收”用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的化学方程式为_______ 。
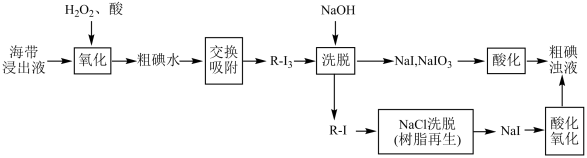
II.离子交换法从海带中提取碘是一种较为先进的制碘工艺。下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。
已知:①I2+I- I
I
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I )有很强的交换吸附能力。
)有很强的交换吸附能力。
③步骤“交换吸附”发生的反应:R-Cl+I =R-I3+Cl-。
=R-I3+Cl-。
试回答下列问题:
(4)下列各步反应中,属于氧化还原反应的有:_______(填序号)
(5)酸性条件下,原料被H2O2氧化时发生的反应有:
①_______ ;
②I2+I- I
I 。
。
依据整个生产流程分析是否可以加过量H2O2;_______ (填“是”或“否”)。并说明理由:_______ 。
(6)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于_______ 。
I.从海水中提取溴的过程如下:

(1)步骤“氧化”中已获得Br2.步骤“吸收”中又将Br2反应为Br-,其目的为
(2)热空气吹出Br2,利用了溴的_______。
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(3)步骤“吸收”用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的化学方程式为
II.离子交换法从海带中提取碘是一种较为先进的制碘工艺。下图是使用离子交换树脂的“离子交换法”从海带中提取碘的主要流程。

已知:①I2+I-
 I
I
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I
 )有很强的交换吸附能力。
)有很强的交换吸附能力。③步骤“交换吸附”发生的反应:R-Cl+I
 =R-I3+Cl-。
=R-I3+Cl-。试回答下列问题:
(4)下列各步反应中,属于氧化还原反应的有:_______(填序号)
| A.交换吸附 | B.洗脱 | C.酸化 | D.NaCl洗脱 |
(5)酸性条件下,原料被H2O2氧化时发生的反应有:
①
②I2+I-
 I
I 。
。依据整个生产流程分析是否可以加过量H2O2;
(6)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的氧化剂。若某企业在酸性条件下选择NaNO2为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,则添加氧化剂与NaI的质量比应不少于
您最近一年使用:0次
2022-04-24更新
|
1132次组卷
|
4卷引用:福建省厦门第一中学2021-2022学年高一下学期期中考试化学试题
福建省厦门第一中学2021-2022学年高一下学期期中考试化学试题(已下线)8.1.1 金属矿物和海水资源的开发利用-2021-2022学年高一化学课后培优练(人教版2019必修第二册)广东省广州市第六中学2021-2022学年高一下学期综合考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期开学验收考试化学试题
名校
6 . 海水化学资源开发利用中的提碘、提溴的部分过程如图所示。下列说法正确的是
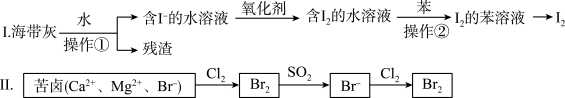
| A.I中操作①用到的玻璃仪器只有烧杯、玻璃棒、胶头滴管 |
| B.I中操作②的苯可用酒精代替 |
C.Ⅱ中SO2与Br2反应的化学方程式为: |
D.Ⅱ中还原性: |
您最近一年使用:0次
2023-04-08更新
|
618次组卷
|
3卷引用:山东省威海市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
7 . 海带灰富含以I-形式存在的碘元素。在实验室中,从海带灰浸取液中提取碘单质的流程如图:
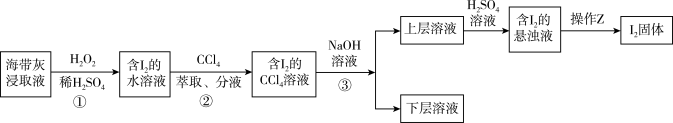
下列说法正确的是

下列说法正确的是
| A.为提高①中反应的速率,可增大硫酸浓度或在高温条件下进行 |
| B.操作②中CCl4,可用酒精、苯等代替 |
| C.操作③使用的是反萃取法,得到的上层溶液为紫红色 |
| D.操作Z所需的玻璃仪器有烧杯、玻璃棒、漏斗 |
您最近一年使用:0次
2022-07-07更新
|
544次组卷
|
4卷引用:山东省济南市2021-2022学年高一下学期期末考试化学试题
名校
解题方法
8 . 某同学检验海带中是否含有碘元素,进行了如下实验。
步骤Ⅰ:灼烧干海带得到海带灰;
步骤Ⅱ:将海带灰加蒸馏水溶解、过滤,得到海带灰浸取液;
步骤Ⅲ:取少量浸取液于试管中,加入淀粉溶液,溶液未变蓝;再加入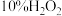 溶液(硫酸酸化),溶液变为蓝色;
溶液(硫酸酸化),溶液变为蓝色;
步骤Ⅳ:将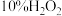 溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
步骤Ⅴ:向步骤Ⅳ所得溶液中通入 ,溶液迅速变为蓝色。
,溶液迅速变为蓝色。
下列说法不正确的是
步骤Ⅰ:灼烧干海带得到海带灰;
步骤Ⅱ:将海带灰加蒸馏水溶解、过滤,得到海带灰浸取液;
步骤Ⅲ:取少量浸取液于试管中,加入淀粉溶液,溶液未变蓝;再加入
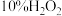 溶液(硫酸酸化),溶液变为蓝色;
溶液(硫酸酸化),溶液变为蓝色;步骤Ⅳ:将
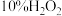 溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;
溶液(硫酸酸化)替换为氯水,重复步骤Ⅲ,溶液未变蓝;步骤Ⅴ:向步骤Ⅳ所得溶液中通入
 ,溶液迅速变为蓝色。
,溶液迅速变为蓝色。下列说法不正确的是
| A.步骤Ⅰ中,灼烧干海带的目的是除去有机化合物,获得可溶性碘化物 |
B.步骤Ⅲ中,反应的离子方程式: |
C.若将步骤Ⅴ中的 替换为 替换为 溶液,也可能观察到溶液变为蓝色 溶液,也可能观察到溶液变为蓝色 |
D.对比步骤Ⅲ、Ⅳ和Ⅴ中实验现象,说明该条件下 氧化性比氯水强 氧化性比氯水强 |
您最近一年使用:0次
2023-04-29更新
|
553次组卷
|
4卷引用:北京市丰台区2023届高三下学期二模考试化学试题
名校
解题方法
9 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
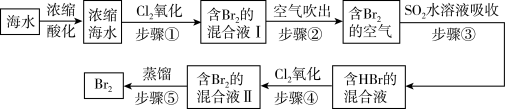
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有___ 个电子转移(用a和NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:____ 、____ 。
(5)“试剂a”通常应具有一定的____ 性。
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:____ 。
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是____ 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收amolBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤:
(5)“试剂a”通常应具有一定的
利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
______KI+______H2O=______KOH+______I2
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是
A. | B.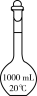 | C.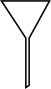 | D. |
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
 =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液30.0mL,恰好反应完全。
则所测盐中碘的含量是
您最近一年使用:0次
名校
解题方法
10 . 溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。从海带中提取碘单质,工艺流程如图。
(1)步骤①操作时,除需要酒精灯、三脚架、泥三角外,还需用到的主要仪器是_____ (填名称)。
(2)海带中碘元素的存在形式为_____ (用化学符号表示)。
(3)步骤⑤的具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层。
①实验步骤的正确顺序为_____→_____→_____→A→H→_____→_____→_____。_____ 。
②静止、分层后,下层溶液的颜色为_____ 。
(4)步骤④中的H2O2可用以下_____ (填字母)试剂代替。
a.Cl2 b.Na2SO3 c.NaCl
(5)步骤⑤中,某学生选择用CCl4来萃取碘的理由_____ 。
(6)步骤⑥使用的是反萃取法,目的是富集碘元素,该步反应的离子方程式为_____ 。每消耗1molI2转移电子数为_____ 。
(7)某同学制得的粗碘中含有少量Na2SO4,对粗碘进行提纯的装置如图所示,采用的分离方法是_____ ;为得到较多较高纯度的单质碘,A容器中可盛放的试剂为_____ (填字母)。
a.冷水 b.热水 c.热氢氧化钠溶液
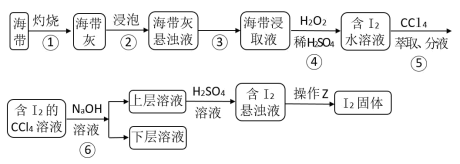
(1)步骤①操作时,除需要酒精灯、三脚架、泥三角外,还需用到的主要仪器是
(2)海带中碘元素的存在形式为
(3)步骤⑤的具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层。
①实验步骤的正确顺序为_____→_____→_____→A→H→_____→_____→_____。
②静止、分层后,下层溶液的颜色为
(4)步骤④中的H2O2可用以下
a.Cl2 b.Na2SO3 c.NaCl
(5)步骤⑤中,某学生选择用CCl4来萃取碘的理由
(6)步骤⑥使用的是反萃取法,目的是富集碘元素,该步反应的离子方程式为
(7)某同学制得的粗碘中含有少量Na2SO4,对粗碘进行提纯的装置如图所示,采用的分离方法是
a.冷水 b.热水 c.热氢氧化钠溶液
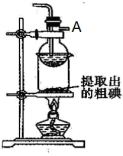
您最近一年使用:0次
2023-03-17更新
|
481次组卷
|
2卷引用:山东省德州市第一中学2022-2023学年高一3月月考化学试题



