名校
解题方法
1 . 海洋是一座巨大的化学资源宝库,如图是从海水中或海产品中提取若干种化学物质的流程图。
I.试剂级NaCl可用海盐(含泥沙、海藻、Ca2+、Mg2+、Fe3+、SO 等杂质)为原料制备。
等杂质)为原料制备。

(1)焙炒海盐的目的是______ 。
(2)根据除杂原理,填写合适的试剂③,并选择每步 预期沉淀的离子。
离子:a.Ca2+ b.Mg2+ c.Fe3+ d.SO
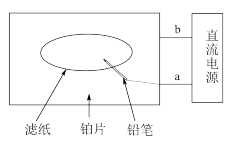
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是______ 。
II.国家海洋局科研学者考察了从浓海水中提溴的一种新型方法:聚四氟乙烯(PTFE)气态膜法提溴。本方法关键是采用了PTFE中空纤维膜,在该膜中,水不可以通过,而溴分子可以自主进入和脱离。
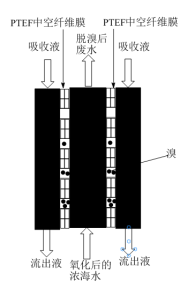
将氧化后的浓海水加入气态膜设备预处理,用NaOH溶液作为吸收液配合处理。处理过程的俯视截面示意图如图所示。经流出液氧化后的流出液检验,流出液中含BrO 离子。
离子。
(4)浓海水中溴元素的存在形式是______ ,氧化浓海水时可选用的氧化剂是______ 。
(5)流出液中另外一种含溴物质是______ 。
(6)说明聚四氟乙烯(PTFE)气态膜是如何在上述过程中起到富集作用______ 。
III.小淳同学按如图实验过程,证明海带中存在碘元素。
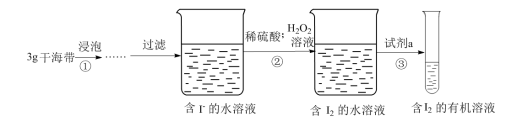
(7)H2O2的作用是______ 。
(8)试剂a不能选择的是(填序号)______ 。
(9)操作③的名称是______ 。
(10)操作③中需要振荡排放气体,放气时分液漏斗的状态是______ 。
小桢同学欲探究I-的性质,进行如图实验:
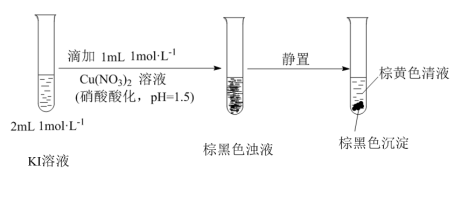
(11)该小组同学推测反应生成了I2。设计实施了如下方案,证实了推测。请将方案补充完整:取棕色清液,______ 。
进一步探究发现:棕黑色沉淀中含有CuI。
(12)由此推知:Cu(NO3)2与KI反应过程中,一定发生的反应的离子方程式为______ 。
I.试剂级NaCl可用海盐(含泥沙、海藻、Ca2+、Mg2+、Fe3+、SO
 等杂质)为原料制备。
等杂质)为原料制备。
(1)焙炒海盐的目的是
(2)根据除杂原理,填写合适的试剂③,并
离子:a.Ca2+ b.Mg2+ c.Fe3+ d.SO

| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 | 适量NaOH溶液 | ① |
| 步骤2 | 适量BaCl2溶液 | ② |
| 步骤3 | 适量③ | ④ |
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是

| A.b极发生还原反应 | B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 | D.a处是负极 |
II.国家海洋局科研学者考察了从浓海水中提溴的一种新型方法:聚四氟乙烯(PTFE)气态膜法提溴。本方法关键是采用了PTFE中空纤维膜,在该膜中,水不可以通过,而溴分子可以自主进入和脱离。
将氧化后的浓海水加入气态膜设备预处理,用NaOH溶液作为吸收液配合处理。处理过程的俯视截面示意图如图所示。经流出液氧化后的流出液检验,流出液中含BrO
 离子。
离子。
(4)浓海水中溴元素的存在形式是
(5)流出液中另外一种含溴物质是
(6)说明聚四氟乙烯(PTFE)气态膜是如何在上述过程中起到富集作用
III.小淳同学按如图实验过程,证明海带中存在碘元素。

(7)H2O2的作用是
(8)试剂a不能选择的是(填序号)
| A.CCl4 | B.苯 | C.酒精 | D.直馏汽油 |
(9)操作③的名称是
(10)操作③中需要振荡排放气体,放气时分液漏斗的状态是
A.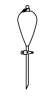 | B.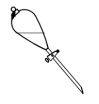 | C.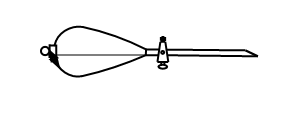 | D. |
小桢同学欲探究I-的性质,进行如图实验:

(11)该小组同学推测反应生成了I2。设计实施了如下方案,证实了推测。请将方案补充完整:取棕色清液,
进一步探究发现:棕黑色沉淀中含有CuI。
(12)由此推知:Cu(NO3)2与KI反应过程中,一定发生的反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 海带提碘过程为海带灼烧为海带灰、用水浸取、过滤,所得浸取液中加氧化剂氧化、萃取分液、加NaOH浓溶液反萃取、酸化后过滤得碘单质。上述过程中,用到的玻璃仪器有
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
| A.②③④⑦ | B.①②④⑥⑦ | C.②④⑥⑦ | D.①②③④⑥⑦ |
您最近一年使用:0次
2023-09-23更新
|
199次组卷
|
6卷引用:河北省部分学校2023-2024学年高三一轮复习联考(一)化学试题
3 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。工业上从含碘海水中制备 的一种方法如图所示。已知氧化性
的一种方法如图所示。已知氧化性 ,还原性
,还原性 。回答下列问题:
。回答下列问题:
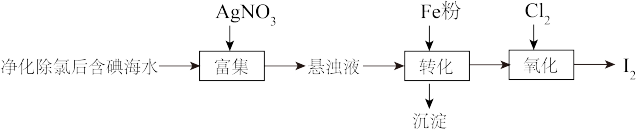
(1)海带中含有丰富的碘元素,处理时应将海带放入_______ (填仪器名称)中进行灼烧得含 的灰烬。
的灰烬。
(2)转化过程加入的Fe粉是过量的,发生的反应为: 。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为
。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为_______ ;若要检验转化过程所加Fe粉是否过量,可取适量转化所得的溶液于试管中,加入_______ 溶液,观察现象。
(3)氧化过程可以用适量的酸化的 代替
代替 ,则该反应的离子方程式为
,则该反应的离子方程式为_______ 。用 做氧化剂时也需控制
做氧化剂时也需控制 的用量,若反应物
的用量,若反应物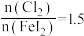 时,氧化产物为
时,氧化产物为 和
和_______ ,当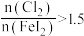 ,
, 会被过量的
会被过量的 进一步氧化从而导致单质碘的收率会降低。
进一步氧化从而导致单质碘的收率会降低。
(4)实验室从含碘废液(除 外,还含有
外,还含有 、
、 、
、 等)中回收碘,其实验过程如图所示:
等)中回收碘,其实验过程如图所示:
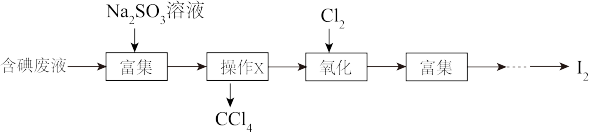
①操作X的名称为_______ 。
②向含碘废液中加入稍过量的 溶液,将废液中的
溶液,将废液中的 还原为
还原为 ,该操作的目的是
,该操作的目的是_______ 。
③氧化时,在三颈烧瓶中将含 的水溶液用盐酸调至pH约为2,缓慢通入
的水溶液用盐酸调至pH约为2,缓慢通入 ,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是
,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是_______ 。(选填字母编号)
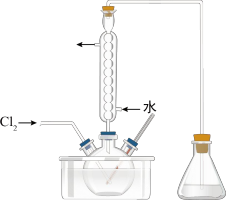
A.增大 的溶解度 B.防止
的溶解度 B.防止 的升华 C.防止水发生分解
的升华 C.防止水发生分解
 的一种方法如图所示。已知氧化性
的一种方法如图所示。已知氧化性 ,还原性
,还原性 。回答下列问题:
。回答下列问题:
(1)海带中含有丰富的碘元素,处理时应将海带放入
 的灰烬。
的灰烬。(2)转化过程加入的Fe粉是过量的,发生的反应为:
 。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为
。若往转化所得的沉淀中加入稀硫酸,反应的离子方程式为(3)氧化过程可以用适量的酸化的
 代替
代替 ,则该反应的离子方程式为
,则该反应的离子方程式为 做氧化剂时也需控制
做氧化剂时也需控制 的用量,若反应物
的用量,若反应物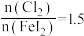 时,氧化产物为
时,氧化产物为 和
和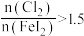 ,
, 会被过量的
会被过量的 进一步氧化从而导致单质碘的收率会降低。
进一步氧化从而导致单质碘的收率会降低。(4)实验室从含碘废液(除
 外,还含有
外,还含有 、
、 、
、 等)中回收碘,其实验过程如图所示:
等)中回收碘,其实验过程如图所示:
①操作X的名称为
②向含碘废液中加入稍过量的
 溶液,将废液中的
溶液,将废液中的 还原为
还原为 ,该操作的目的是
,该操作的目的是③氧化时,在三颈烧瓶中将含
 的水溶液用盐酸调至pH约为2,缓慢通入
的水溶液用盐酸调至pH约为2,缓慢通入 ,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是
,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因可能是
A.增大
 的溶解度 B.防止
的溶解度 B.防止 的升华 C.防止水发生分解
的升华 C.防止水发生分解
您最近一年使用:0次
解题方法
4 . 实验室里从海带中提取碘的流程如下:
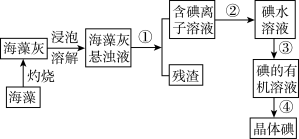
(1)提取碘的过程中有关实验的操作名称①_______ 、②_______ 、③_______ 、④_______ 。
(2)进行步骤①操作时,需要用到的玻璃仪器有:烧杯、漏斗和_______ 。进行步骤③操作时,需要用到的主要仪器是_______ 。
(3)写出上述过程中含I-的溶液通氯气后的离子方程式:_______ ,该反应中的氧化剂是_______ 。
(4)某同学想证明以上流程中的未知无色溶液中含有I-,现有以下试剂可供选择:
①新制氯水、②稀硝酸、③CCl4、④AgNO3溶液、⑤淀粉溶液。(完成以下填空)

(1)提取碘的过程中有关实验的操作名称①
(2)进行步骤①操作时,需要用到的玻璃仪器有:烧杯、漏斗和
(3)写出上述过程中含I-的溶液通氯气后的离子方程式:
(4)某同学想证明以上流程中的未知无色溶液中含有I-,现有以下试剂可供选择:
①新制氯水、②稀硝酸、③CCl4、④AgNO3溶液、⑤淀粉溶液。(完成以下填空)
| 方案 | 选用试剂(填标号) | 主要现象 |
| 1 | 未知溶液、 | |
| 2 | 未知溶液、 |
您最近一年使用:0次
名校
5 . 下列叙述不正确的是
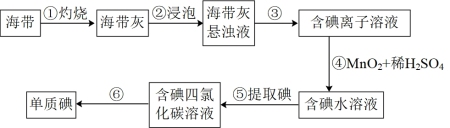

| A.步骤③的分离操作为过滤 |
| B.步骤④中理论上每产生1molI2,需要1molMnO2被氧化 |
| C.步骤⑥操作可以为先加入浓碱过滤,向水层再加入45%硫酸溶液分液,将碘提取出来 |
| D.步骤⑤中加入萃取剂后现象是溶液分层,下层为四氯化碳层呈紫色 |
您最近一年使用:0次
2022-05-15更新
|
195次组卷
|
3卷引用:北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题
北京市昌平区第一中学2021-2022学年高一下学期线上期中学情调研化学试题(已下线)第13练 自然资源的开发利用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)北京市昌平区第一中学2022-2023学年高一上学期期中考试化学试题
解题方法
6 . 海洋是巨大的资源宝库,孕育着丰富的矿产。海水资源的综合利用对人类的生产生活有重要意义。回答下列问题:
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器________ (填“蒸发皿”“坩埚”或“烧杯”)内进行。
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有_________ (填一种即可);
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
(4)欲证明水溶液中含有I2,实验方法为________________ 。
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为___________ 。
(6)步骤②说明溴单质具有_________ 性,步骤③④的目的是______________ 。
(7)步骤③的还原剂若为 溶液,则其离子方程式为
溶液,则其离子方程式为____________ 。
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
| A.稀硝酸 | B.酸性 | C.浓硫酸 | D.稀硫酸、 |
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为
(6)步骤②说明溴单质具有
(7)步骤③的还原剂若为
 溶液,则其离子方程式为
溶液,则其离子方程式为
您最近一年使用:0次
7 . 碘和碘化合物的用途广泛,实验室从海带中提取碘的步骤为:①海带灼烧,②溶解过滤,③在滤液中加入稀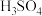 和
和 氧化,④用
氧化,④用 萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
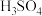 和
和 氧化,④用
氧化,④用 萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是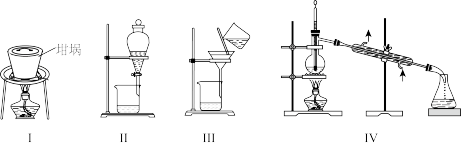
| A.用Ⅰ装置灼烧海带 | B.用Ⅱ装置萃取 | C.用Ⅲ装置过滤 | D.用Ⅳ装置蒸馏 |
您最近一年使用:0次
2022-04-09更新
|
372次组卷
|
3卷引用:重庆市2022届高三第二次诊断性考试康德卷化学试题
8 . 我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
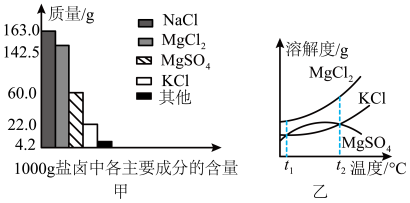
(1)根据图甲所示,写出盐卤中含量最多的盐为__________ 。(填化学式)
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 以上,根据溶解度曲线,首先析出的晶体应是
以上,根据溶解度曲线,首先析出的晶体应是__________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
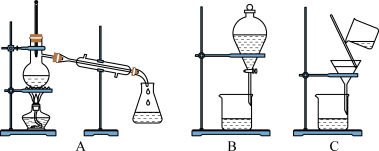
粗盐的提纯应选择图__________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是__________ 。
A.NaOH、 、
、 、HCl B.NaOH、
、HCl B.NaOH、 、
、 、HCl
、HCl
C. 、
、 、NaOH、HCl D.
、NaOH、HCl D. 、NaOH、
、NaOH、 、HCl
、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的__________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中 的存在,
的存在,______________________________ 。
(6)“提取碘”存在以下两种方案。
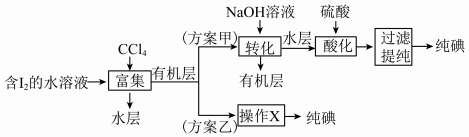
①方案乙中“操作X”的名称是__________ 。
②该流程可循环利用的物质是__________ 。
③采用方案乙得到纯碘的产率较低,原因是______________________________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 以上,根据溶解度曲线,首先析出的晶体应是
以上,根据溶解度曲线,首先析出的晶体应是(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、
 、
、 、HCl B.NaOH、
、HCl B.NaOH、 、
、 、HCl
、HClC.
 、
、 、NaOH、HCl D.
、NaOH、HCl D. 、NaOH、
、NaOH、 、HCl
、HClⅡ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中
 的存在,
的存在,(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次
2023-12-27更新
|
160次组卷
|
2卷引用:河北省保定市1+3联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
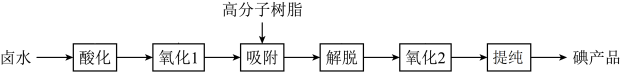
9 . 工业上以卤水(富含 )为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
)为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
 )为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
)为原料用高分子树脂提取碘的工艺流程如图。下列说法不正确的是
| A.“氧化1”过程既可以用氯气,也可以用过氧化氢溶液 |
B.“解脱”可以用亚硫酸钠将碘单质还原为 ,离子方程式为 ,离子方程式为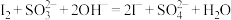 |
| C.用高分子树脂“吸附”,再“解脱”是为了便于分离富集碘元素 |
| D.“提纯”过程包括萃取分液、蒸馏得到粗产品,再利用升华法纯化 |
您最近一年使用:0次
2022-09-03更新
|
183次组卷
|
2卷引用:安徽省江淮十校2022-2023学年高三上学期第一次联考化学试题
解题方法
10 . 化学与生活、生产密切相关,下列说法错误的是
| A.使用医用酒精、紫外线杀菌消毒的过程中均涉及蛋白质变性 |
| B.工业上可采用离子交换法提高海带中碘的提取率 |
| C.使用常温下与浓硫酸不反应的铁质容器贮运浓硫酸 |
| D.晨雾中的光束如梦似幻,是丁达尔效应带来的美景 |
您最近一年使用:0次



