1 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。
(1)工业上海水淡化的方法有___________ 、___________ 。(填两种)
(2)空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如下:
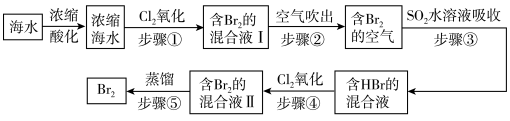
①步骤①中获得 的离子方程式为
的离子方程式为___________ 。
②根据上述反应可判断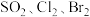 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
③步骤③中若吸收剂为饱和 溶液(足量),则完全吸收
溶液(足量),则完全吸收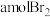 共有
共有___________ 个电子转移(用a和 的代数式表示)。
的代数式表示)。
(3)某化学兴趣小组按如下实验流程提取海带中的碘,请回答相关问题。
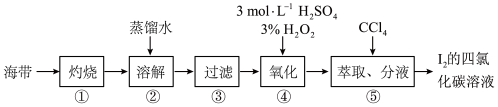
i.第①步是将海带放入_______ (填仪器名称)中,用酒精灯充分加热灰化。
ii.实验第④步骤后应检验碘单质的存在,具体方法是________ 。
iii.海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第_____ 步(填编号)与碘分离的。
iv.写出④中在酸性溶液下反应的离子方程式_______ 。
(1)工业上海水淡化的方法有
(2)空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如下:

①步骤①中获得
 的离子方程式为
的离子方程式为②根据上述反应可判断
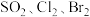 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是③步骤③中若吸收剂为饱和
 溶液(足量),则完全吸收
溶液(足量),则完全吸收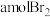 共有
共有 的代数式表示)。
的代数式表示)。(3)某化学兴趣小组按如下实验流程提取海带中的碘,请回答相关问题。

i.第①步是将海带放入
ii.实验第④步骤后应检验碘单质的存在,具体方法是
iii.海带灰中还含有其他无机盐类(硫酸盐、硝酸盐、碳酸盐等),这些盐类是在流程图中的第
iv.写出④中在酸性溶液下反应的离子方程式
您最近一年使用:0次
2 . 化学与人类社会的生产、生活有着密切联系。下列叙述中错误的是
| A.煤的干馏、海带提碘、石油裂解等都涉及化学变化 |
| B.油墨中含有的Fe3O4是一种磁性物质 |
| C.用纳米技术催化CO2合成可降解塑料聚碳酸酯,可实现“碳”的循环利用 |
| D.天然气、沼气等不可再生能源,完全燃烧的主要产物均为CO2和H2O |
您最近一年使用:0次
3 . 海洋植物海带中含有丰富的碘元素,某化学学习小组为了验证海带中含有碘,在实验室从海带中提取碘的流程如图:
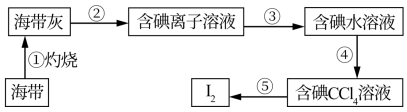
(1)第②步的操作名称是_____ ,用到的玻璃仪器有烧杯、玻璃棒和_____ ,检验溶液中含I-的方法是______ ,海带中碘元素主要以NaI或KI的形式存在,设计实验证明含碘离子溶液中K+的存在______ 。
(2)第③步:氧化。向含 的溶液中加入过量的H2O2和稀H2SO4。配平其离子反应方程式。
的溶液中加入过量的H2O2和稀H2SO4。配平其离子反应方程式。______
 I-+
I-+ H++
H++ H2O2=
H2O2= I2+
I2+ H2O
H2O
(3)第④步:萃取与分液。分液时若打开玻璃活塞后发现液体流不出,原因可能是_____ 。分液后上层液体中是否还有碘单质可以取少许溶液加入_____ 试剂来进行检验。
(4)第⑤步:通过蒸馏从碘的CCl4溶液中提取碘并回收CCl4。蒸馏操作前蒸馏烧瓶内需放几片碎瓷片的目的是______ ,温度计水银球的位置是_____ ,冷凝管水流方向是_____ 。

(1)第②步的操作名称是
(2)第③步:氧化。向含
 的溶液中加入过量的H2O2和稀H2SO4。配平其离子反应方程式。
的溶液中加入过量的H2O2和稀H2SO4。配平其离子反应方程式。 I-+
I-+ H++
H++ H2O2=
H2O2= I2+
I2+ H2O
H2O(3)第④步:萃取与分液。分液时若打开玻璃活塞后发现液体流不出,原因可能是
(4)第⑤步:通过蒸馏从碘的CCl4溶液中提取碘并回收CCl4。蒸馏操作前蒸馏烧瓶内需放几片碎瓷片的目的是
您最近一年使用:0次
2022-01-12更新
|
308次组卷
|
2卷引用:河北省唐山市2021-2022学年高一上学期期末考试化学试题
4 . 开发和利用海洋资源是当前科学研究的一项重要任务,如图是某化工厂对海洋资源综合利用的流程图:
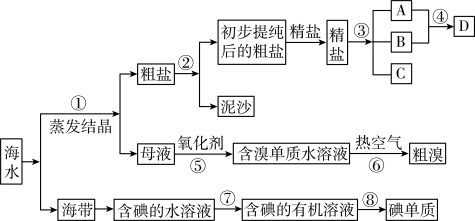
请根据以上信息回答下列问题:
(1)写出流程中⑦所用的方法:_______ 。
(2)初步提纯后的粗盐中含有Ca2+、Mg2+、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:

加入的试剂①、②分别是:_______ 、_______ 。
(3)步骤③的条件是通直流电,其离子方程式为_______ 。D具有杀菌消毒的作用,在喷洒前需要在空气中晾置一会,这样做的原因是_______ 。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克Cl2的氧化能力(氯元素均被还原至-1价)。则亚氯酸钠NaClO2的有效氯含量为_______ (保留两位小数)。
(5)若用来提取Br2,反应⑤所用的氧化剂的来源较合理的是_______ 。
A.从外地购买 B.在当地新建生产厂 C.从本厂生产烧碱处循环
(6)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有_______ 性。对粗溴一般做如下处理:
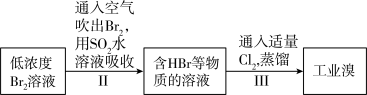
其中步骤Ⅱ、Ⅲ起到的作用是_______ 。
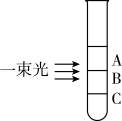
向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应。
(7)写出制备氯化银胶体的方程式:_______ 。
(8)具有明显的丁达尔效应的是区域_______ (填字母),该区域中分散质的粒径大小为_______ 。
(9)分离出C区域的分散质的方法是_______ 。

请根据以上信息回答下列问题:
(1)写出流程中⑦所用的方法:
(2)初步提纯后的粗盐中含有Ca2+、Mg2+、
 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
加入的试剂①、②分别是:
(3)步骤③的条件是通直流电,其离子方程式为
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力(即得电子数)相当于多少克Cl2的氧化能力(氯元素均被还原至-1价)。则亚氯酸钠NaClO2的有效氯含量为
(5)若用来提取Br2,反应⑤所用的氧化剂的来源较合理的是
A.从外地购买 B.在当地新建生产厂 C.从本厂生产烧碱处循环
(6)流程⑥将溴单质从水溶液中分离出来是基于溴单质具有

其中步骤Ⅱ、Ⅲ起到的作用是
向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应。

(7)写出制备氯化银胶体的方程式:
(8)具有明显的丁达尔效应的是区域
(9)分离出C区域的分散质的方法是
您最近一年使用:0次
解题方法
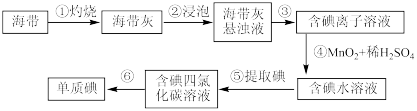
5 . 海带、紫菜等藻类植物中含有丰富的碘元素,下列叙述正确的是( )

| A.加碘食盐可以使淀粉溶液变蓝 |
| B.步骤④中发生的反应为2I-+MnO2+4H+=I2+Mn2++2H2O |
C.步骤④如果用碘酸钾氧化,理论上每产生 ,转移2mol电子 ,转移2mol电子 |
| D.步骤⑤中提取碘的方法是蒸馏 |
您最近一年使用:0次
名校
解题方法
6 . 海带中含有丰富的碘,某校化学兴趣小组的同学们设计联合氯碱工业,以海带灰为原料提碘的工艺流程如图:
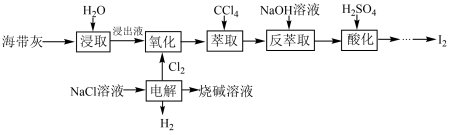
回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是_____ ;请你设计实验证明“浸取”已经进行完全:_____ (需要用到的实验药品有:淀粉溶液、硫酸酸化的H2O2溶液,写出具体实验操作和现象)。
(2)“电解”反应的化学方程式为_____ 。
(3)“萃取”时,CCl4层的颜色为______ 色;“反萃取”时生成NaI和NaIO3,写出该反应的离子方程式:______ 。
(4)“酸化”后生成含I2的悬浊液,需要经过_____ (填操作名称)操作得到I2。
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为______ %
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有_____ (填化学式)。

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是
(2)“电解”反应的化学方程式为
(3)“萃取”时,CCl4层的颜色为
(4)“酸化”后生成含I2的悬浊液,需要经过
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有
您最近一年使用:0次
名校
解题方法
7 . 海洋是巨大的资源宝库,可以制取多种物质。
I.海水提溴
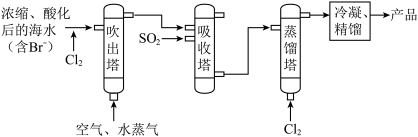
(1)吹出塔中采用气-液逆流的方式(液体从塔顶喷淋,气体从塔底进入),其目的是_______ 。
(2)请写出吸收塔中反应的离子方程式___________ 。
II.海带提碘(海带中碘元素以I-形式存在)
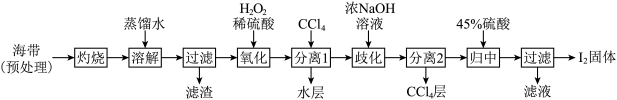
(3)“氧化”过程涉及到的离子方程式是_________ ,请设计一种检验所得溶液含I2的方法:___________ 。
(4)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为________ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为________ 。
(5)图1是制取碘单质的原电池装置,图2是利用碘研制的新型的锌-碘溴液流电池(图中贮液器可储存电解质溶液,增加电池容量)。
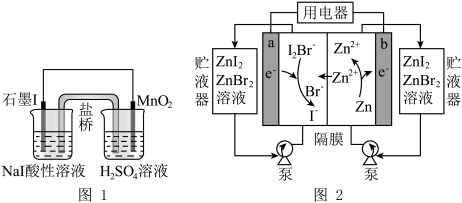
图1中,MnO2极发生的电极反应式为_______ ;图2中,放电时,a电极反应式为________ ,b电极质量减少6.5g时,a电极室增加________ mol离子(不考虑电极室与贮液器的溶液交换)。
I.海水提溴

(1)吹出塔中采用气-液逆流的方式(液体从塔顶喷淋,气体从塔底进入),其目的是
(2)请写出吸收塔中反应的离子方程式
II.海带提碘(海带中碘元素以I-形式存在)

(3)“氧化”过程涉及到的离子方程式是
(4)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为(5)图1是制取碘单质的原电池装置,图2是利用碘研制的新型的锌-碘溴液流电池(图中贮液器可储存电解质溶液,增加电池容量)。

图1中,MnO2极发生的电极反应式为
您最近一年使用:0次
解题方法
8 . 下列方程式与所给事实相符的是
A.工业上冶炼铝: |
B.用H2O2酸性溶液将海带灰中的I-转变为I2: |
C.FeO在空气中加热: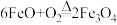 |
D.钢铁制品在潮湿空气中的电化学腐蚀: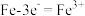 |
您最近一年使用:0次
名校
解题方法
9 . 碘( Godine)是人体必需的微量元素,是维持人体甲状腺正常功能所必需的元素, 人体缺碘时就会患甲状腺肿大,人们主要从饮水、粮食、蔬菜和周围环境中获取碘。多食海带,海鱼等含碘丰富的食品,对于防治甲状腺肿大很有效。某化学课外活动小组在实验室以海带为原料获得少量碘水,并以四氯化碳(沸点76.8℃)为溶剂将碘从碘水中提取出来,甲同学设计实验流程如图所示。请回答下列问题:
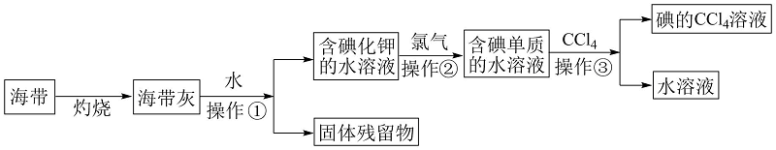
(1)上述流程中灼烧时必须用到最主要 的实验仪器有酒精灯、泥三角和___________ (填名称)。
(2)操作①的名称为___________ ;
(3)操作②中发生反应的离子方程式为______________________ ,乙同学对操作②进行了改进,用绿色氧化剂H2O2代替氯气并加适量稀盐酸,则所发生的离子反应方程式是____________________________________ 。
(4)操作③的实验名称为___________ ,最主要的 实验仪器的名称为___________ ;
(5)丙同学补充增加了一步操作:从碘的CCl4溶液中经过___________ 提取了碘单质并回收CCl4(填该操作名称)
(6)目前,我国推行全民食用的加碘盐是在食盐中加入___________ 这一物质(填写化学式)。

(1)上述流程中灼烧时
(2)操作①的名称为
(3)操作②中发生反应的离子方程式为
(4)操作③的实验名称为
(5)丙同学补充增加了一步操作:从碘的CCl4溶液中经过
(6)目前,我国推行全民食用的加碘盐是在食盐中加入
您最近一年使用:0次
10 . 从海带中提取碘单质,工艺流程如图:

下列说法正确的是

下列说法正确的是
A.含 的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 |
B.碘水中加入 得到碘的 得到碘的 溶液,该操作为萃取,萃取剂也可以用酒精 溶液,该操作为萃取,萃取剂也可以用酒精 |
| C.最后一步蒸馏操作中,冷凝管中的冷凝水应从上口进,下口出 |
| D.在最后得到的溶液中加入几滴淀粉溶液,溶液变蓝色 |
您最近一年使用:0次



