名校
解题方法
1 . I.某小组在实验室模拟工业提溴的流程(见下图),设计下图的装置进行实验。

回答下列问题:
(1)实验中先向A中通入Cl2,反应的离子方程式是_______ 。再向A中鼓入热空气,观察到的现象是_______ 。
(2)A中产生的气体被B中的 水溶液吸收,反应的化学方程式为
水溶液吸收,反应的化学方程式为_______ 。从氧化还原角度分析, 在该反应中体现了
在该反应中体现了_______ 性,下列试剂中能代替 水溶液的是
水溶液的是_______ (选填编号)。
a. 溶液 b. NaCl溶液 c.
溶液 b. NaCl溶液 c. 溶液
溶液
(3)为将B中的溴元素转化为液溴,向反应后B装置的溶液中通入氯气,充分反应,再加入苯,后续的实验操作步骤包含_______ (选填编号)。
a.过滤 b.萃取、分液 c.结晶 d. 蒸馏
(4)将1m3海水浓缩后最终得到21gBr2,若提取率为70%,则海水中溴元素的浓度为_______ g/L。
II.为了从海带中提取碘,该小组设计如下实验:
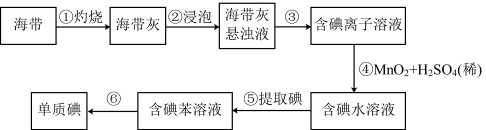
(5)步骤④的作用是_______ (选填编号)。
a. 浓缩 b. 氧化 c. 提取
(6)步骤⑤中选用苯提取碘的原因是_______ 。

回答下列问题:
(1)实验中先向A中通入Cl2,反应的离子方程式是
(2)A中产生的气体被B中的
 水溶液吸收,反应的化学方程式为
水溶液吸收,反应的化学方程式为 在该反应中体现了
在该反应中体现了 水溶液的是
水溶液的是a.
 溶液 b. NaCl溶液 c.
溶液 b. NaCl溶液 c. 溶液
溶液(3)为将B中的溴元素转化为液溴,向反应后B装置的溶液中通入氯气,充分反应,再加入苯,后续的实验操作步骤包含
a.过滤 b.萃取、分液 c.结晶 d. 蒸馏
(4)将1m3海水浓缩后最终得到21gBr2,若提取率为70%,则海水中溴元素的浓度为
II.为了从海带中提取碘,该小组设计如下实验:

(5)步骤④的作用是
a. 浓缩 b. 氧化 c. 提取
(6)步骤⑤中选用苯提取碘的原因是
您最近一年使用:0次
2023-01-13更新
|
332次组卷
|
2卷引用:上海市华东师范大学第三附属中学 2022-2023 学年高一上学期期末考试化学试题
名校
解题方法
2 . 海水的综合利用
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是___________ 。
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是___________ 。
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是___________ 。
A.贝壳在海水提取镁的生产流程中,主要经历了 的过程
的过程
B.工业生产中利用电解熔融 制备镁
制备镁
C.在从海水中提取镁的工业流程中, 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁
(4)下图是海水提溴的工艺流程,下列说法错误的是___________ 。
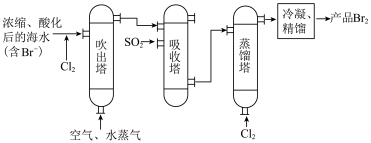
A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为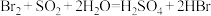
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式___________ 。
②检验阳极产物时可选用___________ ,向阴极附近溶液滴加紫色石蕊试液呈___________ 色。
③实验测得产生的 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为___________  。
。
(6)实验室模拟工业从海藻中提碘的流程如图:
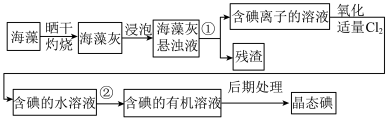
①选择合适实验操作名称填入流程图中:①___________ ,②___________ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
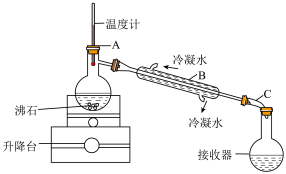
②装置中间部分是“冷凝管”,该装置中有一处明显的错误是___________ 。
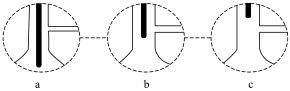
③装置A中,温度计所处的正确位置是___________ 。(选填编号)
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是
A.贝壳在海水提取镁的生产流程中,主要经历了
 的过程
的过程B.工业生产中利用电解熔融
 制备镁
制备镁C.在从海水中提取镁的工业流程中,
 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用
 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁(4)下图是海水提溴的工艺流程,下列说法错误的是

A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为
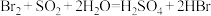
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式
②检验阳极产物时可选用
③实验测得产生的
 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为 。
。(6)实验室模拟工业从海藻中提碘的流程如图:

①选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

②装置中间部分是“冷凝管”,该装置中有一处明显的错误是
③装置A中,温度计所处的正确位置是

您最近一年使用:0次
名校
3 . 从海带中提取碘,经有机溶剂进行富集后,可用反萃取法将I2单质从有机溶剂X中提取出来,其流程如图。下列有关说法错误的是
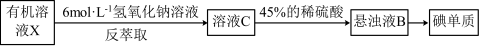
| A.在萃取操作中可采用四氯化碳作为有机溶剂 |
| B.操作过程中由悬浊液B得到碘单质需要的玻璃仪器有烧杯、玻璃棒、漏斗 |
| C.溶液C中碘元素主要以I-形式存在 |
| D.反萃取法的优点在于能耗低且有利于有机溶剂的循环利用 |
您最近一年使用:0次
2023-04-29更新
|
336次组卷
|
5卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
名校
解题方法
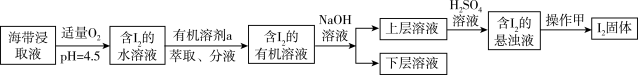
4 . 某学习小组按如下实验流程从海带浸取液中提取碘。 、
、 均为强酸。下列说法错误的是
均为强酸。下列说法错误的是
 、
、 均为强酸。下列说法错误的是
均为强酸。下列说法错误的是A. 的作用是将 的作用是将 转化成离子进入水层,应控制 转化成离子进入水层,应控制 溶液的浓度和体积 溶液的浓度和体积 |
B.加 溶液后分液时,先将下层液体放出后,再从下口将上层液体放出 溶液后分液时,先将下层液体放出后,再从下口将上层液体放出 |
C.加入 溶液,反应的离子方程式为 溶液,反应的离子方程式为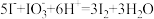 |
| D.操作甲的名称是蒸发 |
您最近一年使用:0次
2022-04-28更新
|
558次组卷
|
7卷引用:山东省菏泽市2021-2022学年高一下学期期中考试化学试题(A)
解题方法
5 . 某同学为了验证海带中含有碘,在实验室进行如下实验。下列说法正确的是
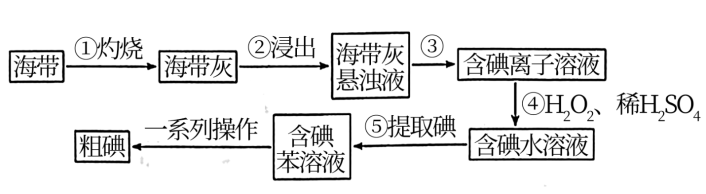

| A.步骤③所需玻璃仪器为漏斗、烧杯、玻璃棒 |
B.步骤④中 的作用为催化剂 的作用为催化剂 |
| C.步骤⑤含碘苯溶液从仪器的下口放出 |
| D.“粗碘”固体中含有少量硫酸钠固体,可采用升华的方法提纯获得碘单质 |
您最近一年使用:0次
2021-07-21更新
|
648次组卷
|
3卷引用:河北省张家口市2020-2021学年高一下学期期末考试化学试题
6 . 海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
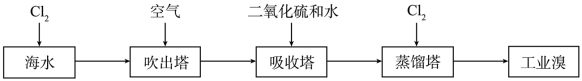
(1)溴元素在元素周期表中的位置为_______ 。
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_______ 。
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______ 。
Ⅱ.海水提镁
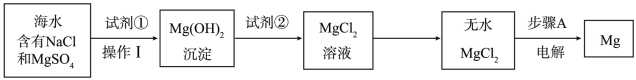
(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(5)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______ 。
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(5)步骤A的化学方程式为
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是
您最近一年使用:0次
2022-07-10更新
|
304次组卷
|
2卷引用:湖北省新高考联考协作体2021-2022学年高一下学期期末考试化学试题
解题方法
7 . 碘元素是人体的必需微量元素之一。某学习小组在实验室进行海带提碘的探究,其流程如下:

上述实验过程中未涉及的操作是

上述实验过程中未涉及的操作是
A.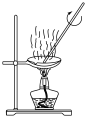 | B.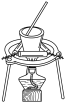 | C.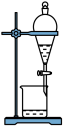 | D.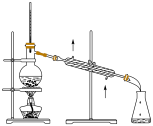 |
您最近一年使用:0次
8 . 溴、碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→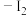 的
的 溶液
溶液
(1)上述实验流程中灼烧用到的仪器是_______ (从下列图中选择,写出名称,下同),萃取分液在_______ 中进行。

(2)“氧化”时加入 和
和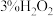 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ 。
(3)检验氧化后的溶液中存在碘单质,可选用的试剂是_______ (填名称)溶液。
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。
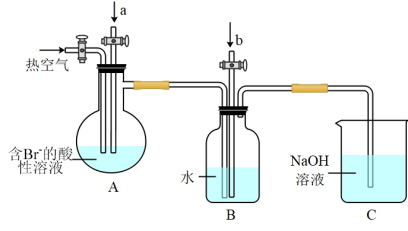
(4)A装置中通入a气体通常为_______ ,发生反应的离子方程式为_______ 。
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是_______ 。
(6)B装置的作用是收集并还原溴,则气体b为_______ 。
(7)C装置的作用是_______ 。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→
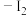 的
的 溶液
溶液(1)上述实验流程中灼烧用到的仪器是

(2)“氧化”时加入
 和
和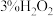 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)检验氧化后的溶液中存在碘单质,可选用的试剂是
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。

(4)A装置中通入a气体通常为
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是
(6)B装置的作用是收集并还原溴,则气体b为
(7)C装置的作用是
您最近一年使用:0次
名校
解题方法
9 . 某同学进行海带提碘实验,部分实验操作如下:将灼烧后的海带灰放入烧杯中,加入蒸馏水充分浸泡后放置在泥三角上,煮沸2~3分钟,冷却后过滤。将适量稀硫酸与双氧水滴入滤液,充分反应后转移至分液漏斗,打开盛有CCl4的试剂瓶,将橡胶塞倒放,取少量加入分液漏斗中,塞紧瓶塞,将分液漏斗多次振荡放气后静置分液,CCl4层从上口倒出。实验中存在错误的有几处
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
2022-01-13更新
|
623次组卷
|
3卷引用:山东省济南市2021-2022学年上学期高三上学期1月学情检测化学试题
10 . 海带中含有碘元素,从海带中提取碘的实验过程如下图所示。

(1)步骤①会用到下列仪器中的_______(填字母)。
(2)海带灰悬浊液含有 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是_______ 。
(3)检验步骤④产生了 的方法是
的方法是_______ 。
(4)步骤⑤“提取”包含以下四个过程。
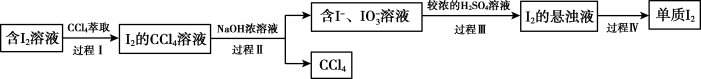
a.过程Ⅰ使用的 体积明显小于含
体积明显小于含 溶液,即可使
溶液,即可使 几乎完全地转移至
几乎完全地转移至 中,推测
中,推测 在
在_______ (填“ ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。
b. 与
与 浓溶液反应的离子方程式是
浓溶液反应的离子方程式是_______ 。
c.过程Ⅰ→过程Ⅲ的目的是_______ 。
d.过程Ⅳ的操作是_______ 。

(1)步骤①会用到下列仪器中的_______(填字母)。
| A.酒精灯 | B.漏斗 | C.坩埚 | D.泥三角 |
 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是(3)检验步骤④产生了
 的方法是
的方法是(4)步骤⑤“提取”包含以下四个过程。

a.过程Ⅰ使用的
 体积明显小于含
体积明显小于含 溶液,即可使
溶液,即可使 几乎完全地转移至
几乎完全地转移至 中,推测
中,推测 在
在 ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。b.
 与
与 浓溶液反应的离子方程式是
浓溶液反应的离子方程式是c.过程Ⅰ→过程Ⅲ的目的是
d.过程Ⅳ的操作是
您最近一年使用:0次



