名校
1 . 乙醛主要用作还原剂、杀菌剂、合成橡胶等,以乙烷为原料合成乙醛的反应机理如图所示。下列说法正确的是
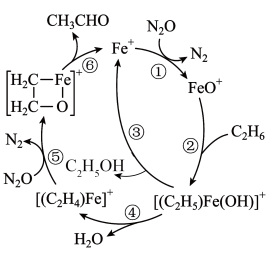
A.反应①中消耗的氧化剂与还原剂的物质的量之比为 |
B.理论上该合成方法中每消耗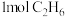 可得到 可得到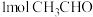 |
C.反应⑤、⑥中均有含 键的产物生成 键的产物生成 |
D.乙醛分子中没有 键,故其与水分子间不能形成氢键 键,故其与水分子间不能形成氢键 |
您最近一年使用:0次
2024-06-05更新
|
189次组卷
|
2卷引用:2024届吉林省吉林市第一中学高三下学期适应性训练化学试题
名校
2 . 连二亚硫酸钠 是一种强碱弱酸盐,利用
是一种强碱弱酸盐,利用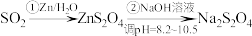 转化制取连二亚硫酸钠的装置如图。已知:
转化制取连二亚硫酸钠的装置如图。已知: 属于两性氢氧化物。下列说法错误的是
属于两性氢氧化物。下列说法错误的是
 是一种强碱弱酸盐,利用
是一种强碱弱酸盐,利用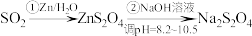 转化制取连二亚硫酸钠的装置如图。已知:
转化制取连二亚硫酸钠的装置如图。已知: 属于两性氢氧化物。下列说法错误的是
属于两性氢氧化物。下列说法错误的是
A.转化①中的氧化剂是 |
| B.开始滴加NaOH溶液的标志是三颈烧瓶中出现浑浊 |
C.调pH至碱性的目的是抑制 水解 水解 |
D.NaOH溶液不能过量,原因是防止 溶解,不利于与 溶解,不利于与 分离 分离 |
您最近一年使用:0次
2024-06-05更新
|
99次组卷
|
2卷引用:2024届吉林省吉林市第一中学高三下学期适应性训练化学试题
名校
解题方法
3 . 东莨菪碱具有扩张毛细血管、改善微循环以及抗晕船晕车等作用,其结构简式如图所示。下列关于东莨菪碱的说法错误的是
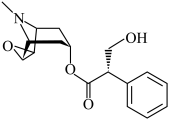
A.能与稀硫酸及 溶液发生反应 溶液发生反应 |
| B.催化氧化后可得到含有醛基的物质 |
| C.苯环上的二氯代物有6种 |
D.完全燃烧时生成的 |
您最近一年使用:0次
2024-06-05更新
|
111次组卷
|
2卷引用:2024届吉林省吉林市第一中学高三下学期适应性训练化学试题
解题方法
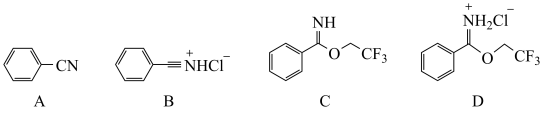
4 . 芳基亚胺酯是重要的有机反应中间体,受热易分解,可由腈在酸催化下与醇发生Pinner反应制备,原理如下图所示。
Ⅱ.向容器中持续通入HCl气体4小时,密封容器。
Ⅲ.室温下在HCl氛围中继续搅拌反应液24小时,冷却至0℃,抽滤得白色固体,用乙腈洗涤。
Ⅳ.将洗涤后的白色固体加入饱和Na2CO3溶液中,在15℃低温下反应,用有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水硫酸钠,抽滤,蒸去溶剂得产品19.50g。
回答下列问题:
(1)实验室中可用浓盐酸和浓硫酸制备干燥HCl气体,下列仪器中一定需要的为_______ (填仪器名称)。_______ (填标号)。_______ ;实验中选择低温的原因为_______ 。
(4)第Ⅳ步萃取时可选用的有机溶剂为_______(填标号)。
(5)第Ⅳ将洗涤后的白色固体加入饱和Na2CO3溶液中,饱和Na2CO3的作用是_______ 。
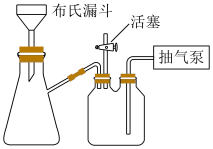
(6)抽滤装置如下图所示,其相对于普通过滤的优点是_______ 。
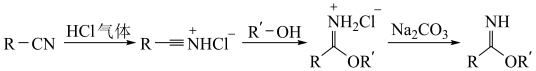
某实验小组以苯甲腈(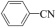 )和三氟乙醇(CF3CH2OH)为原料合成苯甲亚胺三氟乙酯。步骤如下:
)和三氟乙醇(CF3CH2OH)为原料合成苯甲亚胺三氟乙酯。步骤如下:
Ⅱ.向容器中持续通入HCl气体4小时,密封容器。
Ⅲ.室温下在HCl氛围中继续搅拌反应液24小时,冷却至0℃,抽滤得白色固体,用乙腈洗涤。
Ⅳ.将洗涤后的白色固体加入饱和Na2CO3溶液中,在15℃低温下反应,用有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水硫酸钠,抽滤,蒸去溶剂得产品19.50g。
回答下列问题:
(1)实验室中可用浓盐酸和浓硫酸制备干燥HCl气体,下列仪器中一定需要的为

(4)第Ⅳ步萃取时可选用的有机溶剂为_______(填标号)。
| A.甲醇 | B.乙酸 | C.丙酮 | D.乙酸乙酯 |
(5)第Ⅳ将洗涤后的白色固体加入饱和Na2CO3溶液中,饱和Na2CO3的作用是
(6)抽滤装置如下图所示,其相对于普通过滤的优点是
您最近一年使用:0次
解题方法
5 . 我国是最早制得和使用金属锌的国家。某湿法炼锌的萃余液中含有H+、Na+、Zn2+、Fe2+、Mn2+、Co2+、Cd2+、Ni2+、 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
回答下列问题:
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在_______ 区。
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为_______ ,Mn2+被氧化为MnO2,Fe2+与Na2S2O8反应的离子方程式是_______ 。
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有_______ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为: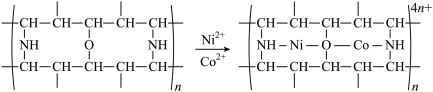 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为_____ 。
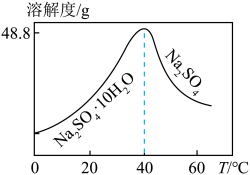
(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为_____ 、洗涤、干燥。_____ 。
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图: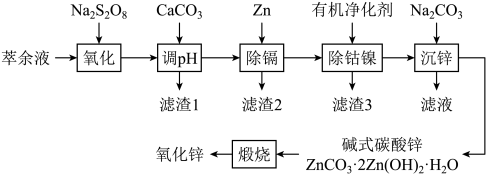
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| Ksp近似值 | 10-38 | 10-17 | 10-17 |
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为:
 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为
您最近一年使用:0次
6 . 化合物 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
是合成抗病毒药物普拉那韦的原料,其合成路线如下。_______ 。
(2)D的化学名称为_______ 。
(3)E→F的反应类型为_______ 。
(4)J的结构简式为_______ 。
(5)M分子中含有两个六元环,则 →M的反应方程式为
→M的反应方程式为_______ 。
(6)在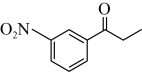 的同分异构体中,满足下列条件的结构有
的同分异构体中,满足下列条件的结构有_______ 种(不考虑立体异构)。
①核磁共振氢谱有5组峰
②遇FeCl3溶液显色
③1mol该物质与银氨溶液反应,最多可生成4molAg
写出其中一种结构简式:_______ 。
 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
是合成抗病毒药物普拉那韦的原料,其合成路线如下。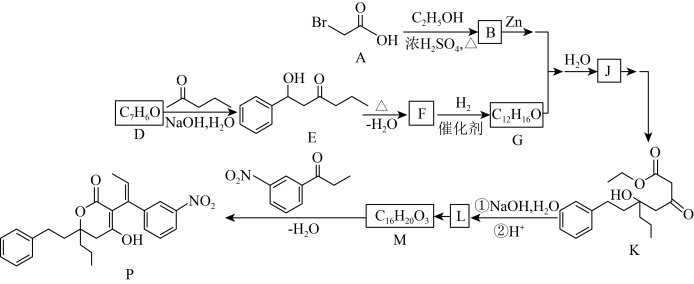
已知: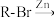
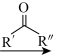

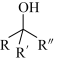
(2)D的化学名称为
(3)E→F的反应类型为
(4)J的结构简式为
(5)M分子中含有两个六元环,则
 →M的反应方程式为
→M的反应方程式为(6)在
 的同分异构体中,满足下列条件的结构有
的同分异构体中,满足下列条件的结构有①核磁共振氢谱有5组峰
②遇FeCl3溶液显色
③1mol该物质与银氨溶液反应,最多可生成4molAg
写出其中一种结构简式:
您最近一年使用:0次
7 . 类比pH,对于稀溶液pc=-lgc,pKa=-lgKa.常温下,向某浓度H2A溶液中加入NaOH(s),保持溶液体积和温度不变,测得pH与pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法正确的是
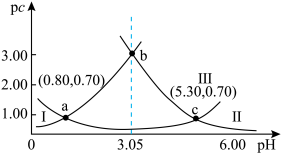
| A.pH=3.05时,c(HA-)>c(A2-)>c(H2A) |
| B.Ka1(H2A)的数量级为10-6 |
| C.c点时,c(Na+)=(10-8.70+3×10-0.7-10-5.30 ) mol·L-1 |
| D.若醋酸的pKa=4.76,则HA-与CH3COO-不能大量共存 |
您最近一年使用:0次
8 . 我国科学家成功合成了世界上首个五氮阴离子盐,局部结构如图所示。其中含有两种10电子离子、一种18电子离子,W、X、Y、Z为原子序数依次增大的短周期元素,Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
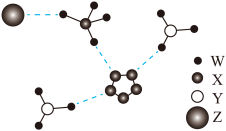
| A.五氮阴离子盐中两种阳离子的立体结构相同 |
| B.X、Y、Z对应的最简单氢化物中沸点最高的是X |
| C.Z的氧化物对应的水化物均为强酸 |
D.五氮阴离子盐中含有的大π键为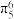 |
您最近一年使用:0次
解题方法
9 . 微生物脱盐电池既可以处理废水中的乙酸和铵盐,又可以实现海水淡化,原理如图所示。下列说法正确的是
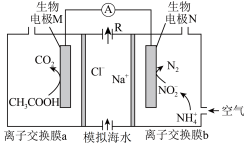
| A.离子交换膜a为阳离子交换膜,b为阴离子交换膜 |
| B.出口R处一定为纯水 |
| C.生成CO2的电极反应式为CH3COOH+2H2O-8e- = 2CO2↑+8H+ |
| D.M极每生成0.1mol CO2,理论上可以从模拟海水中除去117gNaCl |
您最近一年使用:0次
解题方法
10 . 能正确表示下列反应的离子方程式为
A.明矾溶液与过量氨水混合: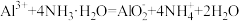 |
| B.氯水久置颜色逐渐褪去:4Cl2+4H2O = HClO4+7HCl |
C.用Na2S2O3做碘量法实验时,pH过低溶液变浑浊: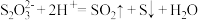 |
D.苯酚钠溶液中通入少量CO2,出现白色浑浊:2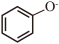 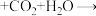 2 2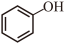 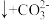 |
您最近一年使用:0次



