名校
1 . 化学与社会、生活及工业生产密切相关。下列有关说法不正确的是
| A.航天器使用的太阳能电池阵和锂离子电池组工作时,均可将化学能转化成电能 |
| B.载人飞船航天器的操纵杆采用的碳纤维属于新型无机非金属材料 |
| C.火箭的整流罩前锥段材料——聚甲基丙烯酰亚胺属于有机高分子材料 |
| D.华为公司自主研发的“麒麟9000芯片”需要以高纯度的硅为原料 |
您最近一年使用:0次
名校
2 . 一种具有消炎止痛功效的有机化合物的结构简式如图所示(虚楔形线、实楔形线分别表示共价键由纸平面向内、向外伸展)。下列说法正确的是
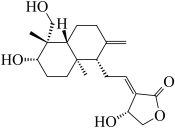
| A.利用质谱仪可测得该分子中官能团的种类有3种 |
| B.该物质可以发生消去反应、取代反应和还原反应 |
| C.该物质的同分异构体中不存在含有酯基、醛基的芳香族化合物 |
| D.1 mol该物质与足量溴的四氯化碳溶液反应,最多可消耗3 mol Br2 |
您最近一年使用:0次
名校
3 . 合成氨反应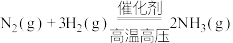 是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
(1)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
①写出N2参与化学吸附的反应方程式:_____________ 。
②以上历程须克服的最大能垒为______ eV。
(2)t℃、0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:
______  ,该反应的
,该反应的
______ (用数字表达式表示,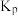 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
②下列叙述能说明该条件下反应达到平衡状态的是______ (填标号)。
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.N2和NH3的平均反应速率之比为1∶2
d.气体密度保持不变
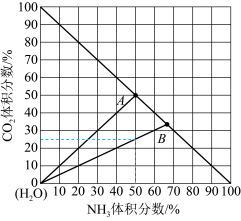
(3)如图是20℃时,NH3-CO2-H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。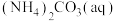 与
与 ,也可选择无水体系反应得到
,也可选择无水体系反应得到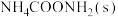 。
。
①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是______ (填“A-H2O”或“B-H2O”)。
②B点可得到的产品是______ (填化学式)。
(4)钌系催化剂是目前合成氨最先进的催化剂。一种钌的化合物晶胞结构如图。该晶胞中与 等距最近的
等距最近的 有
有______ 个,若该晶胞边长为a pm,该晶体的密度为______  (
(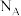 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
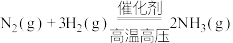 是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:
是目前最有效的工业固氮方法,解决数亿人口生存问题。回答下列问题:(1)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:

①写出N2参与化学吸附的反应方程式:
②以上历程须克服的最大能垒为
(2)t℃、0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:


 ,该反应的
,该反应的
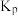 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。②下列叙述能说明该条件下反应达到平衡状态的是
a.氨气的体积分数保持不变
b.容器中氢氮比保持不变
c.N2和NH3的平均反应速率之比为1∶2
d.气体密度保持不变
(3)如图是20℃时,NH3-CO2-H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。
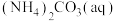 与
与 ,也可选择无水体系反应得到
,也可选择无水体系反应得到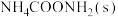 。
。①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是
②B点可得到的产品是
(4)钌系催化剂是目前合成氨最先进的催化剂。一种钌的化合物晶胞结构如图。该晶胞中与
 等距最近的
等距最近的 有
有 (
(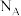 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
4 . 化合物Ⅷ是一种用于制备神经抑制剂的中间体,其合成路线如下:
(1)化合物Ⅰ的分子式是________ 。化合物Ⅷ中的非含氧官能团的名称是________ 。
(2)化合物Ⅰ的沸点高于化合物Ⅱ,其原因是____________ 。
(3)反应①是原子利用率100%的反应,则a为________ 。
(4)反应②的反应类型为________ 。
(5)化合物Ⅲ有多种同分异构体,其中含 结构的有
结构的有________ 种(不计Ⅲ),其中核磁共振氢谱的峰面积比为6∶1∶1的结构简式为________ (写出其中一种)。
(6)写出以 和乙醇为原料合成化合物
和乙醇为原料合成化合物 的单体的合成路线(无机试剂任用)
的单体的合成路线(无机试剂任用)_______________ 。

(1)化合物Ⅰ的分子式是
(2)化合物Ⅰ的沸点高于化合物Ⅱ,其原因是
(3)反应①是原子利用率100%的反应,则a为
(4)反应②的反应类型为
(5)化合物Ⅲ有多种同分异构体,其中含
 结构的有
结构的有(6)写出以
 和乙醇为原料合成化合物
和乙醇为原料合成化合物 的单体的合成路线(无机试剂任用)
的单体的合成路线(无机试剂任用)
您最近一年使用:0次
名校
解题方法
5 . 一种制备 的工艺路线如图所示,反应
的工艺路线如图所示,反应 所得溶液pH在3~4之间,反应
所得溶液pH在3~4之间,反应 需及时补加
需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数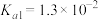 ,
,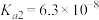 。下列说法正确的是
。下列说法正确的是
 的工艺路线如图所示,反应
的工艺路线如图所示,反应 所得溶液pH在3~4之间,反应
所得溶液pH在3~4之间,反应 需及时补加
需及时补加 以保持反应在
以保持反应在 条件下进行。常温下,
条件下进行。常温下, 的电离平衡常数
的电离平衡常数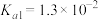 ,
,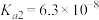 。下列说法正确的是
。下列说法正确的是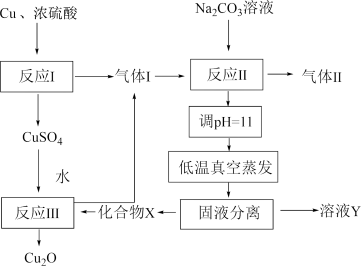
A.反应 、 、 、 、 均为氧化还原反应 均为氧化还原反应 |
B.低温真空蒸发主要目的是防止 被氧化 被氧化 |
C.溶液Y可循环用于反应 所在操作单元吸收气体 所在操作单元吸收气体 |
D.若 产量不变,参与反应 产量不变,参与反应 的X与 的X与 物质的量之比 物质的量之比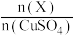 增大时,需补加 增大时,需补加 的量增多 的量增多 |
您最近一年使用:0次
2024-06-10更新
|
100次组卷
|
4卷引用:福建省福州第三中学2023-2024学年高三上学期第五次质量检测化学试题
名校
6 . 下列实验操作、现象与结论相匹配的是
选项 | 实验操作 | 现象 | 结论 |
A | 常温,分别测定浓度均为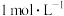 NaCl溶液和CH3COONH4溶液的pH NaCl溶液和CH3COONH4溶液的pH | pH均等于7 | 常温下,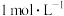 的NaCl溶液和CH3COONH4溶液中水的电离程度相等 的NaCl溶液和CH3COONH4溶液中水的电离程度相等 |
B | 常温,将50 mL苯与50 mL CH3COOH混合 | 混合溶液体积为101 mL | 混合过程中削弱了CH3COOH分子间的氢键,且CH3COOH分子与苯间的作用弱于氢键 |
C | 向Na2SO3和Na2S混合溶液中加入浓硫酸 | 溶液中出现淡黄色沉淀 | +4价和-2价硫可归中为0价 |
D | 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上 | 一段时间后鸡皮变黄 | 鸡皮中含有脂肪 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 镀锌钢构件的酸洗废液中含有2.5mol。L-1盐酸、50%FeCl2·4H2O和2%ZnCl2。实验室从酸洗废液中回收盐酸和FeCl2·4H2O的实验流程如下:
回答下列问题:
I.回收盐酸和FeCl2·4H2O粗产品
(1)操作1应选择___________ (填序号)。
A.水浴加热 B.油浴加热 C.投入沸石
(2)为了获得FeCl2·4H2O粗产品,应加热至留有少量残余液时立即停止。
①立即停止可以避免Fe2+被氧化外,还能___________ 。
②如果残余液过多,可能会导致___________ 。(答一条)
Ⅱ.FeCl2·4H2O粗产品的重结晶
(3)检验FeCl2·4H2O粗产品中含有Fe3+的操作方法是___________ 。
(4)重结晶前加入的物质X为___________ ;操作2的名称是___________ 。
Ⅲ.滴定亚铁离子,测定FeCl2·4H2O晶体纯度
准确称取ag重结晶后的FeCl2·4H2O晶体,溶于酸中并定容至100mL。移取三份25.00mL溶液,滴加几滴指示剂,用cmol。L-1K2Cr2O7标准溶液滴定至终点,半分钟内不恢复原色,消耗K2Cr2O7标准溶液平均体积为VmL(此时Cl-不被氧化)。(M【FeCl2·4H2O】=199 g·mol-1)
(5)计算FeCl2·4H2O晶体的纯度为___________ %(用含a、c的最简代数式表示)。
(6)亚甲基蓝可用作以上指示剂,其结构式如下图。MB可用N,N-二甲基苯胺(DMA)为原料制得。___________ 。
②亚甲基蓝中N原子的杂化方式有___________ 。
③DMA的碱性比苯胺强,说明理由___________ 。
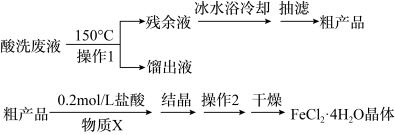
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| FeCl2 | 49.7 | 59.0 | 62.5 | 66.7 | 70.0 | 78.3 | 88.7 | 94.9 |
| ZnCl2 | 342 | 363 | 395 | 437 | 452 | 488 | 541 | 614 |
I.回收盐酸和FeCl2·4H2O粗产品
(1)操作1应选择
A.水浴加热 B.油浴加热 C.投入沸石
(2)为了获得FeCl2·4H2O粗产品,应加热至留有少量残余液时立即停止。
①立即停止可以避免Fe2+被氧化外,还能
②如果残余液过多,可能会导致
Ⅱ.FeCl2·4H2O粗产品的重结晶
(3)检验FeCl2·4H2O粗产品中含有Fe3+的操作方法是
(4)重结晶前加入的物质X为
Ⅲ.滴定亚铁离子,测定FeCl2·4H2O晶体纯度
准确称取ag重结晶后的FeCl2·4H2O晶体,溶于酸中并定容至100mL。移取三份25.00mL溶液,滴加几滴指示剂,用cmol。L-1K2Cr2O7标准溶液滴定至终点,半分钟内不恢复原色,消耗K2Cr2O7标准溶液平均体积为VmL(此时Cl-不被氧化)。(M【FeCl2·4H2O】=199 g·mol-1)
(5)计算FeCl2·4H2O晶体的纯度为
(6)亚甲基蓝可用作以上指示剂,其结构式如下图。MB可用N,N-二甲基苯胺(DMA)为原料制得。

②亚甲基蓝中N原子的杂化方式有
③DMA的碱性比苯胺强,说明理由
您最近一年使用:0次
解题方法
8 . 以辉铋矿(主要成分为Bi2S3,含有FeS2、SiO2杂质)和软锰矿(主要成分为MnO2)为原料制备超细氧化铋的工艺流程如下: ,
, 易发生水解,其反应的离子方程式为:
易发生水解,其反应的离子方程式为: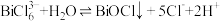 。
。
(1)Bi元素位于第6周期VA族,其价电子轨道表示式为___________ ,BiOCl叫氯氧化铋而不叫次氯酸铋,从化合价角度分析原因为___________ 。
(2)“联合焙烧”时,Bi2S3和MnO2在空气中反应生成Bi2O3和MnSO4.该反应的化学方程式为___________ 。
(3)BiCl 能被有机萃取剂(TBP)苯取,其萃取原理可表示为:
能被有机萃取剂(TBP)苯取,其萃取原理可表示为: 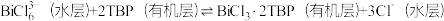 。
。
①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图所示。c(Cl-)最佳为1.3mol·L-1的可能原因是___________ 。
②萃取后分液所得水相中的主要阳离子为___________ (填化学式)。___________ 。
(5)在空气中加热分解草酸铋晶体,测得升温加热过程中剩余固体的质量与起始Bi2(C2O4)3·7H2O的质量的比值随温度变化的关系如图所示。400℃时制得超细氧化铋,其化学式为___________ 。(M[Bi2(C2O4)3·7H2O]=808g·mol-1)

 ,
, 易发生水解,其反应的离子方程式为:
易发生水解,其反应的离子方程式为: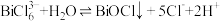 。
。(1)Bi元素位于第6周期VA族,其价电子轨道表示式为
(2)“联合焙烧”时,Bi2S3和MnO2在空气中反应生成Bi2O3和MnSO4.该反应的化学方程式为
(3)BiCl
 能被有机萃取剂(TBP)苯取,其萃取原理可表示为:
能被有机萃取剂(TBP)苯取,其萃取原理可表示为: 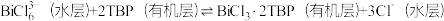 。
。①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图所示。c(Cl-)最佳为1.3mol·L-1的可能原因是
②萃取后分液所得水相中的主要阳离子为

(5)在空气中加热分解草酸铋晶体,测得升温加热过程中剩余固体的质量与起始Bi2(C2O4)3·7H2O的质量的比值随温度变化的关系如图所示。400℃时制得超细氧化铋,其化学式为

您最近一年使用:0次
9 . Hoffman降解是二种由酰胺合成氨的方法。县有产率高、纯度高等优点,在合成上有重要应用。一种用Hoffman降解合成普瑞巴林(pregabal)的合成路线: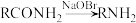
回答下列问题:
(1)B中官能团的名称为___________ 。
(2)只用一种试剂鉴别A、B、C,该试剂是___________ 。
(3)D→E的反应类型是___________ 。
(4)写出B→C的化学反应方程式___________ 。
(5)写出G的结构简式___________ 。
(6)X是B的同分异构体,分子中含一个五元环。能发生银镜反应,但不能使溴的CCl4溶液褪色,其中1H-NMR谱显示有5组峰,且峰面积之比为4:4:2:1:1的结构简式为___________ 。

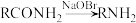
回答下列问题:
(1)B中官能团的名称为
(2)只用一种试剂鉴别A、B、C,该试剂是
(3)D→E的反应类型是
(4)写出B→C的化学反应方程式
(5)写出G的结构简式
(6)X是B的同分异构体,分子中含一个五元环。能发生银镜反应,但不能使溴的CCl4溶液褪色,其中1H-NMR谱显示有5组峰,且峰面积之比为4:4:2:1:1的结构简式为
您最近一年使用:0次
10 . 乙二胺四乙酸(EDTA)是一种重要的络合剂,其能与绝大多数的金属离子形成稳定的配合物,简易机理如图所示。下列叙述错误的是

| A.EDTA的核磁共振氢谱上有3组峰 | B.EDTA中含有两种官能团 |
| C.螯合物中含有4个sp2-pπ键 | D.螯合物中有5个五元螯合环 |
您最近一年使用:0次



