1 . 下列实验操作能达到目的的是
| 选项 | 目的 | 操作 |
| A | 制备Fe(OH)3胶体 | 向煮沸的蒸馏水中滴加5~ 6滴饱和FeCl3溶液,继续煮沸至出现红褐色沉淀 |
| B | 验证食品包装袋内一小包脱氧剂中还原铁粉变质 | 取少量样品溶于盐酸,加入K3[Fe(CN)6]溶液 |
| C | 制备无水AlCl3 | 在HCl气流中加热AlCl3•6H2O |
| D | 证明乙烯具有还原性 | 将溴乙烷与氢氧化钠的乙醇溶液共热,将导管直接通入酸性高锰酸钾溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-22更新
|
469次组卷
|
3卷引用:山东省2021届高三百师联盟二轮复习联考化学试题
名校
2 . “绿色化学”是化工生产中的重要理念。下图为利用尿素工厂废气以及磷肥工厂废渣(液)联合生产硫酸铵的工艺流程。
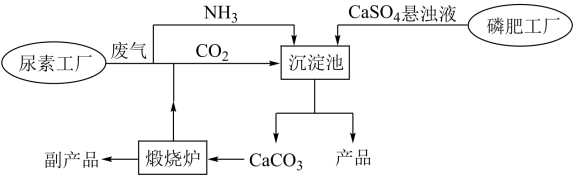
完成下列填空:
(1)沉淀池中发生反应的化学方程式为___________ 。已知硫酸铵溶解度变化趋势与氯化钠相似,则从沉淀池中获得产品的操作包含___________ 、___________ 、洗涤、烘干等。
(2)流程中体现“绿色化学”理念的设计有___________ 、___________ 等。
(3)为在实验室模拟沉淀池中的反应,设计了如图所示的装置,导管a下端连接粗管的目的是___________ ;导管b下端使用多孔球泡的目的是___________ 。
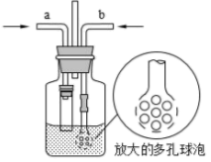
可用甲醛法测定所得 样品中氮的质量分数。其反应原理可以表示为:
样品中氮的质量分数。其反应原理可以表示为:
 [已知:
[已知: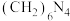 不与NaOH反应]
不与NaOH反应]
实验过程:称取样品1.500g,溶解配制成250mL溶液,取25.00mL样品溶液于锥形瓶中,加入过量的甲醛溶液,摇匀、静置5min后,加入1~2滴甲基橙试液,用NaOH标准溶液滴定至终点。
(4)终点的判断依据是___________ 。
(5)已知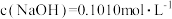 ,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为
,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为___________ 。(保留4位小数),实验测得硫酸铵样品中氮的质量分数略高,原因可能是___________ 。
a.甲醛被氧化 b.没有进行平行实验
c.氢氧化钠溶液久置变质 d.锥形瓶没有用待测液润洗

完成下列填空:
(1)沉淀池中发生反应的化学方程式为
(2)流程中体现“绿色化学”理念的设计有
(3)为在实验室模拟沉淀池中的反应,设计了如图所示的装置,导管a下端连接粗管的目的是

可用甲醛法测定所得
 样品中氮的质量分数。其反应原理可以表示为:
样品中氮的质量分数。其反应原理可以表示为: [已知:
[已知: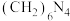 不与NaOH反应]
不与NaOH反应]实验过程:称取样品1.500g,溶解配制成250mL溶液,取25.00mL样品溶液于锥形瓶中,加入过量的甲醛溶液,摇匀、静置5min后,加入1~2滴甲基橙试液,用NaOH标准溶液滴定至终点。
(4)终点的判断依据是
(5)已知
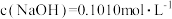 ,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为
,消耗氢氧化钠溶液20.00mL,则所得硫酸铵样品中氮的质量分数为a.甲醛被氧化 b.没有进行平行实验
c.氢氧化钠溶液久置变质 d.锥形瓶没有用待测液润洗
您最近一年使用:0次
2021-04-20更新
|
351次组卷
|
4卷引用:上海市浦东新区2021届高三二模化学试题
上海市浦东新区2021届高三二模化学试题(已下线)化学-2022年高考押题预测卷02(上海卷)(含考试版、全解全析、参考答案、答题卡)(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)上海市宝山区行知中学-2021-2022学年高三下学期3月月考化学试题
3 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 某 固体样品溶于水,加入 固体样品溶于水,加入 溶液,充分反应后,再加稀盐酸,白色沉淀不溶解 溶液,充分反应后,再加稀盐酸,白色沉淀不溶解 | 不能判断该 ,样品已变质 ,样品已变质 |
| B | 将乙醇与浓硫酸混合加热,产生的气体通入酸性 溶液,溶液紫红色褪去 溶液,溶液紫红色褪去 | 产生的气体中一定含有乙烯 |
| C | 取蔗糖水解后的溶液加入少量新制的 悬浊液加热煮沸,没有红色沉淀 悬浊液加热煮沸,没有红色沉淀 | 蔗糖没有水解 |
| D | 向 和 和 的混合溶液中滴入少量 的混合溶液中滴入少量 溶液,产生淡黄色 溶液,产生淡黄色 沉淀 沉淀 | 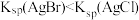 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-10更新
|
617次组卷
|
2卷引用:辽宁省沈阳市(东北三省四城市)2021届高考二模(高三质量监测二)化学试题
名校
4 . 天空课堂第二课中航天员展示了金属锆(40Zr)在无容器实验柜中从液体变成固体时的“再辉”现象。以锆英石(主要成分是ZrSiO4,还含有少量Al2O3、SiO2、Fe2O3等杂质)为原料生产锆的流程如图所示:
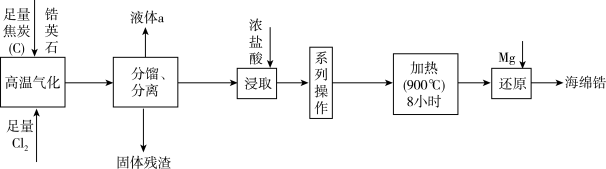
已知:常温下,ZrCl4是白色固体, 604K升华,遇水强烈水解:ZrCl4+9H2O=ZrOCl2·8H2O+2HCl,在浓盐酸中会析出ZrOCl2·8H2O沉淀。请回答下列问题:
(1)“高温气化”中可发生多个反应,写出发生的主要反应的化学方程式是_______ 。
(2)分馏过程中,为防止产品变质,过程中一定需要注意的是_______ 。液体a的电子式是_______ 。
(3)实验室中洗涤ZrOCl2·8H2O沉淀操作是_______ 。
(4)“还原”中氧化剂是_______ (填化学式)。
(5)由于锆铪(Hf)矿石共生,这样制得的锆中常含有少量的铪,需要进一步分离提纯。
第一步:溶解分离
将样品溶于氢氟酸后再加入一定量KOH溶液,锆和铪均以[MF6]2-存在。
①已知在水中K2HfF6比K2ZrF6的溶解度大,且K2ZrF6的溶解度随温度的升高而增大,可以利用_______
方法进行分离。
②离子交换法:利用强碱型酚醛树脂R-N(CH3) Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是
Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是_______ 。
③将所得溶液与有机相磷酸三丁酯(TBP)充分混合、振荡,可以达到Zr与Hf分离。这种分离方法是_______ 。
第二步:高温还原
在高温条件下,加入铝将制得的K2ZrF6还原可得锆,反应的化学方程式是_______ 。

已知:常温下,ZrCl4是白色固体, 604K升华,遇水强烈水解:ZrCl4+9H2O=ZrOCl2·8H2O+2HCl,在浓盐酸中会析出ZrOCl2·8H2O沉淀。请回答下列问题:
(1)“高温气化”中可发生多个反应,写出发生的主要反应的化学方程式是
(2)分馏过程中,为防止产品变质,过程中一定需要注意的是
(3)实验室中洗涤ZrOCl2·8H2O沉淀操作是
(4)“还原”中氧化剂是
(5)由于锆铪(Hf)矿石共生,这样制得的锆中常含有少量的铪,需要进一步分离提纯。
第一步:溶解分离
将样品溶于氢氟酸后再加入一定量KOH溶液,锆和铪均以[MF6]2-存在。
①已知在水中K2HfF6比K2ZrF6的溶解度大,且K2ZrF6的溶解度随温度的升高而增大,可以利用
方法进行分离。
②离子交换法:利用强碱型酚醛树脂R-N(CH3)
 Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是
Cl-阴离子交换剂进行交换分离,原理是:2RN(CH3)3Cl+K2ZrF6= [RN(CH3)3]ZrF6+2 KCl;2RN(CH3)3Cl+K2HfF6=[RN(CH3)3]HfF6+2 KCl。然后再用HF和HCl混合溶液为淋洗剂,先后将这两种阴离子淋洗下来,达到分离的目的。这种方法能够将锆、铪分离的原因是③将所得溶液与有机相磷酸三丁酯(TBP)充分混合、振荡,可以达到Zr与Hf分离。这种分离方法是
第二步:高温还原
在高温条件下,加入铝将制得的K2ZrF6还原可得锆,反应的化学方程式是
您最近一年使用:0次
5 . SO2和焦亚硫酸钠(Na2S2O5)可用作食品添加剂。回答下列问题:
(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为_______ 。欲净化与收集SO2,选择必要装置,按气流方向连接顺序为_______ (填仪器接口的字母编号)。
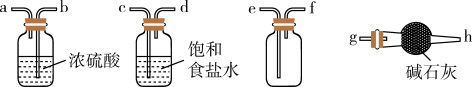
(2)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
已知:2NaHSO3 Na2S2O5+H2O。
Na2S2O5+H2O。
试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
(3)某小组利用下列装置测定空气中SO2的含量。
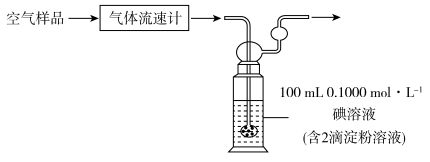
已知该反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI。若空气流速为a m3·min-1,当观察到_______ 时,结束计时,测定耗时t min。假定样品中的SO2可被溶液充分吸收,该空气样品中SO2的含量是_______ mg·m-3。
(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为

(2)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
已知:2NaHSO3
 Na2S2O5+H2O。
Na2S2O5+H2O。试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
| 实验编号 | 实验步骤 | 现象 | 结论 |
| I | 取少量样品,加入除氧蒸馏水 | 固体完全溶解得到无色溶液 | / |
| II | 取实验I的溶液, | 样品已氧化变质 | |
| III | 另取实验I的溶液, | 样品未完全氧化变质 |

已知该反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI。若空气流速为a m3·min-1,当观察到
您最近一年使用:0次
2022-04-22更新
|
1289次组卷
|
5卷引用:广东省广州市2022届高三下学期二模综合测试化学试题
广东省广州市2022届高三下学期二模综合测试化学试题(已下线)化学-2022年高考押题预测卷01(天津卷)(已下线)押广东卷化学第17题 化学实验综合题-备战2022年高考化学临考题号押题(广东卷)(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(练)-2023年高考化学一轮复习讲练测(全国通用)超重点10 高考必考元素——氧、硫
6 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究乙醇消去反应的产物 | 取4mL乙醇,加入12mL浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入2mL溴水中 | 若溴水褪色,则乙醇消去反应的产物为乙烯 |
| B | 探究淀粉是否水解 | 淀粉与稀硫酸混合一段时间后,滴加银氨溶液并水浴加热 | 无银镜出现,说明淀粉没水解 |
| C | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| D | 探究Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究乙醇消去反应的产物 | 取 乙醇,加入 乙醇,加入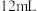 浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入 浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入 溴水中 溴水中 | 若溴水褪色,则乙醇消去反应的产物为乙烯 |
| B | 探究乙酰水杨酸样品中是否含有水杨酸 | 取少量样品,加入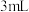 蒸馏水和少量乙醇,振荡,再加入1-2滴 蒸馏水和少量乙醇,振荡,再加入1-2滴 溶液 溶液 | 若有紫色沉淀生成,则该产品中含有水杨酸 |
| C | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入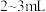 蒸馏水 蒸馏水 | 若无气体生成,则固体粉末为 ;若有气体生成,则固体粉末为 ;若有气体生成,则固体粉末为 |
| D | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-15更新
|
7004次组卷
|
15卷引用:2021年6月浙江高考化学试题变式题21-25
(已下线)2021年6月浙江高考化学试题变式题21-252021年6月新高考浙江化学高考真题(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题17.基础实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题16 基础化学实验-2022年高考化学二轮复习重点专题常考点突破练(已下线)秘籍05 微型实验方案设计与评价-备战2022年高考化学抢分秘籍(全国通用)(已下线)第27讲 物质的制备与性质实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点33 物质的制备-备战2023年高考化学考试易错题(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
解题方法
8 . 氨基甲酸铵(H2NCOONH4)是一种重要的化工原料,可用作化学肥料、灭火剂、洗涤剂等。某化学兴趣小组用以下装置制取氨基甲酸铵。
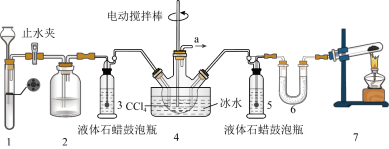
已知:①制取氨基甲酸铵反应为: 2NH3(g)+CO2(g)⇌H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是_______
(2)装置6中的试剂是_______ ,导管a出口直接与尾气处理装置连接,该尾气处理装置中的试剂是_______ 。
(3)装置7中发生反应的化学方程式为_______
(4)三颈烧瓶需用冰水浴冷却,其目的是_______
(5) CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是_______ ,从三颈烧瓶中分离出粗产品的操作是_______
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是_______ [Mr(H2NCOONH4)=78、Mr(NH4HCO3)=79]

已知:①制取氨基甲酸铵反应为: 2NH3(g)+CO2(g)⇌H2NCOONH4(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是
(2)装置6中的试剂是
(3)装置7中发生反应的化学方程式为
(4)三颈烧瓶需用冰水浴冷却,其目的是
(5) CCl4液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨基甲酸铵的质量分数是
您最近一年使用:0次
解题方法
9 . 下列实验方案中,能实现实验目的的是
| 实验目的 | 实验方案 | |
| A | 检验露置的Na2SO3是否变质 | 用盐酸酸化的BaCl2溶液 |
| B | 缩短容量瓶干燥的时间 | 将洗净的容量瓶放在烘箱中烘干 |
| C | 测定Na2CO3(含NaCl)样品纯度 | 取一定质量的样品与足量盐酸反应,用碱石灰吸收产生的气体 |
| D | 验证氧化性强弱:Ag+>Fe2+ | 向FeCl2和KSCN的混合溶液中滴入酸化的AgNO3溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列设计的实验方案能达到实验目的的是
| A.提纯含有少量苯的苯酚:向含有少量苯的苯酚中加入过量氢氧化钠溶液,振荡后静置分液,除去有机相 |
| B.探究温度对化学平衡移动的影响:将盛有NO2和N2O4混合气体的平衡球,分别置于冷水和热水中,观察气体颜色的变化 |
| C.将硝酸亚铁样品溶于稀硫酸,滴加硫氰化钾溶液,溶液变为血红色,可推知该样品已经氧化变质 |
| D.实验室常用浓硫酸与NaCl共热制取少量HCl,也可以用浓硫酸与KI共热制取HI |
您最近一年使用:0次



