解题方法
1 . Co、La元素及其化合物在工业及生活方面有重要应用。回答下列问题:
(1)基态Co的价电子排布图_______ ,核外电子的空间运动状态有_______ 种。
(2)一定条件下, 、
、 、
、 和
和 反应可制得
反应可制得 ,反应的方程式为
,反应的方程式为_______ , 的配位数为
的配位数为_______ 。区别 和
和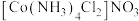 两种溶液的试剂是
两种溶液的试剂是_______ 。
(3) 的八配位金属羰基化合物
的八配位金属羰基化合物 的结构如图所示,
的结构如图所示, 作配体,配位原子为C,而不是O,其原因是
作配体,配位原子为C,而不是O,其原因是_______ ,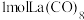 含
含_______  键。
键。 在储氢和超导等领域具有重要应用。高压下,
在储氢和超导等领域具有重要应用。高压下, 中的每个
中的每个 结合4个
结合4个 形成类似
形成类似 的结构独立存在,即得到晶体
的结构独立存在,即得到晶体 。则
。则
_______ 。晶体 的密度为
的密度为_______  。(写出计算式即可)
。(写出计算式即可)
(1)基态Co的价电子排布图
(2)一定条件下,
 、
、 、
、 和
和 反应可制得
反应可制得 ,反应的方程式为
,反应的方程式为 的配位数为
的配位数为 和
和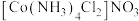 两种溶液的试剂是
两种溶液的试剂是(3)
 的八配位金属羰基化合物
的八配位金属羰基化合物 的结构如图所示,
的结构如图所示, 作配体,配位原子为C,而不是O,其原因是
作配体,配位原子为C,而不是O,其原因是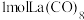 含
含 键。
键。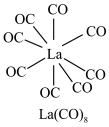
 在储氢和超导等领域具有重要应用。高压下,
在储氢和超导等领域具有重要应用。高压下, 中的每个
中的每个 结合4个
结合4个 形成类似
形成类似 的结构独立存在,即得到晶体
的结构独立存在,即得到晶体 。则
。则
 的密度为
的密度为 。(写出计算式即可)
。(写出计算式即可)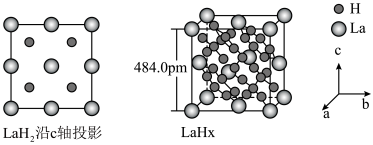
您最近一年使用:0次
2 . 二维磁性材料卤化铬 混合晶体结构如图,在纯氧中发生光氧化反应生成长链状
混合晶体结构如图,在纯氧中发生光氧化反应生成长链状 和
和 。下列说法错误的是
。下列说法错误的是
 混合晶体结构如图,在纯氧中发生光氧化反应生成长链状
混合晶体结构如图,在纯氧中发生光氧化反应生成长链状 和
和 。下列说法错误的是
。下列说法错误的是
A.化学键中离子键成分百分数: |
B. |
| C.生成1mol X―X键转移3mol电子 |
D.熔点: |
您最近一年使用:0次
3 . 从铅银渣(含Pb、Ag、Cu等金属元素)中提取银的流程如图。

| A.“酸浸”过程中可用稀HNO3代替NaNO3 |
B.“络合浸出”时,发生的离子反应为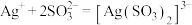 |
| C.浸渣的主要成分是PbSO4 |
D.“还原析银”时,氧化产物与还原产物的物质的量之比为 |
您最近一年使用:0次
解题方法
4 . 高纯二硫化钼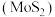 粉体被誉为“固体润滑之王”。由钼精矿(主要成分为
粉体被誉为“固体润滑之王”。由钼精矿(主要成分为 ,还有少量
,还有少量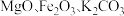 等)制备高纯
等)制备高纯 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)“焙烧”时生成 的化学方程式为
的化学方程式为___________ ;“水洗”的目的是___________ 。
(2)“转化”过程中,存在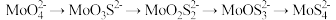 。
。
① 转化为
转化为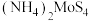 的化学方程式为
的化学方程式为___________ 。
②保持温度为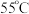 反应
反应 后,冷却至
后,冷却至 并静置
并静置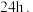 测得
测得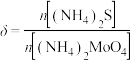 对
对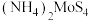 晶体产率的影响如图所示。
晶体产率的影响如图所示。 时,
时,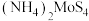 晶体产率为0的原因是
晶体产率为0的原因是___________ ; 时,
时,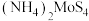 晶体产率继续增大的原因是
晶体产率继续增大的原因是___________ 。
(3)“酸浸”和“高温还原”中产生的气体可通入___________ (填操作单元的名称)中循环使用。
(4) 也可由
也可由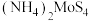 在一定条件下加热分解制得,同时产生
在一定条件下加热分解制得,同时产生 和某种硫单质,且
和某种硫单质,且 与硫单质的物质的量之比为
与硫单质的物质的量之比为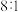 ,则硫单质的分子式为
,则硫单质的分子式为___________ 。
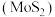 粉体被誉为“固体润滑之王”。由钼精矿(主要成分为
粉体被誉为“固体润滑之王”。由钼精矿(主要成分为 ,还有少量
,还有少量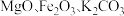 等)制备高纯
等)制备高纯 的一种工艺流程如图所示。
的一种工艺流程如图所示。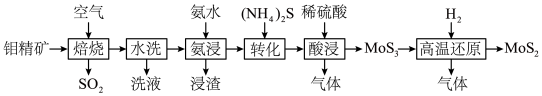
(1)“焙烧”时生成
 的化学方程式为
的化学方程式为(2)“转化”过程中,存在
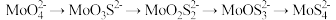 。
。①
 转化为
转化为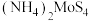 的化学方程式为
的化学方程式为②保持温度为
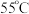 反应
反应 后,冷却至
后,冷却至 并静置
并静置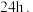 测得
测得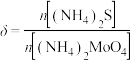 对
对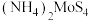 晶体产率的影响如图所示。
晶体产率的影响如图所示。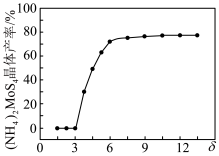
 时,
时,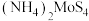 晶体产率为0的原因是
晶体产率为0的原因是 时,
时,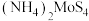 晶体产率继续增大的原因是
晶体产率继续增大的原因是(3)“酸浸”和“高温还原”中产生的气体可通入
(4)
 也可由
也可由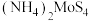 在一定条件下加热分解制得,同时产生
在一定条件下加热分解制得,同时产生 和某种硫单质,且
和某种硫单质,且 与硫单质的物质的量之比为
与硫单质的物质的量之比为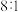 ,则硫单质的分子式为
,则硫单质的分子式为
您最近一年使用:0次
名校
解题方法
5 . 二氯异氰尿酸钠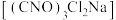 具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和
具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和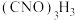 (氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(1)装置B中试剂为___________ 。
(2) 的制备步骤如下:
的制备步骤如下:
①检查装置气密性后加入药品。
②关闭K1,打开K2,向A中滴加足量的浓盐酸,关闭K2,当观察到___________ 时,滴入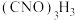 的吡啶溶液,写出
的吡啶溶液,写出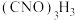 和NaClO发生反应的化学方程式
和NaClO发生反应的化学方程式___________ 。制备过程中要不断通入Cl2,其目的是___________ ,反应完成后需进行的操作为___________ 。
③取装置D中溶液,制得产品。操作为___________ 、过滤、冷水洗涤、低温干燥得到粗产品。
(3)粗产品中 纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量
纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量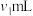
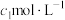 的AgNO3溶液,加入几滴稀
的AgNO3溶液,加入几滴稀 溶液,用
溶液,用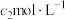 NH4SCN标准溶液滴定至终点,消耗
NH4SCN标准溶液滴定至终点,消耗 标准液。[已知:
标准液。[已知: (白色)]
(白色)]
① (摩尔质量为
(摩尔质量为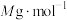 )的纯度为
)的纯度为___________ 。
②下列有关上述滴定操作的说法正确的是___________ 。
a.接近滴定终点时微微转动活塞,使溶液悬挂在尖嘴上,形成半滴,用锥形瓶内壁将其刮落
b.若盛放NH4SCN标准溶液的滴定管没有润洗,使测定结果偏大
c.锥形瓶洗涤后未干燥即加入所配待测溶液,使测定结果偏小
d.滴定前俯视读数,滴定后仰视读数,使测定结果偏小
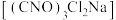 具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和
具有很强的氧化性(遇酸会生成次氯酸),是一种广普高效的杀菌剂,常温下为白色固体、溶于水,难溶于冰水。实验室常用高浓度的NaClO溶液和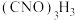 (氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(氰尿酸)溶液,在10℃时反应制备二氯异氰尿酸钠,实验装置如图所示:
(1)装置B中试剂为
(2)
 的制备步骤如下:
的制备步骤如下:①检查装置气密性后加入药品。
②关闭K1,打开K2,向A中滴加足量的浓盐酸,关闭K2,当观察到
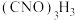 的吡啶溶液,写出
的吡啶溶液,写出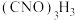 和NaClO发生反应的化学方程式
和NaClO发生反应的化学方程式③取装置D中溶液,制得产品。操作为
(3)粗产品中
 纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量
纯度测定。取m g粗产品溶于少量水,加入过量维生素C充分反应,再加入过量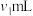
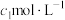 的AgNO3溶液,加入几滴稀
的AgNO3溶液,加入几滴稀 溶液,用
溶液,用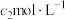 NH4SCN标准溶液滴定至终点,消耗
NH4SCN标准溶液滴定至终点,消耗 标准液。[已知:
标准液。[已知: (白色)]
(白色)]①
 (摩尔质量为
(摩尔质量为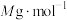 )的纯度为
)的纯度为②下列有关上述滴定操作的说法正确的是
a.接近滴定终点时微微转动活塞,使溶液悬挂在尖嘴上,形成半滴,用锥形瓶内壁将其刮落
b.若盛放NH4SCN标准溶液的滴定管没有润洗,使测定结果偏大
c.锥形瓶洗涤后未干燥即加入所配待测溶液,使测定结果偏小
d.滴定前俯视读数,滴定后仰视读数,使测定结果偏小
您最近一年使用:0次
名校
解题方法
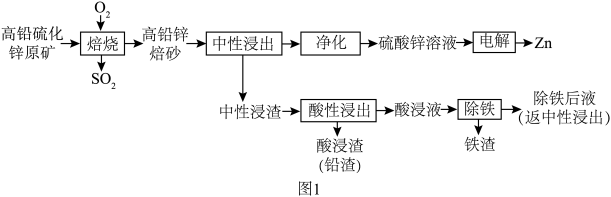
6 . 从高铅硫化锌原矿(主要成分为ZnS、PbS、FeS2、ZnCO3)中提取有价金属的工艺流程如图1所示。回答下列问题:___________ (填一条)。
(2)硫化锌的“焙烧”过程中,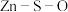 系在温度为1100K下的
系在温度为1100K下的 [
[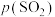 、
、 分别为平衡时两种物质的分压]的等温平衡状态图如图2所示。
分别为平衡时两种物质的分压]的等温平衡状态图如图2所示。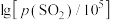 、
、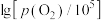 均为-5时,含锌产物为
均为-5时,含锌产物为___________ (填化学式)。
②一定条件下,焙烧过程中A点ZnS发生反应的化学方程式为___________ 。
③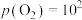 kPa时,若要使ZnSO4转化成更多的ZnO,需进行的操作为
kPa时,若要使ZnSO4转化成更多的ZnO,需进行的操作为___________ (填“降低SO2的分压”或“升高SO2的分压”)。
(3)“中性浸渣”中含有ZnO、PbO、Fe2O3。
①“酸性浸出”时加入的酸是___________ (填化学式,下同)。
②“除铁后液”的主要溶质为___________ 。
③“除铁”过程:先加入ZnS将Fe3+还原为Fe2+,再加入ZnO并通入O2,将其转化为FeOOH.若1 molFe2+转化为FeOOH,则在标准状况下消耗___________ LO2。
(4)“电解”时电极均为Pt极,则阳极反应式为___________ 。
(2)硫化锌的“焙烧”过程中,
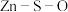 系在温度为1100K下的
系在温度为1100K下的 [
[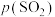 、
、 分别为平衡时两种物质的分压]的等温平衡状态图如图2所示。
分别为平衡时两种物质的分压]的等温平衡状态图如图2所示。 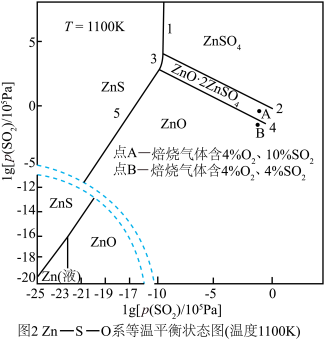
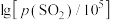 、
、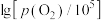 均为-5时,含锌产物为
均为-5时,含锌产物为②一定条件下,焙烧过程中A点ZnS发生反应的化学方程式为
③
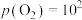 kPa时,若要使ZnSO4转化成更多的ZnO,需进行的操作为
kPa时,若要使ZnSO4转化成更多的ZnO,需进行的操作为(3)“中性浸渣”中含有ZnO、PbO、Fe2O3。
①“酸性浸出”时加入的酸是
②“除铁后液”的主要溶质为
③“除铁”过程:先加入ZnS将Fe3+还原为Fe2+,再加入ZnO并通入O2,将其转化为FeOOH.若1 molFe2+转化为FeOOH,则在标准状况下消耗
(4)“电解”时电极均为Pt极,则阳极反应式为
您最近一年使用:0次
7 . 钪在国防、航天、光电等多领域有重要应用。由钛白水解母液(含Sc3+,H+、Fe2+、Mn2+、 等)制备Sc2O3的工艺流程如下:
等)制备Sc2O3的工艺流程如下: 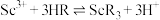 ,其中 HR表示 P204。
,其中 HR表示 P204。
下列说法错误的是
 等)制备Sc2O3的工艺流程如下:
等)制备Sc2O3的工艺流程如下: 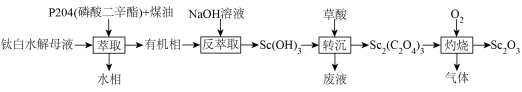
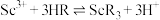 ,其中 HR表示 P204。
,其中 HR表示 P204。下列说法错误的是
A.分批加入萃取剂进行多次萃取可提高  的萃取率 的萃取率 |
B.水相中  的物质的量浓度小于钛白水解母液中的 的物质的量浓度小于钛白水解母液中的 |
C.同一温度下,由“转沉”原理可推知溶度积常数: 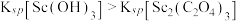 |
| D.“灼烧”反应生成1molSc2O3时,理论上有1.5molO2参加反应 |
您最近一年使用:0次
8 . 某化学兴趣小组利用KBr废液制备溴单质,其流程如图所示(“氧化1”时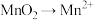 )。下列说法正确的是
)。下列说法正确的是
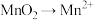 )。下列说法正确的是
)。下列说法正确的是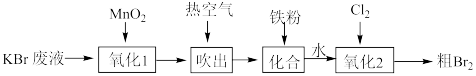
| A.“吹出”时涉及氧化还原反应 |
| B.可用乙醇从溴水中萃取溴 |
C.“氧化1”时若1 mol 发生反应,则转移4 mol电子 发生反应,则转移4 mol电子 |
D.“氧化2”时发生反应 |
您最近一年使用:0次
9 .  电化学循环氧化法将酸性废水中的苯酚降解为
电化学循环氧化法将酸性废水中的苯酚降解为 ,加入
,加入 可加快苯酚的降解,原理如图。已知:
可加快苯酚的降解,原理如图。已知: ,
, 有强氧化性。下列说法错误的是
有强氧化性。下列说法错误的是
 电化学循环氧化法将酸性废水中的苯酚降解为
电化学循环氧化法将酸性废水中的苯酚降解为 ,加入
,加入 可加快苯酚的降解,原理如图。已知:
可加快苯酚的降解,原理如图。已知: ,
, 有强氧化性。下列说法错误的是
有强氧化性。下列说法错误的是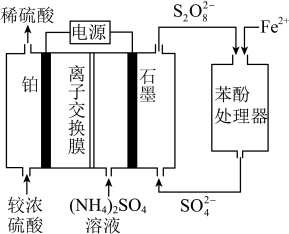
| A.铂连接电源负极,发生还原反应 |
B.石墨上的电极反应: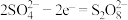 |
C.苯酚降解时发生反应: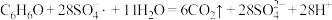 |
D.处理1mol苯酚,有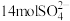 从左向右通过离子交换膜 从左向右通过离子交换膜 |
您最近一年使用:0次
2024-05-12更新
|
285次组卷
|
2卷引用:山东省德州市2024届高三下学期高考适应性练习(二)化学试题
10 . 采用选择性催化还原技术(SCR)可以有效脱除烟气中的氮氧化物( )。
)。
(1)钒基催化剂(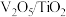 催化剂)可用于
催化剂)可用于 ,反应机理与催化剂表面
,反应机理与催化剂表面 的活性吸附位点有关。基于Lewis酸位点的SCR催化反应循环机理如图甲所示:
的活性吸附位点有关。基于Lewis酸位点的SCR催化反应循环机理如图甲所示: 的总反应化学方程式为
的总反应化学方程式为___________ ,该反应的中间体有___________ 种。
②若烟气中含有硫的氧化物,则会降低 的速率,可能的原因是
的速率,可能的原因是___________ 。
(2)研究发现:当烟气中 和
和 的物质的量相同时,会发生快速SCR反应过程:
的物质的量相同时,会发生快速SCR反应过程: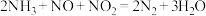 。臭氧对
。臭氧对 具有一定的辅助作用。臭氧先氧化
具有一定的辅助作用。臭氧先氧化 ,发生反应:
,发生反应: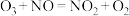 。在不同温度下,经过相同时间后测得
。在不同温度下,经过相同时间后测得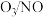 的物质的量之比与
的物质的量之比与 的脱除率关系如图乙所示。
的脱除率关系如图乙所示。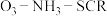 中
中 脱除率均有不同程度的降低,其原因是
脱除率均有不同程度的降低,其原因是___________ (写两条)。
②温度低于250℃,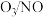 物质的量之比为0.5时,
物质的量之比为0.5时, 脱除率较高的原因是
脱除率较高的原因是___________ 。
③实验发现,向烟气中先通入 ,
, 脱除率低于先通入
脱除率低于先通入 ,可能的原因是
,可能的原因是___________
(3)以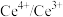 为媒介的间接电化学氧化法可以同时除去烟气中的
为媒介的间接电化学氧化法可以同时除去烟气中的 和
和 ,装置如图丙所示:
,装置如图丙所示:___________ , 参与反应的离子方程式为
参与反应的离子方程式为___________ 。
 )。
)。(1)钒基催化剂(
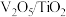 催化剂)可用于
催化剂)可用于 ,反应机理与催化剂表面
,反应机理与催化剂表面 的活性吸附位点有关。基于Lewis酸位点的SCR催化反应循环机理如图甲所示:
的活性吸附位点有关。基于Lewis酸位点的SCR催化反应循环机理如图甲所示: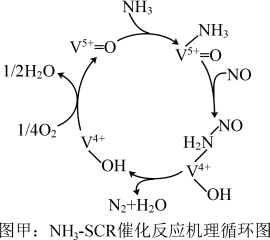
 的总反应化学方程式为
的总反应化学方程式为②若烟气中含有硫的氧化物,则会降低
 的速率,可能的原因是
的速率,可能的原因是(2)研究发现:当烟气中
 和
和 的物质的量相同时,会发生快速SCR反应过程:
的物质的量相同时,会发生快速SCR反应过程: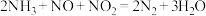 。臭氧对
。臭氧对 具有一定的辅助作用。臭氧先氧化
具有一定的辅助作用。臭氧先氧化 ,发生反应:
,发生反应: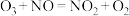 。在不同温度下,经过相同时间后测得
。在不同温度下,经过相同时间后测得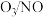 的物质的量之比与
的物质的量之比与 的脱除率关系如图乙所示。
的脱除率关系如图乙所示。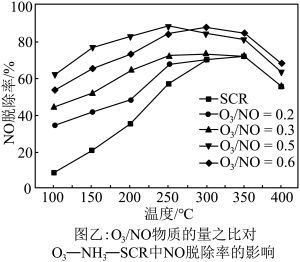
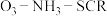 中
中 脱除率均有不同程度的降低,其原因是
脱除率均有不同程度的降低,其原因是②温度低于250℃,
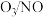 物质的量之比为0.5时,
物质的量之比为0.5时, 脱除率较高的原因是
脱除率较高的原因是③实验发现,向烟气中先通入
 ,
, 脱除率低于先通入
脱除率低于先通入 ,可能的原因是
,可能的原因是(3)以
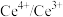 为媒介的间接电化学氧化法可以同时除去烟气中的
为媒介的间接电化学氧化法可以同时除去烟气中的 和
和 ,装置如图丙所示:
,装置如图丙所示: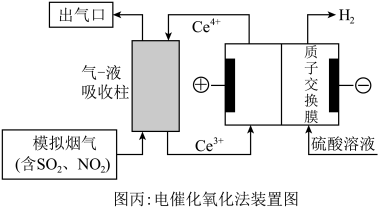
 参与反应的离子方程式为
参与反应的离子方程式为
您最近一年使用:0次



