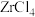名校
解题方法
1 . 某科研团队以溴苯与catB—Br的偶联联反应构建C-B键,反应机理如图,下列说法正确的是

| A.过程中Ni的化合价未发生改变 |
| B.L-Ni-Br为中间产物 |
| C.catB·为催化剂 |
D.理论上产生1mol  消耗Zn与溴苯的物质的量之比为1∶1 消耗Zn与溴苯的物质的量之比为1∶1 |
您最近一年使用:0次
名校
2 . 锆是一种稀有金属,广泛用在航空航天、军工、核反应、原子能领域。一种以锆英砂(主要含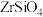 ,还含有少量Cr、Fe、Hf等元素)为原料生产金属锆和副产物硅酸钙的工艺流程如下:
,还含有少量Cr、Fe、Hf等元素)为原料生产金属锆和副产物硅酸钙的工艺流程如下: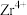 、
、 、
、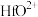 、
、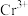 ;
;
②25℃时, ,
,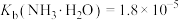 ;
;
③部分氯化物的沸点数据如表所示:
回答下列问题:
(1)“碱熔”时有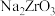 生成,则
生成,则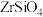 发生反应的化学方程式为
发生反应的化学方程式为______ ,温度和时间对锆英砂碱熔分解率的影响如图所示,应采取的条件为______ 。______ ,流程中可循环利用的物质除TOPO外,还有______ (填化学式)。
(3)“氨沉”时产物为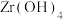 、
、 和
和 ,反应结束后溶液中
,反应结束后溶液中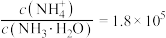 ,则
,则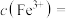
______  ,“滤液2”中主要成分是
,“滤液2”中主要成分是______ (填化学式)。
(4)“煅烧”时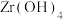 分解生成
分解生成 ,“沸腾氯化”时
,“沸腾氯化”时 发生反应的化学方程式为
发生反应的化学方程式为______ ,氯化反应结束通入 ,目的是
,目的是______ 。
 ,还含有少量Cr、Fe、Hf等元素)为原料生产金属锆和副产物硅酸钙的工艺流程如下:
,还含有少量Cr、Fe、Hf等元素)为原料生产金属锆和副产物硅酸钙的工艺流程如下: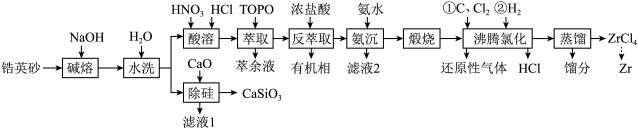
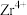 、
、 、
、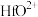 、
、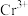 ;
;②25℃时,
 ,
,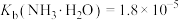 ;
;③部分氯化物的沸点数据如表所示:
物质 |
|
|
|
|
沸点/℃ | 331 | 1300 | 316 | 700 |
(1)“碱熔”时有
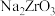 生成,则
生成,则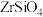 发生反应的化学方程式为
发生反应的化学方程式为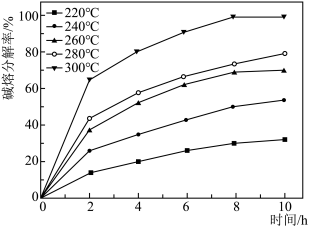
(3)“氨沉”时产物为
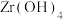 、
、 和
和 ,反应结束后溶液中
,反应结束后溶液中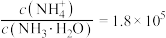 ,则
,则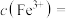
 ,“滤液2”中主要成分是
,“滤液2”中主要成分是(4)“煅烧”时
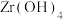 分解生成
分解生成 ,“沸腾氯化”时
,“沸腾氯化”时 发生反应的化学方程式为
发生反应的化学方程式为 ,目的是
,目的是
您最近一年使用:0次
2024-05-21更新
|
436次组卷
|
2卷引用:山东省潍坊市2024届高三下学期二模化学试题
解题方法
3 . 垃圾是放错位置的资源。从某废旧钾离子电池(主要含石墨、 、铝箔、醚类有机物等)回收部分有价金属的流程如图。
、铝箔、醚类有机物等)回收部分有价金属的流程如图。 中
中 为+3价;
为+3价;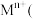 水相
水相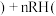 有机相
有机相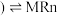 (有机相
(有机相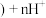 (水相
(水相 。
。
回答下列问题:
(1)为符合“双碳”战略,将“焙烧”后的气体 通入“滤液Ⅰ”至过量,除
通入“滤液Ⅰ”至过量,除 外,还可获得的副产品有
外,还可获得的副产品有______ (填化学式)。
(2)“酸溶”时主要反应的离子方程式为______ 。“酸溶”时不能用 替代双氧水,原因是
替代双氧水,原因是______ 。
(3)“萃取”过程萃取剂与溶液的体积比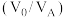 对溶液中金属元素的萃取率影响如图2所示。则
对溶液中金属元素的萃取率影响如图2所示。则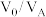 最佳取值为
最佳取值为______ ;“反萃取”时应选择的试剂为______ (填化学式)。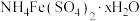 中
中 测定。方法一:称取一定质量晶体加水溶解后,加入足量
测定。方法一:称取一定质量晶体加水溶解后,加入足量 溶液并加热,产生气体全部被一定量的
溶液并加热,产生气体全部被一定量的 吸收,反应结束后,加入指示剂
吸收,反应结束后,加入指示剂______ (填“甲基橙”、“酚酸”或“石蕊”),再用 标准溶液滴定剩余
标准溶液滴定剩余 。方法二:称取一定质量晶体,加水溶解并加入过量的
。方法二:称取一定质量晶体,加水溶解并加入过量的 溶液,沉淀经过滤、水洗、醇洗、烘干、称重。若烘干不彻底,导致
溶液,沉淀经过滤、水洗、醇洗、烘干、称重。若烘干不彻底,导致 测量结果
测量结果______ (填“偏高”、“偏低”或“不影响”);方法三:采用热重分析法测定时,当样品加热到150℃时,失掉1.5个结晶水,失重 ,则
,则
______ 。
 、铝箔、醚类有机物等)回收部分有价金属的流程如图。
、铝箔、醚类有机物等)回收部分有价金属的流程如图。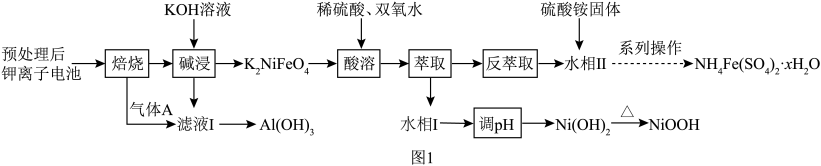
 中
中 为+3价;
为+3价;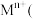 水相
水相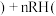 有机相
有机相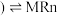 (有机相
(有机相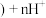 (水相
(水相 。
。回答下列问题:
(1)为符合“双碳”战略,将“焙烧”后的气体
 通入“滤液Ⅰ”至过量,除
通入“滤液Ⅰ”至过量,除 外,还可获得的副产品有
外,还可获得的副产品有(2)“酸溶”时主要反应的离子方程式为
 替代双氧水,原因是
替代双氧水,原因是(3)“萃取”过程萃取剂与溶液的体积比
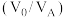 对溶液中金属元素的萃取率影响如图2所示。则
对溶液中金属元素的萃取率影响如图2所示。则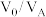 最佳取值为
最佳取值为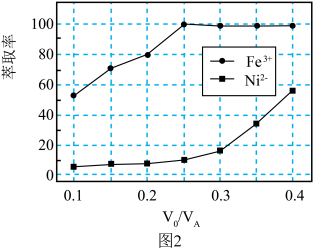
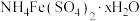 中
中 测定。方法一:称取一定质量晶体加水溶解后,加入足量
测定。方法一:称取一定质量晶体加水溶解后,加入足量 溶液并加热,产生气体全部被一定量的
溶液并加热,产生气体全部被一定量的 吸收,反应结束后,加入指示剂
吸收,反应结束后,加入指示剂 标准溶液滴定剩余
标准溶液滴定剩余 。方法二:称取一定质量晶体,加水溶解并加入过量的
。方法二:称取一定质量晶体,加水溶解并加入过量的 溶液,沉淀经过滤、水洗、醇洗、烘干、称重。若烘干不彻底,导致
溶液,沉淀经过滤、水洗、醇洗、烘干、称重。若烘干不彻底,导致 测量结果
测量结果 ,则
,则
您最近一年使用:0次
名校
4 . 含钴废渣中主要含有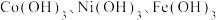 以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:
以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:
(1)“酸浸”过程中, 发生反应的离子方程式为
发生反应的离子方程式为_____________ 。
(2)“除铁”过程中加入 的作用是
的作用是_____________ 。
(3)“除杂”的目的是_____________ 。
(4)“沉钴”后需将沉淀洗净,检验沉淀已洗净的方法是_____________ 。“沉钴”所得固体经过滤、洗涤、干燥,得到纯度80%的 晶体。称取
晶体。称取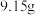 该晶体,在空气中加热一段时间后(杂质变为气态),得到
该晶体,在空气中加热一段时间后(杂质变为气态),得到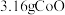 和
和 的混合物。该混合物中
的混合物。该混合物中 和
和 的质量之比
的质量之比_____________ 。
(5)“萃取”“反萃取”的目的是_____________ ;有机萃取剂与溶液的体积比 对溶液中
对溶液中 萃取率影响如图,则
萃取率影响如图,则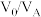 的最佳取值为
的最佳取值为_____________ 。
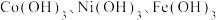 以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下:
以及少量的钙、镁等杂质。一种提取钴氧化物的工艺流程如下: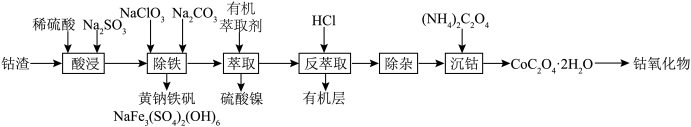
(1)“酸浸”过程中,
 发生反应的离子方程式为
发生反应的离子方程式为(2)“除铁”过程中加入
 的作用是
的作用是(3)“除杂”的目的是
(4)“沉钴”后需将沉淀洗净,检验沉淀已洗净的方法是
 晶体。称取
晶体。称取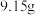 该晶体,在空气中加热一段时间后(杂质变为气态),得到
该晶体,在空气中加热一段时间后(杂质变为气态),得到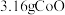 和
和 的混合物。该混合物中
的混合物。该混合物中 和
和 的质量之比
的质量之比(5)“萃取”“反萃取”的目的是
 对溶液中
对溶液中 萃取率影响如图,则
萃取率影响如图,则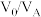 的最佳取值为
的最佳取值为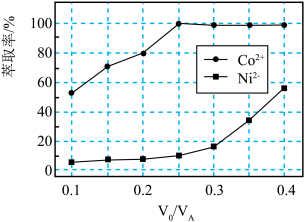
您最近一年使用:0次
2024-05-21更新
|
132次组卷
|
2卷引用:2024届山东省高三下学期联合模拟考试模拟预测化学试题
解题方法
5 . 一种利用湿法炼锌净化渣回收钴并制备碱式碳酸锌的工艺如下图所示,已知净化渣含有较多的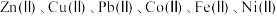 的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为
的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为 价)。
价)。 。
。
(1)浸出渣主要成分为_______ 。
(2)大多数金属硫化物都难溶于水,选择 除铜的原因是
除铜的原因是_______ ,若加入 后溶液中
后溶液中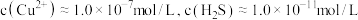 ,则溶液的
,则溶液的 约为
约为_______ 。
(3)研究加入 后温度和时间对金属脱除率的影响,所得曲线如下图所示。
后温度和时间对金属脱除率的影响,所得曲线如下图所示。_______ , 滤渣中还含有
滤渣中还含有_______ 。
(4)在适宜的条件下,加入 并调节溶液
并调节溶液 至
至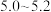 ,反应生成
,反应生成 的离子方程式为
的离子方程式为_______ 。以 湿法炼锌净化渣(
湿法炼锌净化渣( 的质量分数为
的质量分数为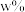 )为原料提取出
)为原料提取出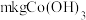 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为_______  (填含
(填含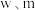 的表达式)。
的表达式)。
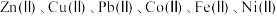 的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为
的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为 价)。
价)。
 。
。(1)浸出渣主要成分为
(2)大多数金属硫化物都难溶于水,选择
 除铜的原因是
除铜的原因是 后溶液中
后溶液中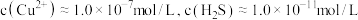 ,则溶液的
,则溶液的 约为
约为(3)研究加入
 后温度和时间对金属脱除率的影响,所得曲线如下图所示。
后温度和时间对金属脱除率的影响,所得曲线如下图所示。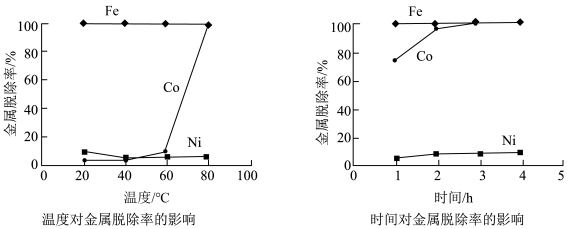
 滤渣中还含有
滤渣中还含有(4)在适宜的条件下,加入
 并调节溶液
并调节溶液 至
至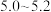 ,反应生成
,反应生成 的离子方程式为
的离子方程式为 湿法炼锌净化渣(
湿法炼锌净化渣( 的质量分数为
的质量分数为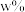 )为原料提取出
)为原料提取出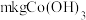 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为 (填含
(填含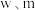 的表达式)。
的表达式)。
您最近一年使用:0次
名校
6 . 某铜冶炼厂烟气净化工序含砷废水中主要含有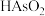 和硫酸及少量
和硫酸及少量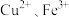 等,以其为原料制备
等,以其为原料制备 的工艺流程如图:
的工艺流程如图: 范围:
范围:
下列说法错误的是
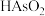 和硫酸及少量
和硫酸及少量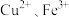 等,以其为原料制备
等,以其为原料制备 的工艺流程如图:
的工艺流程如图: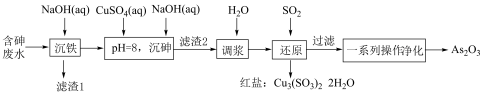
 范围:
范围:金属离子 |
|
|
开始沉淀的 | 1.5 | 4.7 |
沉淀完全的 | 3.7 | 6.6 |
A.“沉铁”调 的范围是 的范围是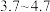 |
B.“滤渣2”成分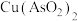 和 和 |
C.“还原”过程中生成红盐的化学方程式: |
| D.“一系列操作”仅涉及物理变化 |
您最近一年使用:0次
2024-05-21更新
|
121次组卷
|
2卷引用:2024届山东省高三下学期联合模拟考试模拟预测化学试题
解题方法
7 . 部分含氮物质的分类与相应化合物关系如图所示。下列说法错误的是

| A.b具有碱性和还原性 |
| B.反应Ⅰ中氧化产物和还原产物的物质的量之比为1∶1 |
C.反应Ⅱ过程中生成0.1mol  时,转移1mol电子 时,转移1mol电子 |
| D.反应Ⅲ能有效降低水体中的氮元素含量 |
您最近一年使用:0次
8 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是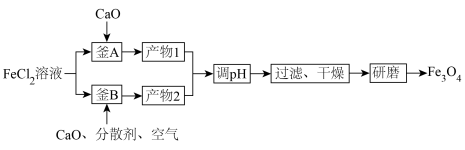
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为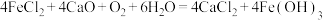 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近一年使用:0次
9 . 氧钒碱式碳酸铵晶体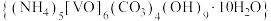 ,紫红色,难溶于水和乙醇。其制备及氮元素含量的测定实验如下(已知
,紫红色,难溶于水和乙醇。其制备及氮元素含量的测定实验如下(已知 易被
易被 氧化)。回答下列问题。
氧化)。回答下列问题。
Ⅰ.制备
步骤1:向 中加入足量盐酸酸化的
中加入足量盐酸酸化的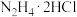 溶液,微沸数分钟。
溶液,微沸数分钟。
步骤2:向足量 溶液中缓慢加入制得的
溶液中缓慢加入制得的 溶液,有气泡产生并析出紫红色晶体。
溶液,有气泡产生并析出紫红色晶体。
步骤3:反应结束后抽滤,先后用饱和 溶液、无水乙醇洗涤,静置得产品。
溶液、无水乙醇洗涤,静置得产品。
(1)“步骤1”产生无色无污染的气体,该反应的化学方程式为______ 。
(2)用无水乙醇洗涤的目的是______ 。
(3)“步骤2”可在如图装置中进行。______ 。(按气流方向,用字母标号表示)。
②检查装置气密性,加入试剂。先打开 ,通入一段时间气体目的是
,通入一段时间气体目的是______ ,当观察到______ (填实验现象)时,再关闭 ,打开
,打开 ,进行实验。
,进行实验。
③生成氧钒碱式碳酸铵晶体的化学方程式为______ 。
Ⅱ.产品中氮元素含量的测定
精确称取wg晶体加入如图所示的三颈烧瓶中,然后逐滴加入足量10%NaOH溶液充分反应,通入水蒸气,将氨全部蒸出,并用蒸馏水冲洗导管内壁,用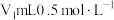 的饱和硼酸标准溶液完全吸收。取下接收瓶,用0.5
的饱和硼酸标准溶液完全吸收。取下接收瓶,用0.5 盐酸标准溶液滴定,到终点时消耗
盐酸标准溶液滴定,到终点时消耗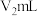 盐酸。
盐酸。
已知: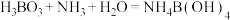 ,
, 。
。
(4)“冰盐水”的作用是______ 。
(5)样品中氮元素质量分数的表达式为______ 。
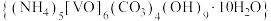 ,紫红色,难溶于水和乙醇。其制备及氮元素含量的测定实验如下(已知
,紫红色,难溶于水和乙醇。其制备及氮元素含量的测定实验如下(已知 易被
易被 氧化)。回答下列问题。
氧化)。回答下列问题。Ⅰ.制备
步骤1:向
 中加入足量盐酸酸化的
中加入足量盐酸酸化的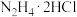 溶液,微沸数分钟。
溶液,微沸数分钟。步骤2:向足量
 溶液中缓慢加入制得的
溶液中缓慢加入制得的 溶液,有气泡产生并析出紫红色晶体。
溶液,有气泡产生并析出紫红色晶体。步骤3:反应结束后抽滤,先后用饱和
 溶液、无水乙醇洗涤,静置得产品。
溶液、无水乙醇洗涤,静置得产品。(1)“步骤1”产生无色无污染的气体,该反应的化学方程式为
(2)用无水乙醇洗涤的目的是
(3)“步骤2”可在如图装置中进行。
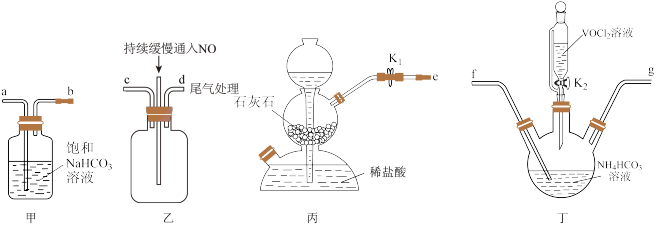
②检查装置气密性,加入试剂。先打开
 ,通入一段时间气体目的是
,通入一段时间气体目的是 ,打开
,打开 ,进行实验。
,进行实验。③生成氧钒碱式碳酸铵晶体的化学方程式为
Ⅱ.产品中氮元素含量的测定
精确称取wg晶体加入如图所示的三颈烧瓶中,然后逐滴加入足量10%NaOH溶液充分反应,通入水蒸气,将氨全部蒸出,并用蒸馏水冲洗导管内壁,用
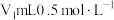 的饱和硼酸标准溶液完全吸收。取下接收瓶,用0.5
的饱和硼酸标准溶液完全吸收。取下接收瓶,用0.5 盐酸标准溶液滴定,到终点时消耗
盐酸标准溶液滴定,到终点时消耗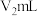 盐酸。
盐酸。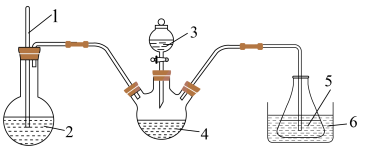
已知:
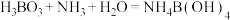 ,
, 。
。(4)“冰盐水”的作用是
(5)样品中氮元素质量分数的表达式为
您最近一年使用:0次
解题方法
10 . Co、La元素及其化合物在工业及生活方面有重要应用。回答下列问题:
(1)基态Co的价电子排布图_______ ,核外电子的空间运动状态有_______ 种。
(2)一定条件下, 、
、 、
、 和
和 反应可制得
反应可制得 ,反应的方程式为
,反应的方程式为_______ , 的配位数为
的配位数为_______ 。区别 和
和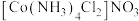 两种溶液的试剂是
两种溶液的试剂是_______ 。
(3) 的八配位金属羰基化合物
的八配位金属羰基化合物 的结构如图所示,
的结构如图所示, 作配体,配位原子为C,而不是O,其原因是
作配体,配位原子为C,而不是O,其原因是_______ ,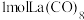 含
含_______  键。
键。 在储氢和超导等领域具有重要应用。高压下,
在储氢和超导等领域具有重要应用。高压下, 中的每个
中的每个 结合4个
结合4个 形成类似
形成类似 的结构独立存在,即得到晶体
的结构独立存在,即得到晶体 。则
。则
_______ 。晶体 的密度为
的密度为_______  。(写出计算式即可)
。(写出计算式即可)
(1)基态Co的价电子排布图
(2)一定条件下,
 、
、 、
、 和
和 反应可制得
反应可制得 ,反应的方程式为
,反应的方程式为 的配位数为
的配位数为 和
和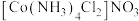 两种溶液的试剂是
两种溶液的试剂是(3)
 的八配位金属羰基化合物
的八配位金属羰基化合物 的结构如图所示,
的结构如图所示, 作配体,配位原子为C,而不是O,其原因是
作配体,配位原子为C,而不是O,其原因是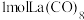 含
含 键。
键。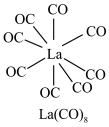
 在储氢和超导等领域具有重要应用。高压下,
在储氢和超导等领域具有重要应用。高压下, 中的每个
中的每个 结合4个
结合4个 形成类似
形成类似 的结构独立存在,即得到晶体
的结构独立存在,即得到晶体 。则
。则
 的密度为
的密度为 。(写出计算式即可)
。(写出计算式即可)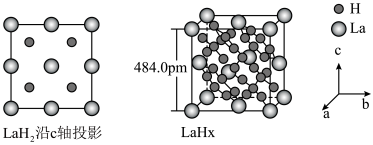
您最近一年使用:0次