1 . 卤素单质及化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)日前,日本悍然将含有 、
、 等多种放射性核素的核污染水排入大海,对海洋生态造成极大危害。
等多种放射性核素的核污染水排入大海,对海洋生态造成极大危害。
① 与
与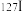 互称为
互称为___________ ,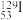 原子中含有中子数为
原子中含有中子数为___________ 。
② 常用作食盐中的补碘剂,其化学名称是
常用作食盐中的补碘剂,其化学名称是___________ 。
(2)①液溴极易挥发,实验室保存时为防止其挥发,通常会加入___________ 液封(填字母)。
a.水 b.煤油 c.
②海水提取溴时,常利用热空气将溴吹入 溶液,已知反应生成了两种盐,其中一种为
溶液,已知反应生成了两种盐,其中一种为 。写出
。写出 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(3) 是现今最常用的自来水消毒剂,可利用反应
是现今最常用的自来水消毒剂,可利用反应 制备,该反应中氧化剂与还原剂的物质的量之比为
制备,该反应中氧化剂与还原剂的物质的量之比为___________ ,每生成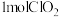 转移的电子数为
转移的电子数为___________ 。
(4)①氟气具有极强的氧化性,可与所有金属反应,但在室温下与铁、铜等块状金属反应却并不明显,可能的原因是___________ 。
②-40℃时, 与冰反应生成HFO和HF,HFO的电子式是
与冰反应生成HFO和HF,HFO的电子式是___________ ,请写出HFO与水发生反应生成两种化合物的化学方程式___________ 。
(1)日前,日本悍然将含有
 、
、 等多种放射性核素的核污染水排入大海,对海洋生态造成极大危害。
等多种放射性核素的核污染水排入大海,对海洋生态造成极大危害。①
 与
与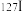 互称为
互称为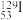 原子中含有中子数为
原子中含有中子数为②
 常用作食盐中的补碘剂,其化学名称是
常用作食盐中的补碘剂,其化学名称是(2)①液溴极易挥发,实验室保存时为防止其挥发,通常会加入
a.水 b.煤油 c.

②海水提取溴时,常利用热空气将溴吹入
 溶液,已知反应生成了两种盐,其中一种为
溶液,已知反应生成了两种盐,其中一种为 。写出
。写出 与
与 反应的离子方程式:
反应的离子方程式:(3)
 是现今最常用的自来水消毒剂,可利用反应
是现今最常用的自来水消毒剂,可利用反应 制备,该反应中氧化剂与还原剂的物质的量之比为
制备,该反应中氧化剂与还原剂的物质的量之比为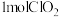 转移的电子数为
转移的电子数为(4)①氟气具有极强的氧化性,可与所有金属反应,但在室温下与铁、铜等块状金属反应却并不明显,可能的原因是
②-40℃时,
 与冰反应生成HFO和HF,HFO的电子式是
与冰反应生成HFO和HF,HFO的电子式是
您最近一年使用:0次
名校
2 . 酸性溶液中几种离子存在如图转化关系,下列说法正确的是


A. 在反应Ⅰ中体现还原性,在反应Ⅱ中体现氧化性 在反应Ⅰ中体现还原性,在反应Ⅱ中体现氧化性 |
B.各微粒还原性强弱: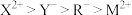 |
C.可推测反应 无法进行 无法进行 |
D.某溶液含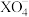 、 、 、 、 各1 各1 ,与足量含 ,与足量含 的溶液充分反应,最多生成3.5 的溶液充分反应,最多生成3.5  |
您最近一年使用:0次
2023-11-18更新
|
219次组卷
|
3卷引用:四川省泸州市泸县第五中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
3 . MgSO4·7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO4·7H2O的主要流程如下:

已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)“操作a”的名称是___________ 。
(2)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价是___________ 。
(3)MgCO3溶于稀硫酸的化学方程式为___________ 。
(4)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为___________ 。
(5)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是___________ 。

已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)“操作a”的名称是
(2)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价是
(3)MgCO3溶于稀硫酸的化学方程式为
(4)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为
(5)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是
您最近一年使用:0次
2023-11-14更新
|
160次组卷
|
2卷引用:四川省遂宁市射洪中学校2023-2024学年高一上学期10月月考化学试题
名校
4 . 某含铬废水中含有一定浓度的 ,同时还含有少量的
,同时还含有少量的 杂质,某研究小组为消除废水污染同时获得
杂质,某研究小组为消除废水污染同时获得 (铬绿),设计如下流程:
(铬绿),设计如下流程:

已知:在酸性环境中 的氧化性强于
的氧化性强于 。
。
(1)“滤渣”的主要成分为___________ (写化学式)。
(2)已知“酸化”调节pH时, 转化为
转化为 。
。
①下列溶液中可以代替“还原”过程中 溶液的是
溶液的是___________ (填标号)。
A.淀粉水解液 B.浓硫酸 C. 溶液 D.
溶液 D. 溶液
溶液
②“还原”步骤中,先加入硫酸酸化,再加入 溶液。若不加
溶液。若不加 酸化,可能造成的后果是
酸化,可能造成的后果是___________ ;若每消耗0.1mol  转移0.4mol
转移0.4mol  ,则加入
,则加入 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
(3)已知室温条件下,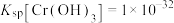 。若“沉铬”后滤液中
。若“沉铬”后滤液中 恰好完全沉淀[
恰好完全沉淀[
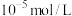 ],则此时溶液的pH=
],则此时溶液的pH=___________ 。
(4)“沉铬”过程所用浓氨水也可换用浓碳酸钠溶液,此时除得到 外,还会有大量气泡生成,试写出反应的离子方程式:
外,还会有大量气泡生成,试写出反应的离子方程式:___________ 。
(5)“滤液”中的 也可利用电解法直接被还原为
也可利用电解法直接被还原为 ,装置如图所示。则该装置的阳极区产生的离子与
,装置如图所示。则该装置的阳极区产生的离子与 反应的离子方程式为
反应的离子方程式为___________ 。

 ,同时还含有少量的
,同时还含有少量的 杂质,某研究小组为消除废水污染同时获得
杂质,某研究小组为消除废水污染同时获得 (铬绿),设计如下流程:
(铬绿),设计如下流程:
已知:在酸性环境中
 的氧化性强于
的氧化性强于 。
。(1)“滤渣”的主要成分为
(2)已知“酸化”调节pH时,
 转化为
转化为 。
。①下列溶液中可以代替“还原”过程中
 溶液的是
溶液的是A.淀粉水解液 B.浓硫酸 C.
 溶液 D.
溶液 D. 溶液
溶液②“还原”步骤中,先加入硫酸酸化,再加入
 溶液。若不加
溶液。若不加 酸化,可能造成的后果是
酸化,可能造成的后果是 转移0.4mol
转移0.4mol  ,则加入
,则加入 时发生反应的离子方程式为
时发生反应的离子方程式为(3)已知室温条件下,
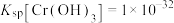 。若“沉铬”后滤液中
。若“沉铬”后滤液中 恰好完全沉淀[
恰好完全沉淀[
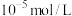 ],则此时溶液的pH=
],则此时溶液的pH=(4)“沉铬”过程所用浓氨水也可换用浓碳酸钠溶液,此时除得到
 外,还会有大量气泡生成,试写出反应的离子方程式:
外,还会有大量气泡生成,试写出反应的离子方程式:(5)“滤液”中的
 也可利用电解法直接被还原为
也可利用电解法直接被还原为 ,装置如图所示。则该装置的阳极区产生的离子与
,装置如图所示。则该装置的阳极区产生的离子与 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
2023-11-08更新
|
256次组卷
|
3卷引用:四川省南充市白塔中学2023-2024学年高三上学期第五次考试理科综合试题
解题方法
5 . 草酸钴可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、Al2O3、Fe、SiO2等)制备草酸钴晶体(CoC2O4·2H2O)的流程如下:

已知:①草酸钴晶体难溶于水。
②RH为有机物(难电离)、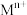 代表金属离子,
代表金属离子, 。
。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
④滤液中Co元素以Co2+形式存在。
回答下列问题:
(1)为提高浸出速率,除将含钴废料粉碎外,还可采取的措施有___________ (写出两条)。
(2)“浸出液”中加入H2O2后发生反应的离子方程式为___________ 。
(3)加入氧化钴调节溶液的pH,调节的pH范围是___________ 。
(4)操作①在实验室所用的主要仪器为___________ 。
(5)可向操作①后溶有 的有机层中加入
的有机层中加入___________ 使 从有机相返回水相,实现金属回收利用,另外也可使
从有机相返回水相,实现金属回收利用,另外也可使___________ 循环使用。
(6)可否考虑先将 转化为
转化为 ,再利用反应
,再利用反应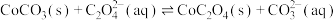 ,将
,将 转化为
转化为 :
:___________ (填“能”或“不能”),说明理由:___________ 。[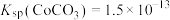 ,
, ]
]

已知:①草酸钴晶体难溶于水。
②RH为有机物(难电离)、
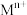 代表金属离子,
代表金属离子, 。
。③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |  |  |  |  |  |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.5 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 8.0 |
回答下列问题:
(1)为提高浸出速率,除将含钴废料粉碎外,还可采取的措施有
(2)“浸出液”中加入H2O2后发生反应的离子方程式为
(3)加入氧化钴调节溶液的pH,调节的pH范围是
(4)操作①在实验室所用的主要仪器为
(5)可向操作①后溶有
 的有机层中加入
的有机层中加入 从有机相返回水相,实现金属回收利用,另外也可使
从有机相返回水相,实现金属回收利用,另外也可使(6)可否考虑先将
 转化为
转化为 ,再利用反应
,再利用反应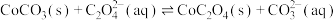 ,将
,将 转化为
转化为 :
: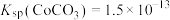 ,
, ]
]
您最近一年使用:0次
2023-11-08更新
|
792次组卷
|
4卷引用:工业流程题
6 . 以 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
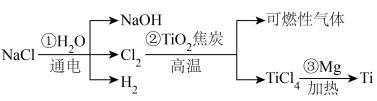
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为___________ 。
(2) 在
在 中燃烧的现象是
中燃烧的现象是___________ ,恰好完全反应后,将产物溶于水制得密度为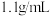 ,质量分数为
,质量分数为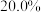 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为___________ 。
(3)步骤②发生反应的化学方程式为___________ ,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是___________ 。
 为原料制备
为原料制备 和
和 ,并利用
,并利用 冶炼金属钛(Ti)的工艺流程如下:
冶炼金属钛(Ti)的工艺流程如下:
已知:高温条件下Ti的性质很活泼。
回答下列问题:
(1)在实际生产中,应避免步骤①的产物
 与
与 接触发生副反应,降低
接触发生副反应,降低 纯度,解释其原因,用离子方程式表示为
纯度,解释其原因,用离子方程式表示为(2)
 在
在 中燃烧的现象是
中燃烧的现象是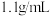 ,质量分数为
,质量分数为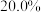 的盐酸溶液,其物质的量浓度为
的盐酸溶液,其物质的量浓度为(3)步骤②发生反应的化学方程式为
(4)步骤③须在稀有气体(如氩)的氛围下进行,稀有气体的作用是
您最近一年使用:0次
7 . 利用所学化学知识回答下列问题。
(1) 、
、 和
和 是钠的化合物,其中可以作为调味品主要成分的是
是钠的化合物,其中可以作为调味品主要成分的是___________ (填化学式), 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(2)可用___________ (填试剂,下同)除去 中混有的
中混有的 ,可用
,可用___________ 除去 溶液中混有的
溶液中混有的 。
。
(3)可用于区别 和
和 的试剂是
的试剂是______ ,发生反应的离子方程式为_______ 。
(4)工业上常用绿矾( )处理废水中含有的重铬酸根离子(
)处理废水中含有的重铬酸根离子( ),该反应的离子方程式为:______
),该反应的离子方程式为:______ ______
______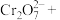 ______
______ ______
______ _____
_____ _____
_____ ,从酸、碱、盐及混合物的角度分类,绿矾属于
,从酸、碱、盐及混合物的角度分类,绿矾属于___________ 。配平以上离子方程式,并用双线桥标出该反应电子转移的情况___________ ,其中还原剂是___________ (填离子符号),每处理 ,转移电子的物质的量为
,转移电子的物质的量为___________ 。
(1)
 、
、 和
和 是钠的化合物,其中可以作为调味品主要成分的是
是钠的化合物,其中可以作为调味品主要成分的是 与
与 反应的化学方程式为
反应的化学方程式为(2)可用
 中混有的
中混有的 ,可用
,可用 溶液中混有的
溶液中混有的 。
。(3)可用于区别
 和
和 的试剂是
的试剂是(4)工业上常用绿矾(
 )处理废水中含有的重铬酸根离子(
)处理废水中含有的重铬酸根离子( ),该反应的离子方程式为:______
),该反应的离子方程式为:______ ______
______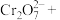 ______
______ ______
______ _____
_____ _____
_____ ,从酸、碱、盐及混合物的角度分类,绿矾属于
,从酸、碱、盐及混合物的角度分类,绿矾属于 ,转移电子的物质的量为
,转移电子的物质的量为
您最近一年使用:0次
8 . 下列说法错误的是
| A.维生素C可用作抗氧化剂是由于其难以被氧化 |
B. 溶液与 溶液与 溶液混合不能发生离子反应 溶液混合不能发生离子反应 |
C.反应 的发生说明 的发生说明 的氧化性强于 的氧化性强于 |
D. 溶于稀硝酸的离子方程式为 溶于稀硝酸的离子方程式为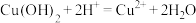 |
您最近一年使用:0次
解题方法
9 . 研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)在酸性条件下,可发生反应: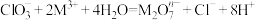 ,在该过程中
,在该过程中 被
被______ (填“氧化”或“还原”),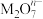 中M的化合价是
中M的化合价是______ 价。
(2)卫星发射时以N2H4(联氨)和N2O4为火箭的动力源,二者发生的反应为: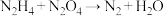 ,反应温度高达2700℃,回答下列问题。
,反应温度高达2700℃,回答下列问题。
①配平方程式:____________
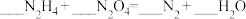
②氧化产物与还原产物的质量之比为______ 。
③用双线桥标出该反应电子转移的方向和数目_____ 。
(3)某同学设计如下实验研究H2O2的性质:
①从理论上分析H2O2具有还原性的原因____________________ 。
②能证明H2O2具有氧化性的实验是______ (填序号),写出该实验过程中发生反应的离子方程式____________________ 。
(1)在酸性条件下,可发生反应:
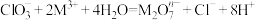 ,在该过程中
,在该过程中 被
被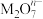 中M的化合价是
中M的化合价是(2)卫星发射时以N2H4(联氨)和N2O4为火箭的动力源,二者发生的反应为:
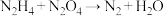 ,反应温度高达2700℃,回答下列问题。
,反应温度高达2700℃,回答下列问题。①配平方程式:
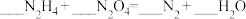
②氧化产物与还原产物的质量之比为
③用双线桥标出该反应电子转移的方向和数目
(3)某同学设计如下实验研究H2O2的性质:
序号 | 实验 | 实验现象 |
Ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
Ⅱ | 向5%H2O2酸性溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
②能证明H2O2具有氧化性的实验是
您最近一年使用:0次
10 . 电解锌的生产过程中产生大量富钴渣,主要含金属Zn、Cd及CoO、MnO和FeO。采用以下工艺可利用富钴渣生产高纯锌:

回答下列问题:
(1)在“溶浸”中,需搅拌并控制温度85℃,其目的是________ 。
(2)加入H2O2后生成FeOOH的化学方程式为________ 。
(3)“滤液①”中含有的金属离子有Cd2+、Co2+、________ 。
(4)“除锰钴”中,生成MnO2的离子方程式为________ 。
(5)还原除杂的“滤渣”主要成分是________ 。
(6)“电解”可通过如图装置实现。电解时,钛合金上的电极反应式为________ 。电解后,不锈钢区域的NaOH溶液浓度________ (填“增大”“减小”或“不变”)。


回答下列问题:
(1)在“溶浸”中,需搅拌并控制温度85℃,其目的是
(2)加入H2O2后生成FeOOH的化学方程式为
(3)“滤液①”中含有的金属离子有Cd2+、Co2+、
(4)“除锰钴”中,生成MnO2的离子方程式为
(5)还原除杂的“滤渣”主要成分是
(6)“电解”可通过如图装置实现。电解时,钛合金上的电极反应式为

您最近一年使用:0次



