1 . 捕集并转化CO2可以有效实现碳达峰、碳中和。
Ⅰ.工业上利用两种温室气体CH4和CO2催化重整制取H2和CO,主要反应为:
反应①:
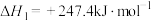
过程中还发生三个副反应:
反应②:

反应③: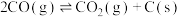
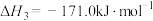
反应④: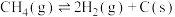 △H4
△H4
将CH4与CO2(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中H2与CO的物质的量之比、CO2的转化率与温度的关系如图所示:
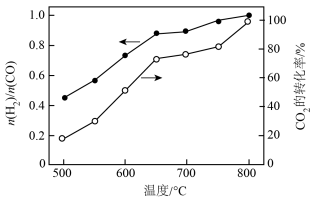
(1)△H4=___________ kJ·mol-1。
(2)500℃时, 比较小,此时发生的副反应以
比较小,此时发生的副反应以___________ (选填②、③、④中一种)为主。升高温度,产物中H2与CO的物质的量之比增大的原因是___________ 。
Ⅱ.光催化CH4和CO2生成CO和H2催化反应机理如图所示:
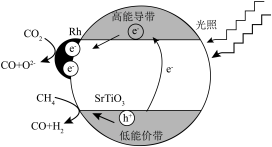
(3)上述反应机理中表现出氧化性的粒子有___________ 。
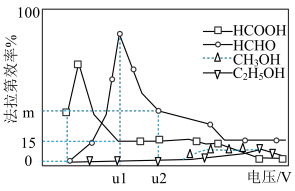
Ⅲ.用光电化学法将CO2还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:
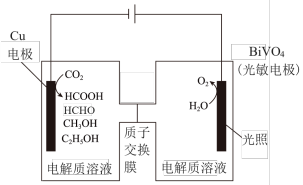
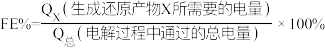 ,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
(4)当电解电压为u1V时,阴极生成HCHO的电极反应式为___________ 。
(5)当电解电压为u2V时,电解生成的HCOOH和HCHO的物质的量之比为5:6,生成HCHO的法拉第效率m为___________ 。
Ⅰ.工业上利用两种温室气体CH4和CO2催化重整制取H2和CO,主要反应为:
反应①:

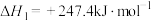
过程中还发生三个副反应:
反应②:


反应③:
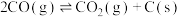
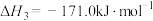
反应④:
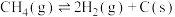 △H4
△H4将CH4与CO2(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中H2与CO的物质的量之比、CO2的转化率与温度的关系如图所示:

(1)△H4=
(2)500℃时,
 比较小,此时发生的副反应以
比较小,此时发生的副反应以Ⅱ.光催化CH4和CO2生成CO和H2催化反应机理如图所示:

(3)上述反应机理中表现出氧化性的粒子有
Ⅲ.用光电化学法将CO2还原为有机物实现碳资源的再生利用,其装置如左图所示,其他条件一定时,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如右图所示:


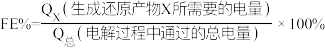 ,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,其中,Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。(4)当电解电压为u1V时,阴极生成HCHO的电极反应式为
(5)当电解电压为u2V时,电解生成的HCOOH和HCHO的物质的量之比为5:6,生成HCHO的法拉第效率m为
您最近半年使用:0次
名校
解题方法
2 . 丙烷经催化脱氢可制丙烯: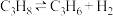 。600℃,将一定浓度的
。600℃,将一定浓度的 与固定浓度的
与固定浓度的 通过含催化剂的恒容反应器,经相同时间,流出的
通过含催化剂的恒容反应器,经相同时间,流出的 、
、 和
和 浓度随初始
浓度随初始 浓度的变化关系如图。
浓度的变化关系如图。

已知:①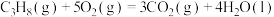
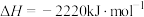
②
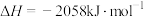
③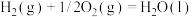
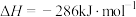
下列说法不正确的是
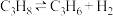 。600℃,将一定浓度的
。600℃,将一定浓度的 与固定浓度的
与固定浓度的 通过含催化剂的恒容反应器,经相同时间,流出的
通过含催化剂的恒容反应器,经相同时间,流出的 、
、 和
和 浓度随初始
浓度随初始 浓度的变化关系如图。
浓度的变化关系如图。
已知:①
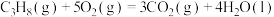
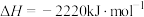
②

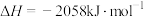
③
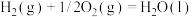
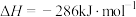
下列说法不正确的是
A. 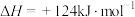 |
B.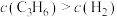 的原因: 的原因: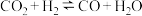 |
C.其他条件不变, 越大, 越大, 转化率越小 转化率越小 |
D.若体系只有 、 、 、 、 和 和 生成,则初始物质浓度 生成,则初始物质浓度 与流出物质浓度 与流出物质浓度 之间一定存在: 之间一定存在: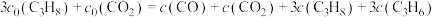 |
您最近半年使用:0次
名校
解题方法
3 . 利用 和
和 重整技术可获得合成气(主要成分为
重整技术可获得合成气(主要成分为 、
、 ),重整过程中部分反应的热化学方程式:
),重整过程中部分反应的热化学方程式:
反应Ⅰ:
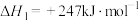
反应Ⅱ:
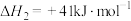
反应Ⅲ:

相同时间内,不同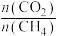 配比随温度变化对出口合成气中
配比随温度变化对出口合成气中 的影响如图所示。
的影响如图所示。

下列说法正确的是
 和
和 重整技术可获得合成气(主要成分为
重整技术可获得合成气(主要成分为 、
、 ),重整过程中部分反应的热化学方程式:
),重整过程中部分反应的热化学方程式:反应Ⅰ:

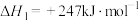
反应Ⅱ:

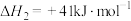
反应Ⅲ:


相同时间内,不同
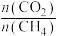 配比随温度变化对出口合成气中
配比随温度变化对出口合成气中 的影响如图所示。
的影响如图所示。
下列说法正确的是
A.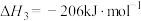 |
B. 时, 时, 点的 点的 大于 大于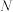 点的是反应Ⅱ导致的 点的是反应Ⅱ导致的 |
| C.使用合适的催化剂可以提高合成气的平衡产率 |
D.当 时,温度高于 时,温度高于 后 后 减小是由于反应Ⅲ平衡逆向移动 减小是由于反应Ⅲ平衡逆向移动 |
您最近半年使用:0次
解题方法
4 . 尿素  是常用的化肥与工业原料,其生产与应用有着重要的意义。
是常用的化肥与工业原料,其生产与应用有着重要的意义。
(1)尿素生产一般控制在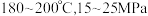 下进行,主要涉及下列反应:
下进行,主要涉及下列反应:
反应1
反应2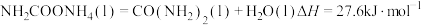
反应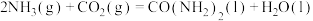 的
的
___________ 。
(2) 具有强还原性,生产尿素过程中,常通入适量氧气防止镍制容器表面的金属钝化膜
具有强还原性,生产尿素过程中,常通入适量氧气防止镍制容器表面的金属钝化膜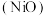 被破坏。
被破坏。
① 与
与 反应产生
反应产生 的化学方程式为
的化学方程式为___________ 。
②生产时通入的 气体中常混有少量
气体中常混有少量 。有氧气存在的条件下,
。有氧气存在的条件下, 腐蚀反应容器的速率会更快,其原因是
腐蚀反应容器的速率会更快,其原因是___________ 。
(3)尿素在结晶过程中主要副反应是尿素发生脱氨反应。其反应历程如下:
反应3 CO(NH2)2(l)=HNCO(g)+NH3(g) (快反应)
反应4 HNCO(g)+CO(NH2)2(l)=(H2NCO)2NH(l)(缩二脲) (慢反应)
①在缩二脲的结构式( )中圈出电子云密度最小的氢原子
)中圈出电子云密度最小的氢原子___________ 。
②在尿素结晶过程中,反应3可视为处于平衡状态。实验表明,在合成尿素的体系中, 的浓度越高,缩二脲生成速率越慢,其原因是
的浓度越高,缩二脲生成速率越慢,其原因是___________ 。
(4)含结晶水的 晶体表面存在结构“
晶体表面存在结构“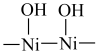 ”,用加热后的
”,用加热后的  晶体作催化剂,以
晶体作催化剂,以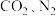 为原料,电解
为原料,电解 溶液可获得尿素。
溶液可获得尿素。
①生成尿素的电极方程式为___________ 。
②加热后的 晶体表面会产生
晶体表面会产生 位点,
位点, 位点与
位点与 位点共同形成
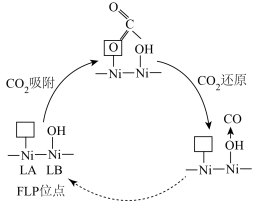
位点共同形成 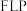 位点,其催化机理(部分)如图所示。实验表明,在
位点,其催化机理(部分)如图所示。实验表明,在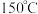 下加热
下加热  晶体得到的催化剂催化效果最好,温度过高或过低催化效果会降低的原因是
晶体得到的催化剂催化效果最好,温度过高或过低催化效果会降低的原因是___________ 。
③电解质溶液中若存在 极大地降低催化剂的活性,原因是
极大地降低催化剂的活性,原因是___________ 。
 是常用的化肥与工业原料,其生产与应用有着重要的意义。
是常用的化肥与工业原料,其生产与应用有着重要的意义。(1)尿素生产一般控制在
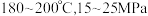 下进行,主要涉及下列反应:
下进行,主要涉及下列反应:反应1

反应2
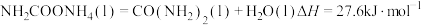
反应
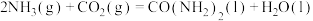 的
的
(2)
 具有强还原性,生产尿素过程中,常通入适量氧气防止镍制容器表面的金属钝化膜
具有强还原性,生产尿素过程中,常通入适量氧气防止镍制容器表面的金属钝化膜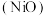 被破坏。
被破坏。①
 与
与 反应产生
反应产生 的化学方程式为
的化学方程式为②生产时通入的
 气体中常混有少量
气体中常混有少量 。有氧气存在的条件下,
。有氧气存在的条件下, 腐蚀反应容器的速率会更快,其原因是
腐蚀反应容器的速率会更快,其原因是(3)尿素在结晶过程中主要副反应是尿素发生脱氨反应。其反应历程如下:
反应3 CO(NH2)2(l)=HNCO(g)+NH3(g) (快反应)
反应4 HNCO(g)+CO(NH2)2(l)=(H2NCO)2NH(l)(缩二脲) (慢反应)
①在缩二脲的结构式(
 )中圈出电子云密度最小的氢原子
)中圈出电子云密度最小的氢原子②在尿素结晶过程中,反应3可视为处于平衡状态。实验表明,在合成尿素的体系中,
 的浓度越高,缩二脲生成速率越慢,其原因是
的浓度越高,缩二脲生成速率越慢,其原因是(4)含结晶水的
 晶体表面存在结构“
晶体表面存在结构“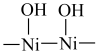 ”,用加热后的
”,用加热后的  晶体作催化剂,以
晶体作催化剂,以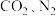 为原料,电解
为原料,电解 溶液可获得尿素。
溶液可获得尿素。
①生成尿素的电极方程式为
②加热后的
 晶体表面会产生
晶体表面会产生 位点,
位点, 位点与
位点与 位点共同形成
位点共同形成 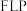 位点,其催化机理(部分)如图所示。实验表明,在
位点,其催化机理(部分)如图所示。实验表明,在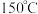 下加热
下加热  晶体得到的催化剂催化效果最好,温度过高或过低催化效果会降低的原因是
晶体得到的催化剂催化效果最好,温度过高或过低催化效果会降低的原因是③电解质溶液中若存在
 极大地降低催化剂的活性,原因是
极大地降低催化剂的活性,原因是
您最近半年使用:0次
5 .  、
、 是重要污染物,处理
是重要污染物,处理 、
、 等污染物对建设美丽中国具有重要意义。回答下列问题。
等污染物对建设美丽中国具有重要意义。回答下列问题。
(1)已知 还原
还原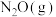 的反应机理如图1所示:
的反应机理如图1所示:
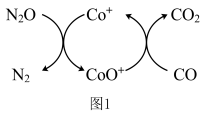
已知:
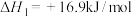

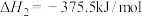
则 与
与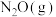 反应的热化学方程式为
反应的热化学方程式为___________ 。
(2)研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。雨水中含有来自大气中的 ,溶于水的
,溶于水的 只有部分转化为
只有部分转化为 。已知
。已知 时,
时,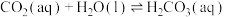
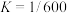 ,正反应的速率可表示为
,正反应的速率可表示为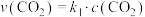 ,逆反应的速率可表示
,逆反应的速率可表示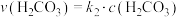 ,则
,则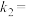
___________ (用含 的代数式表示)。
的代数式表示)。
(3)电解法转化 是实现可再生能源有效利用的关键手段之一,其装置原理如图2所示。
是实现可再生能源有效利用的关键手段之一,其装置原理如图2所示。

① 为电源的
为电源的___________ (填“正极”或“负极”),该装置的阴极的电极反应式为___________ 。
②若电解开始前两极室溶液质量相等,当电解过程转移了 电子,则阴阳极室溶液质量差为
电子,则阴阳极室溶液质量差为___________  。
。
(4)近年来,低温等离子技术是在高压放电下, 产生
产生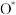 自由基,
自由基,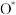 自由基将
自由基将 氧化为
氧化为 后,再用
后,再用 溶液吸收,达到消除
溶液吸收,达到消除 的目的。实验室将模拟气(
的目的。实验室将模拟气( 、
、 、
、 )以一定流速通入低温等离子体装置,实验装置如图3所示。
)以一定流速通入低温等离子体装置,实验装置如图3所示。

已知:
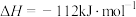 。
。
①等离子体技术在低温条件下可提高 的转化率,原因是
的转化率,原因是___________ 。
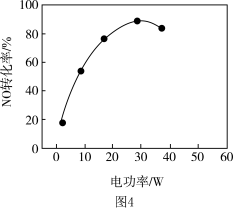
②其他条件相同,等离子体的电功率与 的转化率关系如图4所示,当电功率大于
的转化率关系如图4所示,当电功率大于 时,
时, 转化率下降的原因可能是
转化率下降的原因可能是___________ 。
 、
、 是重要污染物,处理
是重要污染物,处理 、
、 等污染物对建设美丽中国具有重要意义。回答下列问题。
等污染物对建设美丽中国具有重要意义。回答下列问题。(1)已知
 还原
还原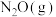 的反应机理如图1所示:
的反应机理如图1所示: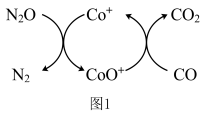
已知:

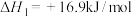

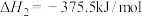
则
 与
与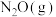 反应的热化学方程式为
反应的热化学方程式为(2)研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。雨水中含有来自大气中的
 ,溶于水的
,溶于水的 只有部分转化为
只有部分转化为 。已知
。已知 时,
时,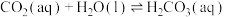
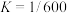 ,正反应的速率可表示为
,正反应的速率可表示为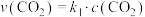 ,逆反应的速率可表示
,逆反应的速率可表示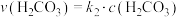 ,则
,则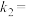
 的代数式表示)。
的代数式表示)。(3)电解法转化
 是实现可再生能源有效利用的关键手段之一,其装置原理如图2所示。
是实现可再生能源有效利用的关键手段之一,其装置原理如图2所示。
①
 为电源的
为电源的②若电解开始前两极室溶液质量相等,当电解过程转移了
 电子,则阴阳极室溶液质量差为
电子,则阴阳极室溶液质量差为 。
。(4)近年来,低温等离子技术是在高压放电下,
 产生
产生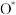 自由基,
自由基,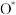 自由基将
自由基将 氧化为
氧化为 后,再用
后,再用 溶液吸收,达到消除
溶液吸收,达到消除 的目的。实验室将模拟气(
的目的。实验室将模拟气( 、
、 、
、 )以一定流速通入低温等离子体装置,实验装置如图3所示。
)以一定流速通入低温等离子体装置,实验装置如图3所示。
已知:

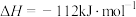 。
。①等离子体技术在低温条件下可提高
 的转化率,原因是
的转化率,原因是②其他条件相同,等离子体的电功率与
 的转化率关系如图4所示,当电功率大于
的转化率关系如图4所示,当电功率大于 时,
时, 转化率下降的原因可能是
转化率下降的原因可能是
您最近半年使用:0次
名校
6 . 环氧乙烷(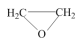 ,简称EO)是一种重要的工业原料和消毒剂。工业上用乙烯制备EO。
,简称EO)是一种重要的工业原料和消毒剂。工业上用乙烯制备EO。
(1)一定条件下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)的过程中部分物料与能量变化如图所示。
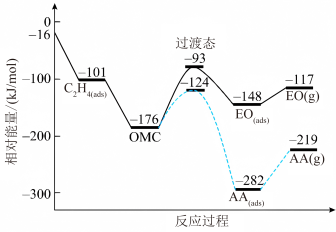
①中间体OMC生成吸附态EO(ads)的活化能为_______ kJ/mol。
②由EO(g)生成AA(g)的热化学方程式为_______ 。
(2)一定条件下,用Ag作催化剂,氧气直接氧化乙烯制环氧乙烷(部分机理未配平)。
主反应:2CH2=CH2(g)+O2(g)=2EO(g) ΔH=-213.8kJ/mol
副反应:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH=-1323kJ/mol
催化机理:O2+Ag(助剂)→ (ads)+Ag+
(ads)+Ag+
 (ads)+ CH2=CH2+Ag+→EO+ O(ads)+Ag
(ads)+ CH2=CH2+Ag+→EO+ O(ads)+Ag
O(ads)+ CH2=CH2→CO2+H2O
实际生产采用220-260℃的可能原因是________ 。
(3)乙烯电解制备EO的原理示意如图。
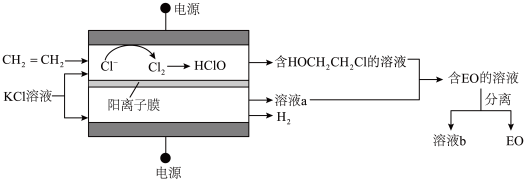
阳极室产生Cl2后发生的反应有:Cl2+H2O=HCl+HClO、CH2=CH2+HClO=HOCH2CH2Cl。
法拉第效率FE的定义:FE(B)= ×100%
×100%
①若FE(EO)=100%,则溶液b的溶质为________ (化学式)。
②一定条件下,反应物按一定流速通过该装置。当乙烯完全消耗时,测得FE(EO)≈70%,S(EO)≈97%。
推测FE(EO)≈70%的原因:若没有生成EO的乙烯全部在阳极放电生成CO2,则生成CO2的电极反应方程式为______ ,FE(CO2)≈____ %。经检验阳极放电产物没有CO2,则S(EO)≈97%的可能原因是______ 。
 ,简称EO)是一种重要的工业原料和消毒剂。工业上用乙烯制备EO。
,简称EO)是一种重要的工业原料和消毒剂。工业上用乙烯制备EO。(1)一定条件下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)的过程中部分物料与能量变化如图所示。

①中间体OMC生成吸附态EO(ads)的活化能为
②由EO(g)生成AA(g)的热化学方程式为
(2)一定条件下,用Ag作催化剂,氧气直接氧化乙烯制环氧乙烷(部分机理未配平)。
主反应:2CH2=CH2(g)+O2(g)=2EO(g) ΔH=-213.8kJ/mol
副反应:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH=-1323kJ/mol
催化机理:O2+Ag(助剂)→
 (ads)+Ag+
(ads)+Ag+ (ads)+ CH2=CH2+Ag+→EO+ O(ads)+Ag
(ads)+ CH2=CH2+Ag+→EO+ O(ads)+AgO(ads)+ CH2=CH2→CO2+H2O
实际生产采用220-260℃的可能原因是
(3)乙烯电解制备EO的原理示意如图。

阳极室产生Cl2后发生的反应有:Cl2+H2O=HCl+HClO、CH2=CH2+HClO=HOCH2CH2Cl。
法拉第效率FE的定义:FE(B)=
 ×100%
×100%①若FE(EO)=100%,则溶液b的溶质为
②一定条件下,反应物按一定流速通过该装置。当乙烯完全消耗时,测得FE(EO)≈70%,S(EO)≈97%。
推测FE(EO)≈70%的原因:若没有生成EO的乙烯全部在阳极放电生成CO2,则生成CO2的电极反应方程式为
您最近半年使用:0次
7 . 我国提出“碳达峰”目标是在2030年前达到最高值,2060年前达到“碳中和”。因此,二氧化碳的综合利用尤为重要。
(1)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚( )也有广泛的应用。
)也有广泛的应用。
反应Ⅰ:
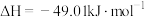
反应Ⅱ:
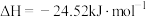
反应Ⅲ:
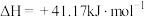
①结合计算分析反应 的自发性:
的自发性:___________ 。
②恒压、投料比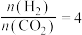 的情况下,不同温度下
的情况下,不同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的
的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)如下图所示:
消耗总量的百分比)如下图所示:
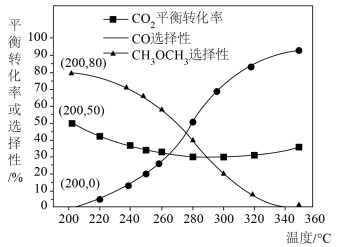
当温度超过 ,
, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是___________ 。
③工业实际设计温度一般在 范围内变化,不能过高的原因是
范围内变化,不能过高的原因是___________ 。
(2)研究表明,在电解质水溶液中, 气体可被电化学还原。
气体可被电化学还原。
① 在碱性介质中电还原为正丙醇(
在碱性介质中电还原为正丙醇(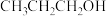 )的电极反应方程式为
)的电极反应方程式为___________ 。
②在电解质水溶液中,三种不同催化剂( 、
、 、
、 )上
)上 电还原为
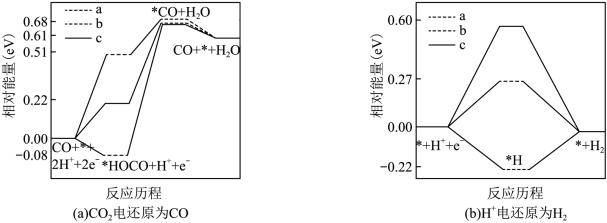
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。由此判断,
的反应可同时发生),相对能量变化如图。由此判断, 电还原为
电还原为 从易到难的顺序为
从易到难的顺序为___________ (用 、
、 、
、 字母排序)。
字母排序)。
(3) 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( 、
、 表示乙苯分子中
表示乙苯分子中 或
或 原子的位置;
原子的位置; 、
、 为催化剂的活性位点,其中
为催化剂的活性位点,其中 位点带部分正电荷,
位点带部分正电荷,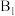 、
、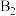 位点带部分负电荷)。
位点带部分负电荷)。

图中所示反应机理中步骤Ⅰ和步骤Ⅱ可描述为___________ 。
(1)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(
 )也有广泛的应用。
)也有广泛的应用。反应Ⅰ:

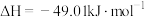
反应Ⅱ:

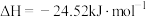
反应Ⅲ:

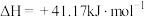
①结合计算分析反应
 的自发性:
的自发性:②恒压、投料比
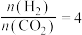 的情况下,不同温度下
的情况下,不同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的
的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)如下图所示:
消耗总量的百分比)如下图所示:
当温度超过
 ,
, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是③工业实际设计温度一般在
 范围内变化,不能过高的原因是
范围内变化,不能过高的原因是(2)研究表明,在电解质水溶液中,
 气体可被电化学还原。
气体可被电化学还原。①
 在碱性介质中电还原为正丙醇(
在碱性介质中电还原为正丙醇(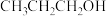 )的电极反应方程式为
)的电极反应方程式为②在电解质水溶液中,三种不同催化剂(
 、
、 、
、 )上
)上 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。由此判断,
的反应可同时发生),相对能量变化如图。由此判断, 电还原为
电还原为 从易到难的顺序为
从易到难的顺序为 、
、 、
、 字母排序)。
字母排序)。
(3)
 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示( 、
、 表示乙苯分子中
表示乙苯分子中 或
或 原子的位置;
原子的位置; 、
、 为催化剂的活性位点,其中
为催化剂的活性位点,其中 位点带部分正电荷,
位点带部分正电荷,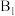 、
、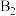 位点带部分负电荷)。
位点带部分负电荷)。
图中所示反应机理中步骤Ⅰ和步骤Ⅱ可描述为
您最近半年使用:0次
解题方法
8 . 脱除沼气中的H2S具有重要意义,脱除H2S有多种方法。
(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g) =169.8kJ/mol
=169.8kJ/mol
反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g) =63.7kJ/mol
=63.7kJ/mol
现将硫化氢和甲烷按照2:1体积比投料,并用N2稀释,常压和不同温度下反应,反应相同时间后,H2、S2和CS2体积分数如图所示。 =
=___________ 。
②1050℃时,H2的体积分数为___________ 。
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,其原因可能是___________ 。
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。___________ 。
②与受热分解法相比,光电催化法的优点是___________ 。
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。___________ 。
②脱除一段时间后,催化剂的活性降低,原因是___________ 。
(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g)
 =169.8kJ/mol
=169.8kJ/mol反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g)
 =63.7kJ/mol
=63.7kJ/mol现将硫化氢和甲烷按照2:1体积比投料,并用N2稀释,常压和不同温度下反应,反应相同时间后,H2、S2和CS2体积分数如图所示。

 =
=②1050℃时,H2的体积分数为
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,其原因可能是
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。
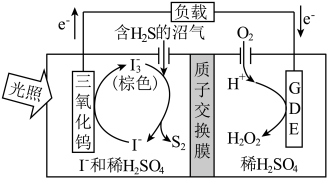
②与受热分解法相比,光电催化法的优点是
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。
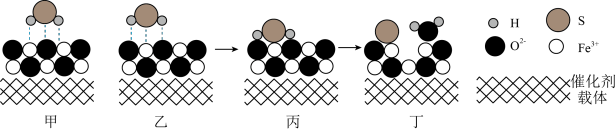
②脱除一段时间后,催化剂的活性降低,原因是
您最近半年使用:0次
9 . 我国要在2030年前实现碳达峰、2060年前实现碳中和的目标,CO2的捕集与转化是研究的重要课题。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=___________ kJ·mol-1。
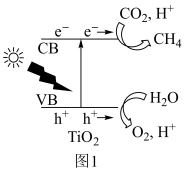
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),___________ 。
(3)一种电化学法将CO2转化为乙烯的原理如图2所示。
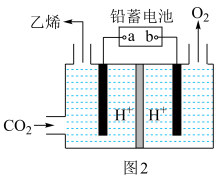
①阴极上的电极反应式为___________ 。
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为___________ 。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),

(3)一种电化学法将CO2转化为乙烯的原理如图2所示。

①阴极上的电极反应式为
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为
您最近半年使用:0次
名校
解题方法
10 .  催化剂能催化
催化剂能催化 脱除烟气中的NO,反应为
脱除烟气中的NO,反应为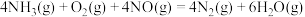

(1)催化剂___________ 改变ΔH(填“能”或“不能”)
(2)催化剂的制备。将预先制备的一定量的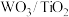 粉末置于80℃的水中,在搅拌下加入一定量的
粉末置于80℃的水中,在搅拌下加入一定量的 溶液,经蒸发焙烧等工序得到颗粒状
溶液,经蒸发焙烧等工序得到颗粒状 催化剂。在水溶液中
催化剂。在水溶液中 水解为
水解为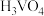 沉淀的离子方程式为
沉淀的离子方程式为___________ ;
(3)催化剂的应用。将一定物质的量浓度的NO、 、
、 (其余为
(其余为 )气体匀速通过装有
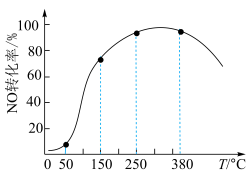
)气体匀速通过装有 催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在50~150℃范围内,NO转化为
催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在50~150℃范围内,NO转化为 的转化率迅速上升,原因是:
的转化率迅速上升,原因是:___________
(4)废催化剂的回收。回收 催化剂并制备
催化剂并制备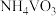 的过程可表示为
的过程可表示为

①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有___________ 。
②向pH=8的 溶液中加入过量的
溶液中加入过量的 溶液,生成
溶液,生成 沉淀。已知
沉淀。已知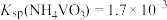 ,加过量
,加过量 溶液的目的是
溶液的目的是___________ 。
(5)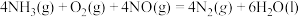 ΔH
ΔH___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
 催化剂能催化
催化剂能催化 脱除烟气中的NO,反应为
脱除烟气中的NO,反应为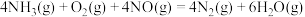

(1)催化剂
(2)催化剂的制备。将预先制备的一定量的
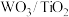 粉末置于80℃的水中,在搅拌下加入一定量的
粉末置于80℃的水中,在搅拌下加入一定量的 溶液,经蒸发焙烧等工序得到颗粒状
溶液,经蒸发焙烧等工序得到颗粒状 催化剂。在水溶液中
催化剂。在水溶液中 水解为
水解为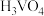 沉淀的离子方程式为
沉淀的离子方程式为(3)催化剂的应用。将一定物质的量浓度的NO、
 、
、 (其余为
(其余为 )气体匀速通过装有
)气体匀速通过装有 催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在50~150℃范围内,NO转化为
催化剂的反应器,测得NO的转化率随温度的变化如题图所示。反应温度在50~150℃范围内,NO转化为 的转化率迅速上升,原因是:
的转化率迅速上升,原因是:
(4)废催化剂的回收。回收
 催化剂并制备
催化剂并制备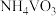 的过程可表示为
的过程可表示为
①酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有
②向pH=8的
 溶液中加入过量的
溶液中加入过量的 溶液,生成
溶液,生成 沉淀。已知
沉淀。已知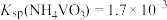 ,加过量
,加过量 溶液的目的是
溶液的目的是(5)
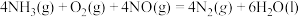 ΔH
ΔH (填“>”“<”或“=”)
(填“>”“<”或“=”)
您最近半年使用:0次



