1 . 在容积为2L的恒容密闭容器中发生反应 ,图Ⅰ表示200℃时容器中A、B、C的物质的量随时间的变化关系,图Ⅱ表示不同温度下达到平衡时C的体积分数随起始
,图Ⅰ表示200℃时容器中A、B、C的物质的量随时间的变化关系,图Ⅱ表示不同温度下达到平衡时C的体积分数随起始 的变化关系,则下列结论正确的是
的变化关系,则下列结论正确的是

 ,图Ⅰ表示200℃时容器中A、B、C的物质的量随时间的变化关系,图Ⅱ表示不同温度下达到平衡时C的体积分数随起始
,图Ⅰ表示200℃时容器中A、B、C的物质的量随时间的变化关系,图Ⅱ表示不同温度下达到平衡时C的体积分数随起始 的变化关系,则下列结论正确的是
的变化关系,则下列结论正确的是
A.由图Ⅱ可知反应 的 的 ,且 ,且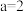 |
B.200℃时,反应从开始到平衡的平均速率 |
C.200℃时,向容器中充入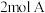 和 和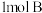 ,达到平衡时,A的体积分数等于0.5 ,达到平衡时,A的体积分数等于0.5 |
| D.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)<v(逆) |
您最近一年使用:0次
2 . 在体积均为2L的恒容容器中,分别在200℃和T℃时,发生如下反应 ,A的物质的量浓度(单位:mol/L)随时间变化的有关实验数据见下表:
,A的物质的量浓度(单位:mol/L)随时间变化的有关实验数据见下表:
下列有关该反应的描述正确的是
 ,A的物质的量浓度(单位:mol/L)随时间变化的有关实验数据见下表:
,A的物质的量浓度(单位:mol/L)随时间变化的有关实验数据见下表:时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
200℃ | 0.80 | 0.55 | 0.35 | 0.20 | 0.15 | 0.15 |
T℃ | 1.00 | 0.65 | 0.35 | 0.18 | 0.18 | 0.18 |
| A.在200℃时,4min内用B表示的化学反应速率为0.225mol/(L·min) |
| B.T℃下,6min时反应刚好达到平衡状态 |
| C.从表中可以看出T>200℃ |
| D.在该题目条件下,无法判断正反应方向是否为放热反应 |
您最近一年使用:0次
2023-07-05更新
|
284次组卷
|
3卷引用:湖北省黄石市第二中学2023-2024学年高二上学期第三次统测化学试题
名校
解题方法
3 . 反应A+3B=2C+D在四种不同情况下的反应速率分别为①v(A)=0.15 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.5 mol·L-1·s-1 ④v(D)=0.45 mol·L-1·s-1,则反应速率由快到慢的顺序为
| A.④>③>①>② | B.②>④>③>① |
| C.②>③>④>① | D.④>③>②>① |
您最近一年使用:0次
2022-12-21更新
|
366次组卷
|
21卷引用:2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷
2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷(已下线)2010-2011学年内蒙古赤峰二中高一下学期期中考试化学试卷(已下线)2010-2011学年辽宁省辽南协作体高一下学期期中考试化学试卷(已下线)2010—2011学年福建省三明二中高一下期期中考试化学试卷(已下线)2011-2012学年云南省玉溪一中高二上学期期末考试化学试卷(已下线)2011-2012年湖南凤凰华鑫中学高一下学期第三次月考(理)化学试卷(已下线)【南昌新东方】2019 外国语 高一下期中河北省易县中学2019-2020学年高一4月线上考试(A部)化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题山西省运城市2019-2020学年高一下学期期中调研化学试题陕西省咸阳百灵学校2019-2020学年高一下学期第二次月考化学试题新疆生产建设兵团第四师第一中学2019-2020学年高一下学期期中考试化学试题河北省唐山市英才国际学校2020-2021学年高一下学期期中考试化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题(已下线)期末综合检测卷03【综合检测】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)吉林省延边朝鲜族自治州延边二中北校区2020-2021学年高一下学期第一次月考化学试题浙江省台州市书生中学2021-2022学年高一下学期阶段性测试(3月)化学试题山东省德州市跃华学校2020-2021学年高一下学期第二次质量调研化学试题6.1.1化学反应速率(课后)-2019苏教版必修2课前课中课后上海市回民中学2023-2024学年高二上学期期中考试化学试题云南省保山市腾冲市第八中学2022-2023学年高一下学期期中考试化学试卷
解题方法
4 . 由H、C、N、O、S等元素形成多种化合物在生产生活中有着重要应用。
(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出CO2与NH3合成尿素同时生成液态水的热化学反应方程式:___________ 。
(2)某密闭容器中存在反应:CO(g)+2H2(g) CH3OH(g),起始时容器中只有a mol/LCO和b mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
CH3OH(g),起始时容器中只有a mol/LCO和b mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
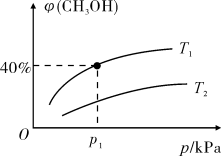
①温度T1和T2时对应的平衡常数分别为K1、K2,则K1___________ K2(填“>”“<”或“=”);
②若恒温恒容条件下,起始时充入1 mol CO和2 mol H2,达平衡后,CO的转化率为α1,此时,若再充入1 mol CO和2 mol H2,再次达平衡后,CO的转化率为α2,则α1___________ α2(填“>”“<”“=”或“无法确定”)。
(3)最近有人尝试用H2还原工业尾气中SO2,该反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:
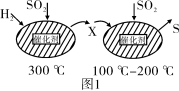
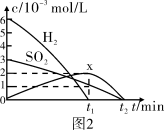
①分析可知X为___________ (写化学式),0~t1时间段的温度为___________ ,0~t1时间段用SO2表示的化学反应速率为___________ 。
②总反应的化学方程式为___________ 。
(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
写出CO2与NH3合成尿素同时生成液态水的热化学反应方程式:
(2)某密闭容器中存在反应:CO(g)+2H2(g)
 CH3OH(g),起始时容器中只有a mol/LCO和b mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
CH3OH(g),起始时容器中只有a mol/LCO和b mol/L H2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
①温度T1和T2时对应的平衡常数分别为K1、K2,则K1
②若恒温恒容条件下,起始时充入1 mol CO和2 mol H2,达平衡后,CO的转化率为α1,此时,若再充入1 mol CO和2 mol H2,再次达平衡后,CO的转化率为α2,则α1
(3)最近有人尝试用H2还原工业尾气中SO2,该反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:


①分析可知X为
②总反应的化学方程式为
您最近一年使用:0次
名校
5 . 在一定温度时,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生如下反应:A(s)+2B(g)  C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol·L-1 。下列叙述不正确的是
C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol·L-1 。下列叙述不正确的是
 C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol·L-1 。下列叙述不正确的是
C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol·L-1 。下列叙述不正确的是| A.在5 min内该反应用C的浓度变化表示的反应速率为0.02 mol·L-1·min-1 |
| B.5 min时,容器内D的浓度为0.2 mol·L-1 |
| C.该可逆反应随反应的进行容器内压强逐渐减小 |
| D.5 min时容器内气体总的物质的量为2.5 mol |
您最近一年使用:0次
2021-08-25更新
|
1611次组卷
|
9卷引用:湖北省阳新高中2021-2022学年高二上学期9月月考化学试题
湖北省阳新高中2021-2022学年高二上学期9月月考化学试题(已下线)2.1.1 化学反应速率-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)2.1.1 化学反应速率的表示方法-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)河南省原阳县第三高级中学2021-2022学年高二上学期第一次月考化学试题 (已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)河南省通许县一中2022—2023年高二上学期第一次月考化学试题【定心卷】2.2.1 化学反应速率随堂练习-人教版2023-2024学年选择性必修1广西横州市横州中学2023-2024学年高二上学期9月月考化学试题
解题方法
6 . 反应4A(g)+3B(g)=2C(g)+5D(g)在四种不同条件下的反应速率分别为( )
①v(A)=0.02mol·L-1·s-1;
②v(B)=0.6mol·L-1·min-1;
③v(C)=0.3mol·L-1·min-1;
④v(D)=1.2mol·L-1·min-1
其中表示该反应速率最慢的是( )
①v(A)=0.02mol·L-1·s-1;
②v(B)=0.6mol·L-1·min-1;
③v(C)=0.3mol·L-1·min-1;
④v(D)=1.2mol·L-1·min-1
其中表示该反应速率最慢的是( )
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
解题方法
7 . 随着社会的发展 ,环境问题越来越受到人们的关注。请回答下列相关问题。
I.汽车尾气中含有 CO、NO 等有害气体 ,某新型催化剂能促使 NO、CO 转化为 2 种无毒气体。T℃时,将 0.8 molNO 和 0. 8molCO 充入容积为 2L 的密闭容器中,模拟尾气转化,容器中 NO 物质的量随时间变化如图所示 。
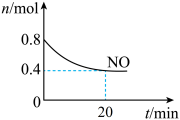
(1)将NO、CO转化为2种无毒气体的化学方程式是___________________ 。
(2)反应开始至20min,v (NO) =_________ mol/ (L• min) 。
(3)下列说法正确的是__________ 。
a.新型催化剂可以加快 NO、CO的转化
b.该反应进行到 20 min 时达到化学平衡状态
c.平衡时CO的浓度是 0.4 mol/ L
d.混合气体的总压强不随时间的变化而变化说明上述反应达到平衡状态
e.保持容器体积不变,充入 He 增大压强,反应速率加快
II我国最近在太阳能光电催化— 化学耦合分解硫化氢研究中获得新进展 ,相关装置如图所示。
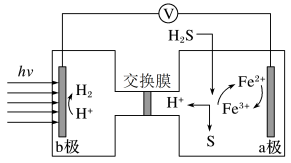
(1)负极为_________ 极(填“ a” 或“ b” ) 发生的电极反应式为______________ 。
(2)为使电池持续放电 ,交换膜需选用___________ 交换膜(填“阳离子” 或“阴离子”或“质子”)。
(3)分解硫化氢的离子方程式为_______________________ 。
I.汽车尾气中含有 CO、NO 等有害气体 ,某新型催化剂能促使 NO、CO 转化为 2 种无毒气体。T℃时,将 0.8 molNO 和 0. 8molCO 充入容积为 2L 的密闭容器中,模拟尾气转化,容器中 NO 物质的量随时间变化如图所示 。

(1)将NO、CO转化为2种无毒气体的化学方程式是
(2)反应开始至20min,v (NO) =
(3)下列说法正确的是
a.新型催化剂可以加快 NO、CO的转化
b.该反应进行到 20 min 时达到化学平衡状态
c.平衡时CO的浓度是 0.4 mol/ L
d.混合气体的总压强不随时间的变化而变化说明上述反应达到平衡状态
e.保持容器体积不变,充入 He 增大压强,反应速率加快
II我国最近在太阳能光电催化— 化学耦合分解硫化氢研究中获得新进展 ,相关装置如图所示。

(1)负极为
(2)为使电池持续放电 ,交换膜需选用
(3)分解硫化氢的离子方程式为
您最近一年使用:0次
2020-07-26更新
|
290次组卷
|
2卷引用:湖北省阳新高中2021-2022学年高二上学期9月月考化学试题
名校
解题方法
8 . 某温度时,在2L恒容容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
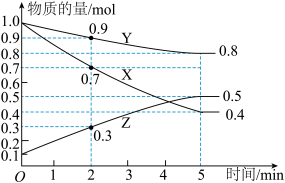
(1)由图中的数据分析,该反应的化学方程式为___ 。
(2)反应开始至2min、5min时,Z的平均反应速率分别为___ 、___ 。
(3)5min后Z的生成速率___ (填“大于”“小于”或“等于”)5min末Z的生成速率。

(1)由图中的数据分析,该反应的化学方程式为
(2)反应开始至2min、5min时,Z的平均反应速率分别为
(3)5min后Z的生成速率
您最近一年使用:0次
2020-05-15更新
|
160次组卷
|
10卷引用:2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷
2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷(已下线)2010年浙江省浙东北三校高一第二学期期中联考化学试题(已下线)2012年苏教版高中化学必修2 2.1化学反应速率与反应限度练习卷(已下线)2012-2013学年江苏省江都区丁沟中学高一下学期期中考试化学试卷(已下线)2012-2013学年河北省存瑞中学高一下学期第三次月考化学试卷2014-2015河北省成安一中等三校高一下学期期中联考化学试卷2014-2015学年湖北省松滋一中高一下学期6月月考化学试卷黑龙江省青冈县一中2018-2019学年高一下学期期末考试(A+班)化学试题山西省运城市临猗县临晋中学2019-2020学年高一下学期开学复课摸底考试化学试题(已下线)2.1+化学反应速率-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)
名校
解题方法
9 . 研究氮氧化合物的治理是环保的一项重要工作,合理应用和处理氮的化合物,在生产生活中有着重要的意义。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+181.5 kJ·mol-1某科研小组尝试利用固体表面催化工艺进行NO的分解。若用●● 、●○ 、○○和 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如下图所示。从吸附到解吸的过程中,能量状态最低的是
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如下图所示。从吸附到解吸的过程中,能量状态最低的是___________ (填字母序号)。
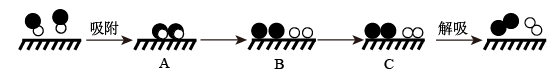
(2)为减少汽车尾气中NOx的排放,常采用CxHy(烃)催化还原NOx消除氮氧化物的污染。
例如:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
②CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H2=-1160 kJ/mol
③CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3
则△H3=___________ 。
(3)亚硝酰氯(ClNO)是有机合成中常用试剂,已知:2NO(g)+Cl2(g) 2 ClNO(g) △H<0
2 ClNO(g) △H<0
①一定温度下,将2 molNO与2 molCl2置于2L密闭容器中发生反应,若该反应4min后达平衡,此时压强是初始的0.8倍,则平均反应速率v(Cl2)=___________ mol·L-1·min-1。下列可判断反应达平衡状态的是___________ (项序号字母)。
A 混合气体的平均相对分子质量不变
B 混合气体密度保持不变
C NO和Cl2的物质的量之比保持不变
D 每消耗1 mol NO同时生成1molClNO
②为了加快化学反应速率,同时提高NO的转化率,其他条件不变时,可采取的措施有___________ (填选项序号字母)。
A 升高温度 B 缩小容器体积
C 再充入Cl2气体 D 使用合适的催化剂
③一定条件下在恒温恒容的密闭容器中,按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图象如图(b)所示,当n(NO)/n(Cl2)=2.5时,达到平衡状态,ClNO的体积分数可能是图中D、E、F三点中的___________ 点。
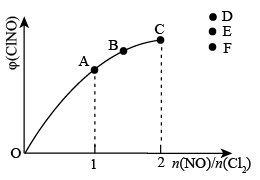
(4)已知2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g) N2O2(g)(快),v1正=k1正c2(NO),v1逆 =k1逆c (N2O2)
N2O2(g)(快),v1正=k1正c2(NO),v1逆 =k1逆c (N2O2)
②N2O2(g)+O2(g) 2NO2(g)(慢),v2正=k2正c(N2O2)·c(O2),v2逆=k2逆c2(NO2)
2NO2(g)(慢),v2正=k2正c(N2O2)·c(O2),v2逆=k2逆c2(NO2)
比较反应①的活化能E1与反应②的活化能E2的大小:E1___________ E2(填“>”、"<”或“=”):2NO(g)+O2(g) 2NO2(g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为
2NO2(g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为___________ 。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+181.5 kJ·mol-1某科研小组尝试利用固体表面催化工艺进行NO的分解。若用●● 、●○ 、○○和
 分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如下图所示。从吸附到解吸的过程中,能量状态最低的是
分别表示N2、NO、O2和固体催化剂,在固体催化剂表面分解NO的过程如下图所示。从吸附到解吸的过程中,能量状态最低的是
(2)为减少汽车尾气中NOx的排放,常采用CxHy(烃)催化还原NOx消除氮氧化物的污染。
例如:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
②CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H2=-1160 kJ/mol
③CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3
则△H3=
(3)亚硝酰氯(ClNO)是有机合成中常用试剂,已知:2NO(g)+Cl2(g)
 2 ClNO(g) △H<0
2 ClNO(g) △H<0①一定温度下,将2 molNO与2 molCl2置于2L密闭容器中发生反应,若该反应4min后达平衡,此时压强是初始的0.8倍,则平均反应速率v(Cl2)=
A 混合气体的平均相对分子质量不变
B 混合气体密度保持不变
C NO和Cl2的物质的量之比保持不变
D 每消耗1 mol NO同时生成1molClNO
②为了加快化学反应速率,同时提高NO的转化率,其他条件不变时,可采取的措施有
A 升高温度 B 缩小容器体积
C 再充入Cl2气体 D 使用合适的催化剂
③一定条件下在恒温恒容的密闭容器中,按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图象如图(b)所示,当n(NO)/n(Cl2)=2.5时,达到平衡状态,ClNO的体积分数可能是图中D、E、F三点中的

(4)已知2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:①2NO(g)
 N2O2(g)(快),v1正=k1正c2(NO),v1逆 =k1逆c (N2O2)
N2O2(g)(快),v1正=k1正c2(NO),v1逆 =k1逆c (N2O2)②N2O2(g)+O2(g)
 2NO2(g)(慢),v2正=k2正c(N2O2)·c(O2),v2逆=k2逆c2(NO2)
2NO2(g)(慢),v2正=k2正c(N2O2)·c(O2),v2逆=k2逆c2(NO2)比较反应①的活化能E1与反应②的活化能E2的大小:E1
 2NO2(g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为
2NO2(g)的平衡常数K与上述反应速率常数k1正、k1逆、k2正、k2逆的关系式为
您最近一年使用:0次
2019-04-09更新
|
478次组卷
|
3卷引用:湖北省黄石市有色第一中学2021-2022学年高二上学期期中考试化学试题
真题
名校
10 . 对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
| A.v(W)=3v(Z) | B.2v(X)=3v(Z) | C.2v(X)=v(Y) | D.3v(W)=2v(X) |
您最近一年使用:0次
2019-01-30更新
|
5584次组卷
|
126卷引用:湖北省黄石市育英高中2020-2021学年高二上学期第一次月考化学试题
湖北省黄石市育英高中2020-2021学年高二上学期第一次月考化学试题2010年普通高等学校招生全国统一考试化学试题(海南卷)2010年高考化学试题分项专题八 化学反应速率和化学平衡(已下线)2010年辽宁省本溪市高一下学期期末考试化学A卷(已下线)2010年辽宁省沈阳四校联合体高二上学期期中考试化学卷(已下线)2010年河北省黄骅中学高二上学期期中考试化学试卷(已下线)2011-2012学年山东省宁阳四中高二上学期期中学分认定化学试卷(已下线)2011-2012学年云南蒙自高中高二上学期期中考试化学试卷(已下线)2011-2012学年江苏省南京三中高二下学期期末考试化学选修试卷(已下线)2011-2012学年陕西师大附中高二年级第一学期期中考试化学试卷(已下线)2013-2014学年山东省临沂市重点中学高二上学期期中考试化学试卷(已下线)2013-2014浙江省宁波市高一下学期期末考试化学试卷(已下线)2014秋季甘肃省白银市一中高二第一学期期中理科化学试卷2015-2016学年河北省定兴第三中学高二上学期第一次月考化学试卷2015-2016学年甘肃省张掖二中高二上学期10月月考化学试卷2015-2016学年山东省淄博市淄川一中等三校高二上期末联考化学试卷2015-2016学年山西省怀仁一中高一下期中化学试卷2015-2016学年北大附中河南分校高一下期末化学试卷2015-2016学年湖南省娄底市重点中学高一下学期期末化学试卷2016-2017学年河南郑州外国语学校高二上开学考试化学2016-2017学年黑龙江哈尔滨师大附中高二上开学考化学卷2016-2017学年江西省玉山一中高二上第一次月考化学卷2016-2017学年河南省新乡市延津县中学高二上第一次月考化学卷2016-2017学年广西宾阳中学高二上9月月考化学试卷2016-2017学年江西省赣州市十四校高二上学期期中化学试卷甘肃省兰州第一中学2016-2017学年高一下学期期中考试化学试题湖南省宁远县第一中学2016-2017学年高一下学期期中考试化学试题贵州市兴义市第八中学2016-2017学年高一下学期期中考试化学试题湖南省邵阳市第二中学2016-2017学年高一下学期期末考试(理)化学试题湖南省邵阳市第二中学2016-2017学年高一下学期期末考试(文)化学试题河南省平顶山市郏县第一高级中学2017-2018学年高二上学期第一次月考化学试题河北省涞水波峰中学2017-2018学年高二(实验班)上学期9月月考化学试题2018届高三一轮复习化学:微考点53-化学反应速率的计算河北省武邑中学2017-2018学年高二上学期第一次月考化学试题江西省南昌市第二中学2017-2018学年高二上学期第一次月考化学试题云南省德宏州芒市第一中学2017-2018学年高二上学期期中考试化学试题黑龙江省哈尔滨市第三中学2017-2018学年高二上学期期中考试化学试题云南省曲靖市宣威市第三中学2017-2018学年高二下学期3月月考化学试题【全国百强校】新疆生产建设兵团第二中学2017-2018学年高一下学期期中考试化学试题【全国百强校】北京101中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2017-2018学年高一下学期期末考试化学试题(已下线)2018年9月4日 《每日一题》人教必修4-化学反应速率的计算河北省蠡县中学2018-2019学年高二上学期第一次(8月)月考化学试题河北省保定市蠡县中学2018-2019学年高二上学期9月月考化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高二上学期10月月考化学试题甘肃省岷县第二中学2018-2019学年高二上学期期中考试化学试题步步为赢 高一化学暑假作业:作业十九 综合评估新疆阿克苏市高级中学2018-2019学年高一下学期期末考试化学试题黑龙江省哈尔滨市第六中学2018-2019学年高一下学期期末考试化学试题(已下线)2019年9月3日《每日一题》 选修4 化学反应速率的计算辽宁省建平第二高级中学2019-2020学年高二上学期9月月考化学试题甘肃省武威市第六中学2019-2020学年高二上学期第二次段考化学试题海南省文昌中学2019-2020学年高二上学期第二次月考化学试题云南省河口县第一中学2019-2020学年高二上学期12月月考化学试题云南省楚雄市实验中学2018—2019学年高二上学期11月月考化学试题云南省绥江县第三中学2019-2020学年高二上学期期末考试化学试题新疆昌吉回族自治州玛纳斯县第一中学2018-2019学年高二上学期第一次月考化学试题课时1 化学反应速率——A学习区 夯实基础(苏教版必修2)新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二上学期第一次月考化学试题新疆昌吉市教育共同体2019-2020学年高一下学期期中考试化学试题江苏省徐州市2018~2019学年高一下学期期末抽测化学试题黑龙江省哈尔滨市宾县第二中学2019-2020学年高二下学期期中考试化学试题江西省宜春市高安中学2019-2020学年高一下学期期中考试化学(B)试题黑龙江省哈尔滨市双城区兆麟中学2019-2020学年度高一下学期期中考试化学试题宁夏银川市宁夏大学附属中学2019-2020学年高二下期第二次月考化学试题黑龙江省海林市朝鲜族中学2019-2020学年高一下学期期末考试化学试题甘肃省武威市第十八中学2019-2020学年高一下学期期末模拟考试化学试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题吉林省松原市前郭尔罗斯蒙古族自治县蒙古族中学2019-2020学年高一下学期网课检测化学试题云南省弥勒市第一中学2019-2020学年高一下学期化学期末复习题吉林省长春实验中学2019-2020学年高一6月月考化学试题陕西省商洛市洛南中学2020-2021学年高二上学期第一次月考化学试题(已下线)2.1 化学反应速率(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第二章 化学反应速率和化学平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)河南省驻马店市正阳县高级中学2020-2021学年高二上学期第一次月考化学试题宁夏回族自治区青铜峡市高级中学2020-2021学年高二上学期第一次月考化学试题安徽省安庆市宜秀区白泽湖中学2020-2021学年高二上学期第一次月考化学试题四川省自贡市江姐中学2020-2021学年高二上学期第一次月考化学试题海南省海口市灵山中学2020-2021学年高二上学期期中考试化学试题吉林油田第十一中学2020-2021学年高二上学期期中考试化学试题陕西省宝鸡市金台区2020-2021学年高二上学期期中考试化学(理)试题甘肃省武威市民勤县第一中学2020-2021学年高二上学期12月月考化学试题(理科)云南省玉溪第二中学2020-2021学年高二上学期期中质量检测化学试题(已下线)6.1.1 化学反应速率 练习-2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)吉林省吉林市江城中学2021届高三上学期12月月考化学试题陕西省宝鸡市千阳中学2019-2020学年高一下学期月考化学试题甘肃省武威市民勤县第四中学2020-2021学年高二下学期第一次月考化学(普通班)试题吉林省白城市第一中学2020-2021学年高一下学期期中考试化学试题内蒙古自治区乌拉特前旗第一中学2020-2021学年高一下学期4月月考化学试题(已下线)2.1.1 化学反应速率-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)考向21 化学反应速率及影响因素-备战2022年高考化学一轮复习考点微专题新疆阜康市第一中学2021-2022学年高二上学期第一次月考化学试题新疆阿克苏地区拜城县第一中学2021-2022学年高二上学期第一次月考化学试题河南省濮阳县实验高中2021-2022学年高二上学期第二次月考化学试题山西省天镇县实验中学2021-2022学年高二上学期期中考试化学试题广东省湛江市第二十一中学2021-2022学年高二上学期期中考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高二上学期期末考试化学试题(已下线)2.1.1 化学反应速率的表示方法(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)6.1.1 化学反应速率(第1课时 化学反应速率的概念和简单计算)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)江西省芦溪中学2021-2022学年高二上学期第二次段考化学(理)试题福建省福州黎明中学2021-2022学年高二上学期期中考试化学试题(已下线)第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)湖南省常德市鼎城区第一中学2021-2022学年高一下学期4月月考化学试题新疆叶城县第八中学2021-2022学年高二上学期期末考试化学(理)试题 陕西省西安市周至县第四中学2021-2022学年高一下学期期中考试化学试题黑龙江省饶河县高级中学2021-2022学年高一下学期期中考试化学试题福建省莆田华侨中学2022-2023学年高二上学期期中考试化学试题上海市闵行(文绮)中学2022-2023学年高二上学期期中考试化学试题广东省兴宁市沐彬中学2022-2023学年高二上学期期中考试化学试题广东省中山大学附属中学2022-2023学年高二上学期期中考试化学试题广东省开平市忠源纪念中学2021-2022学年高二上学期第二次月考化学试题新疆疏附县第一中学2022-2023学年高二上学期期中考试化学试题广西防城港市防城中学2021-2022学年高二上学期期中考试化学试题广西贺州市平桂管理区公会中学2021-2022学年上学期高二第二次月考化学(理)试题吉林省洮南市第一中学2021-2022学年高一下学期第一次月考化学试题广东省江门广雅中学2022-2023学年高二上学期期中考试化学试题福建省福州第十五中学2022-2023学年高二上学期11月线上限时训练化学试题湖北省宜昌市协作体2022-2023学年高一下学期期中考试化学试题河北省河北南宫中学2022-2023学年高一下学期5月月考化学试题内蒙古乌兰浩特市第四中学2022-2023学年高一下学期第三次月考化学试题作业(四) 化学反应速率作业(十三) 化学反应的历程和化学反应速率河北省沧州市东光县等三县联考2022-2023学年高一下学期4月月考化学试题第二章 第一节 化学反应速率 第1课时 化学反应速率(已下线)合格考汇编13化学反应速率和限度海南省省直辖县级行政单位澄迈县澄迈中学2023-2024学年高二上学期11月期中化学试题



