吉林省长春汽车经济技术开发区第六中学2020-2021学年高二上学期月考化学试题
吉林
高二
阶段练习
2020-11-04
429次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学
一、单选题 添加题型下试题
| A.食品、蔬菜贮存在冰箱或冰柜里 |
| B.家用铁锅、铁铲等餐具保持干燥 |
| C.制造蜂窝煤时加入生石灰 |
| D.把块状煤碾成粉状再燃烧 |
【知识点】 影响化学反应速率的因素
 ,若反应速率分别用
,若反应速率分别用 、
、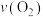 、
、 、
、 表示,则正确的关系式是
表示,则正确的关系式是A.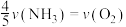 | B.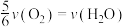 |
C.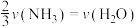 | D.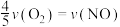 |
【知识点】 化学反应速率与化学计量数之间的关系解读
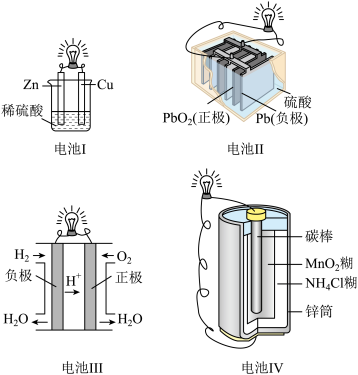
| A.电池Ⅰ中锌是正极 |
| B.电池Ⅱ是一次性电池 |
| C.电池Ⅲ工作时,氢气发生还原反应 |
| D.电池Ⅳ工作时,电子由锌通过导线流向碳棒 |
【知识点】 原电池
| A.能自发进行的反应一定能迅速发生 |
| B.非自发进行的反应一定不可能发生 |
| C.能自发进行的反应实际可能没有发生 |
D.常温下发生反应2H2O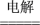 2H2↑ + O2↑,说明常温下水的分解反应是自发反应 2H2↑ + O2↑,说明常温下水的分解反应是自发反应 |
【知识点】 化学反应自发过程解读 反应进行方向判据的应用解读
| A.增大压强,活化分子百分数增多,化学反应速率一定增大 |
| B.升高温度,活化分子百分数不一定增大,化学反应速率一定增大 |
| C.增大反应物浓度,活化分子百分数增加,化学反应速率增大 |
| D.使用正催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大 |
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B.H2、I2(g)、HI混合气体加压后颜色变深 |
| C.红棕色的NO2加压后颜色先变深再变浅 |
| D.实验室用排饱和食盐水的方法收集氯气 |
A | B | C | D |
|
|
|
|
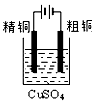
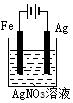
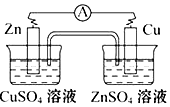
铜的精炼 | 铁上镀银 | 防止Fe被腐蚀 | 构成铜锌原电池 |
| A.A | B.B | C.C | D.D |
【知识点】 金属的电化学腐蚀与防护 原电池概念及组成 电解原理的应用
| A.0.32 mol·L-1·s-1 | B.0.16 mol·L-1·s-1 |
| C.1.6 mol·L-1·s-1 | D.0.8 mol·L-1·s-1 |
| 选项 | 强电解质 | 弱电解质 | 非电解质 |
| A | NaCl | HCl | CO2 |
| B | NaHCO3 | NH3·H2O | CCl4 |
| C | BaCO3 | Ba(OH)2 | Cu |
| D | H2SO4 | NaOH | C2H5OH |
| A.A | B.B | C.C | D.D |
 2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,
2Z(g)+W(g)(正反应为放热反应)的反应过程。若使a曲线变为b曲线,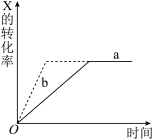
| A.加入催化剂 | B.增大Y的浓度 |
| C.降低温度 | D.增大体系压强 |
| A.20mL3mol·L-1的X溶液 | B.20mL2mol·L-1的X溶液 |
| C.10mL4mol·L-1的X溶液 | D.10mL2mol·L-1的X溶液 |
【知识点】 物质的量浓度的基础计算解读 浓度对化学反应速率的影响解读

| A.在此构想的物质循环中太阳能最终转化为化学能 |
| B.此循环过程中热能转化成为化学能 |
| C.此循环过程有利于节能环保 |
| D.此循环过程中没有发生氧化还原反应 |
【知识点】 氧化还原反应定义、本质及特征解读 能量的相互转化
 ,恒容时,温度升高,H2浓度减小,下列说法
,恒容时,温度升高,H2浓度减小,下列说法| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率增大,正反应速率减小 |
D.该反应的化学方程式为CO+H2O CO2+H2 CO2+H2 |
 CH3OH(g)达到平衡后,若只改变某一条件,下列示意图正确的是
CH3OH(g)达到平衡后,若只改变某一条件,下列示意图正确的是A.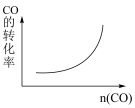 | B.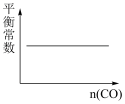 |
C. | D. |
【知识点】 化学平衡常数的影响因素及应用解读
 cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是
cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是 | A.反应速率增大 | B.W的体积分数降低 |
| C.N的转化率提高 | D.平衡向右移动 |
【知识点】 压强对化学平衡移动的影响解读
 2C(g),反应过程混合物中C%与温度关系如下图,下列说法正确的是
2C(g),反应过程混合物中C%与温度关系如下图,下列说法正确的是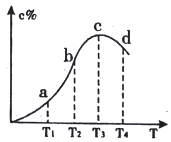
| A.正反应速率: v(c)>v(d)>v(b) | B.化学平衡常数: K(d)>K(c) |
| C.由c向d变化时,v(正)<v(逆) | D.该可逆反应的正反应为吸热反应 |
【知识点】 化学平衡图像分析
 该电池工作时,下列说法错误的是
该电池工作时,下列说法错误的是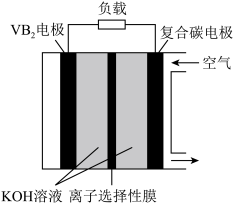
| A.负载通过0.04 mol电子时,有0.224 L(标准状况)O2参与反应 |
| B.正极区溶液的pH降低、负极区溶液的pH升高 |
C.电池总反应为 |
| D.电流由复合碳电极经负载、VB2电极、KOH溶液回到复合碳电极 |
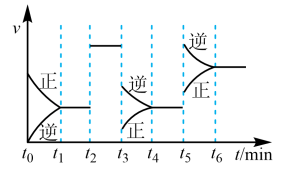
| A.t2时使用了催化剂 | B.t3时采取减小反应体系压强的措施 |
| C.t5时采取升温的措施 | D.反应在t6时刻,SO3体积分数最大 |
【知识点】 影响化学反应速率的因素 化学平衡的移动及其影响因素
 2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是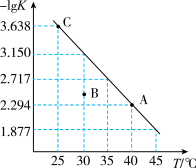
| A.C 点对应状态的平衡常数 K(C)=10-3.638 |
| B.该反应的ΔH>0 |
| C.混合气体的平均相对分子质量不变时,该反应一定达到平衡状态 |
D.30℃时,B 点对应状态的  < < |
【知识点】 化学平衡常数的影响因素及应用解读
 。25℃时,
。25℃时, 醋酸溶液中存在下述关系:
醋酸溶液中存在下述关系: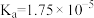 ,是该温度下醋酸的电离平衡常数
,是该温度下醋酸的电离平衡常数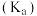 。下列说法正确的是
。下列说法正确的是A.向该溶液中滴加几滴浓盐酸,平衡逆向移动, 减小 减小 |
B.向该溶液中加少量 固体,平衡正向移动 固体,平衡正向移动 |
C.该温度下 醋酸溶液 醋酸溶液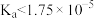 |
D.升高温度, 增大, 增大, 变大 变大 |
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A.相同条件下在冰醋酸中,硝酸是这四种酸中最弱的酸 |
| B.在冰醋酸中,这四种酸都没有完全电离 |
C.在冰醋酸中,硫酸的电离方程式为H2SO4⇌H++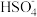 、 、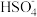 ⇌H++ ⇌H++ |
| D.电解质的强弱与所处的溶剂无关 |

| A.图Ⅰ是加入适当催化剂的变化情况 | B.图Ⅱ是扩大容器体积的变化情况 |
| C.图Ⅲ是升高温度的变化情况 | D.图Ⅲ是增大压强的变化情况 |
 和SO
和SO 。下列关于该装置的说法
。下列关于该装置的说法
| A.SO2通入阳极,该电极上发生氧化反应 |
| B.物质A为硫酸 |
C.阴极的电极反应为NO-5e-+6H+=NH +H2O +H2O |
| D.(NH4)2SO4可作为肥料 |
 CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按ω=
CH2=CHCH2Cl(g)+HCl(g)。在一定压强下,按ω= 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、ω的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的是( )
)与温度(T)、ω的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的是( )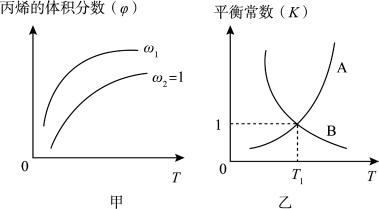
| A.图甲中ω1>1 |
| B.图乙中,线A表示正反应的平衡常数 |
| C.在恒容容器中进行,压强不变时反应达到平衡状态 |
| D.当温度为T1、ω=2时,Cl2的转化率约为33.3% |
 MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:| 反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2)/mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
下列说法正确的是( )
| A.0~2min内的平均速率为v(CO)=0.6mol/(L·min) |
| B.4min后,平衡移动的原因可能是向容器中加入了2.2mol的SO2 |
| C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应 |
| D.其他条件不变,若起始时容器中MgSO4、CO均为1.0mol,则平衡时n(SO2)>0.6mol |
二、填空题 添加题型下试题
(1)写出Na2S2O3溶液与稀硫酸反应的化学方程式
(2)写出甲烷燃料电池碱性环境中的负极反应方程式
(3)写出酸性高锰酸钾溶液与H2C2O4反应的离子方程式
(4)向K2Cr2O7溶液中滴加少量浓硫酸,溶液橙色加深,写出解释该现象的离子方程式
(5)写出碳酸的电离方程式
三、解答题 添加题型下试题
I.甲组同学,为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图A、B所示的实验。请回答下列问题:
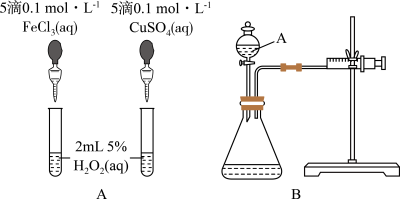
(1)定性比较:图A可通过观察
(2)定量比较:如图B所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
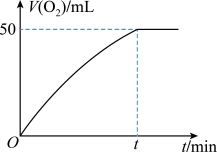
(3)将0.1mol MnO2粉末加入到50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。计算H2O2的初始物质的量浓度
Ⅱ.乙组同学按照如图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。

(1)实验原理:硫代硫酸钠溶液与稀硫酸反应。
(2)实验目的:
装置A,探究浓度对化学反应速率的影响;装置B,探究
(3)通过A、B装置,分别进行了三组实验,数据记录如下,并经分析得出相关结论:
| 实验组号 | 温度/℃ | Na2S2O3溶液 | H2SO4 | 加入H2O的体积/mL | 出现沉淀所需时间/s | ||
| 体积 /mL | 浓度(mol•L−1) | 体积/mL | 浓度/(mol•L−1) | ||||
| I | 0 | 5 | 0.1 | 10 | 0.1 | 5 | 8 |
| Ⅱ | 0 | 5 | 0.1 | 5 | 0.1 | 10 | 12 |
| Ⅲ | 30 | 5 | 0.1 | 5 | 0.1 | 10 | 4 |
②2H2(g)+O2(g)=2H2O(1)ΔH2=-571.6kJ/mol
③2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1)ΔH3=-2599.2kJ/mol
则由C(石墨)和H2(g)反应生成1molC2H2(g)的焓变ΔH=
Ⅱ.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:| T/°C | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为
(2)
a.容器中压强不变
b.混合气体中c(CO)不变
c.容器中气体平均摩尔质量不变
d.1molH-H键断裂的同时断裂2molH-O键
(3)某温度下,在2L的密闭容器中,加入1molCO2和1molH2充分反应达平衡时,CO平衡浓度为0.25mol/L,试通过计算判断此时的温度为
(4)在830℃温度下,某时刻测得c(CO2)=0.5mol/L,c(H2O)=0.5mol/L,c(CO)=1mol/L,c(H2)=1.5mol/L,则此时v(正)
(5)在830℃温度下,向该平衡体系中再充入一定量的氢气,CO2的转化率
A.16.67% B.22.2% C.33.3% D.36.8%
Ⅲ.CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
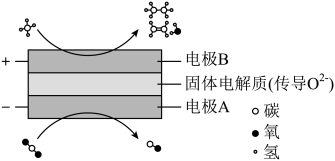
根据图示,写出阴极的反应式为
试卷分析
试卷题型(共 28题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 影响化学反应速率的因素 | |
| 2 | 0.65 | 化学反应速率与化学计量数之间的关系 | |
| 3 | 0.65 | 原电池 | |
| 4 | 0.65 | 化学反应自发过程 反应进行方向判据的应用 | |
| 5 | 0.85 | 碰撞理论及活化能 | |
| 6 | 0.65 | 化学平衡的移动 浓度对化学平衡移动的影响 压强对化学平衡移动的影响 勒夏特列原理的应用 | |
| 7 | 0.85 | 金属的电化学腐蚀与防护 原电池概念及组成 电解原理的应用 | |
| 8 | 0.85 | 化学反应的速率 化学反应速率计算 | |
| 9 | 0.94 | 强电解质与弱电解质 | |
| 10 | 0.85 | 催化剂对化学反应速率的影响 化学平衡的移动及其影响因素 与转化率变化有关图像的分析 | |
| 11 | 0.85 | 物质的量浓度的基础计算 浓度对化学反应速率的影响 | |
| 12 | 0.65 | 氧化还原反应定义、本质及特征 能量的相互转化 | |
| 13 | 0.85 | 温度对化学平衡移动的影响 压强对化学平衡移动的影响 化学平衡常数的概念及表达方式 | |
| 14 | 0.85 | 化学平衡常数的影响因素及应用 | |
| 15 | 0.65 | 压强对化学平衡移动的影响 | |
| 16 | 0.65 | 化学平衡图像分析 | |
| 17 | 0.65 | 原电池电极反应式书写 新型电池 原电池有关计算 | |
| 18 | 0.65 | 影响化学反应速率的因素 化学平衡的移动及其影响因素 | |
| 19 | 0.65 | 化学平衡常数的影响因素及应用 | |
| 20 | 0.65 | 弱电解质的电离平衡 电离平衡常数及影响因素 浓度对电离平衡的影响 | |
| 21 | 0.85 | 弱电解质的电离平衡 弱电解质在水溶液中的电离平衡 电离平衡常数及影响因素 | |
| 22 | 0.65 | 化学平衡的移动及其影响因素 化学平衡图像分析 化学反应速率与化学平衡的综合应用 | |
| 23 | 0.85 | 电解池电极反应式及化学方程式的书写与判断 电解原理的应用实验 | |
| 24 | 0.4 | 化学平衡常数的影响因素及应用 化学平衡题中基于图表数据的相关计算 | |
| 25 | 0.65 | 化学反应速率计算 等效平衡理论的综合应用 化学平衡常数的影响因素及应用 化学平衡题中基于图表数据的相关计算 | |
| 二、填空题 | |||
| 26 | 0.65 | 氧化还原反应方程式的配平 浓度对化学平衡移动的影响 弱电解质的电离方程式 烃燃料电池 | |
| 三、解答题 | |||
| 27 | 0.65 | 测定某些反应的反应速率 外因对化学反应速率影响的综合分析 | 实验探究题 |
| 28 | 0.65 | 盖斯定律的应用 化学平衡状态的判断方法 化学平衡常数的有关计算 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |