真题
1 . 为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计和结论都正确的是
| 选项 | 影响因素 | 方案设计 | 现象 | 结论 |
| A | 浓度 | 向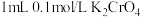 溶液中加入 溶液中加入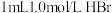 溶液 溶液 | 黄色溶液变橙色 | 增大反应物浓度,平衡向正反应方向移动 |
| B | 压强 | 向恒温恒容密闭玻璃容器中充入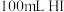 气体,分解达到平衡后再充入 气体,分解达到平衡后再充入 | 气体颜色不变 | 对于反应前后气体总体积不变的可逆反应,改变压强平衡不移动 |
| C | 温度 | 将封装有 和 和 混合气体的烧瓶浸泡在热水中 混合气体的烧瓶浸泡在热水中 | 气体颜色变深 | 升高温度,平衡向吸热反应方向移动 |
| D | 催化剂 | 向 乙酸乙酯中加入 乙酸乙酯中加入  溶液,水浴加热 溶液,水浴加热 | 上层液体逐渐减少 | 使用合适的催化剂可使平衡向正反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
真题
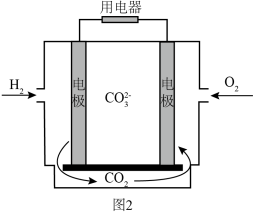
2 . 氢是清洁能源,硼氢化钠( )是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为
)是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为 ,
, )
)

请回答:
(1)该反应能自发进行的条件是_______。
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是_______。
(3)为加速 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比
水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比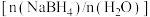 之间的关系,结果如图1所示。请解释ab段变化的原因
之间的关系,结果如图1所示。请解释ab段变化的原因_______ 。_______ 。该电池以 恒定电流工作14分钟,消耗
恒定电流工作14分钟,消耗 体积为
体积为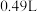 ,故可测得该电池将化学能转化为电能的转化率为
,故可测得该电池将化学能转化为电能的转化率为_______ 。[已知:该条件下 的摩尔体积为
的摩尔体积为 ;电荷量
;电荷量 电流
电流 时间
时间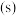 ;
;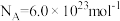 ;
;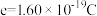 。]
。] )再生为
)再生为 。(已知:
。(已知: 是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比
是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比 计算方法;当
计算方法;当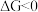 时,反应能自发进行。)
时,反应能自发进行。)
I.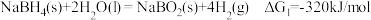
II.
III.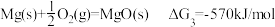
请书写一个方程式表示 再生为
再生为 的一种制备方法,并注明
的一种制备方法,并注明
_______ 。(要求:反应物不超过三种物质;氢原子利用率为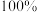 。)
。)
 )是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为
)是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为 ,
, )
)
请回答:
(1)该反应能自发进行的条件是_______。
| A.高温 | B.低温 | C.任意温度 | D.无法判断 |
| A.升高溶液温度 | B.加入少量异丙胺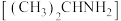 |
C.加入少量固体硼酸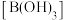 | D.增大体系压强 |
 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比
水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比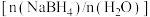 之间的关系,结果如图1所示。请解释ab段变化的原因
之间的关系,结果如图1所示。请解释ab段变化的原因
 恒定电流工作14分钟,消耗
恒定电流工作14分钟,消耗 体积为
体积为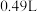 ,故可测得该电池将化学能转化为电能的转化率为
,故可测得该电池将化学能转化为电能的转化率为 的摩尔体积为
的摩尔体积为 ;电荷量
;电荷量 电流
电流 时间
时间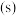 ;
;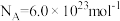 ;
;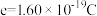 。]
。]
 )再生为
)再生为 。(已知:
。(已知: 是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比
是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比 计算方法;当
计算方法;当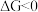 时,反应能自发进行。)
时,反应能自发进行。)I.
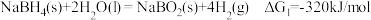
II.

III.
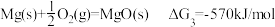
请书写一个方程式表示
 再生为
再生为 的一种制备方法,并注明
的一种制备方法,并注明
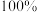 。)
。)
您最近一年使用:0次
2024·全国·高考真题
3 . 我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数为4。下列叙述错误的是
纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数为4。下列叙述错误的是
 纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数为4。下列叙述错误的是
纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能力。W、X、Y、Z的原子序数依次增加,且W、X、Y属于不同族的短周期元素。W的外层电子数是其内层电子数的2倍,X和Y的第一电离能都比左右相邻元素的高。Z的M层未成对电子数为4。下列叙述错误的是| A.W、X、Y、Z四种元素的单质中Z的熔点最高 |
B.在X的简单氢化物中X原子轨道杂化类型为 |
C.Y的氢氧化物难溶于NaCl溶液,可以溶于 溶液 溶液 |
D. 中 中 提供电子对与 提供电子对与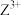 形成配位键 形成配位键 |
您最近一年使用:0次
昨日更新
|
1852次组卷
|
4卷引用:2024年新课标卷理综化学试题(网络回忆版,内容不完整)
(已下线)2024年新课标卷理综化学试题(网络回忆版,内容不完整)2024年新课标卷理科综合化学试题(已下线)2024年高考化学真题完全解读(新课标卷)河南省驻马店市新蔡县第一高级中学2023-2024学年高二下学期6月月考化学试题
名校
解题方法
4 . 下列离子方程式正确的是
A.二元弱碱 与足量稀硫酸溶液反应: 与足量稀硫酸溶液反应: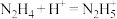 |
B. 溶于浓氨水: 溶于浓氨水: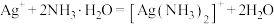 |
C. 溶液中加 溶液中加 溶液: 溶液: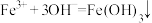 |
D. 溶液吸收 溶液吸收 : : |
您最近一年使用:0次
昨日更新
|
123次组卷
|
2卷引用:广西桂林市第十八中学2023-2024学年高三下学期5月月考化学试卷
真题
解题方法
5 . 按物质组成分类,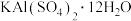 属于
属于
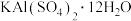 属于
属于| A.酸 | B.碱 | C.盐 | D.混合物 |
您最近一年使用:0次
6 . 某种离子型铁的氧化物晶胞如图所示,它由A、B两种正方体单元构成,且两种正方体单元中氧离子的空间位置相同。通过Li+嵌入或脱嵌该晶胞的棱心和体心,可将该晶体设计为纳米硅基锂电池的正极材料 (m、n为正整数),已知:脱嵌率=
(m、n为正整数),已知:脱嵌率=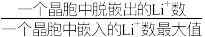 ×100%。
×100%。
 (m、n为正整数),已知:脱嵌率=
(m、n为正整数),已知:脱嵌率=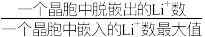 ×100%。
×100%。
| A.当Li+嵌入晶胞体心和所有棱心时,该锂电池正极材料的化学式为LiFe6O8 |
| B.若该锂电池正极材料中n(Fe2+):n(Fe3+)=5:7,则Li+的脱嵌率为75% |
C.该锂电池充电时阳极发生的反应为 |
| D.该锂电池放电时,每转移2mol e-,正极材料增重14g |
您最近一年使用:0次
名校
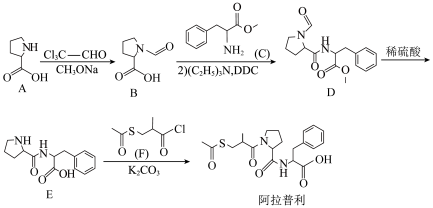
7 . 阿拉普利是治疗高血压的长效药,合成路线如图:
(1)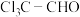 中官能团的名称为
中官能团的名称为_______ 。
(2)写出A→B的化学方程式:_______ ;制备E的过程中,设计A→B的目的是_______ 。
(3)E和F反应生成阿拉普利的反应类型是_______ ; 的作用是
的作用是_______ 。
(4)阿拉普利分子中含有_______ 个手性碳原子。
(5)C的芳香族同分异构体中,同时具备下列条件的结构有_______ 种(不包括立体异构体)。
①既能发生银镜反应,又能发生水解反应
②苯环上只有两种取代基,且其中一个为
其中核磁共振氢谱显示有五组峰,且峰面积比为6:2:2:2:1的结构简式为_______ 。
(1)
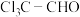 中官能团的名称为
中官能团的名称为(2)写出A→B的化学方程式:
(3)E和F反应生成阿拉普利的反应类型是
 的作用是
的作用是(4)阿拉普利分子中含有
(5)C的芳香族同分异构体中,同时具备下列条件的结构有
①既能发生银镜反应,又能发生水解反应
②苯环上只有两种取代基,且其中一个为

其中核磁共振氢谱显示有五组峰,且峰面积比为6:2:2:2:1的结构简式为
您最近一年使用:0次
昨日更新
|
374次组卷
|
4卷引用:2024届河南省周口市高三5月全真模拟理科综合试题-高中化学
名校
解题方法
8 . 下列离子方程式与所给事实相符的是
A.向水杨酸溶液中加入碳酸氢钠: |
B.碱性锌锰电池工作时正极反应: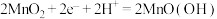 |
C.将少量 通入NaClO溶液中: 通入NaClO溶液中: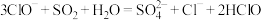 |
D.向乙二醇溶液中加入足量酸性高锰酸钾溶液: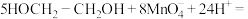  |
您最近一年使用:0次
真题
解题方法
9 . 一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)

A.电池总反应为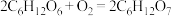 |
| B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用 |
| C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入 |
D.两电极间血液中的 在电场驱动下的迁移方向为b→a 在电场驱动下的迁移方向为b→a |
您最近一年使用:0次
10 . 钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。 ,其他金属离子不沉淀,即认为完全分离。
,其他金属离子不沉淀,即认为完全分离。
已知:①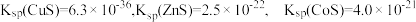 。
。
②以氢氧化物形式沉淀时,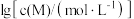 和溶液
和溶液 的关系如图所示。
的关系如图所示。
(1)“酸浸”前,需将废渣磨碎,其目的是_____ 。
(2)“酸浸”步骤中, 发生反应的化学方程式是
发生反应的化学方程式是_____ 。
(3)假设“沉铜”后得到的滤液中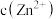 和
和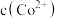 均为
均为 ,向其中加入
,向其中加入 至
至 沉淀完全,此时溶液中
沉淀完全,此时溶液中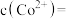
_____  ,据此判断能否实现
,据此判断能否实现 和
和 的完全分离
的完全分离_____ (填“能”或“不能”)。
(4)“沉锰”步骤中,生成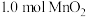 ,产生
,产生 的物质的量为
的物质的量为_____ 。
(5)“沉淀”步骤中,用 调
调 ,分离出的滤渣是
,分离出的滤渣是_____ 。
(6)“沉钴”步骤中,控制溶液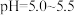 ,加入适量的
,加入适量的 氧化
氧化 ,其反应的离子方程式为
,其反应的离子方程式为_____ 。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是_____ 。
 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
 ,其他金属离子不沉淀,即认为完全分离。
,其他金属离子不沉淀,即认为完全分离。已知:①
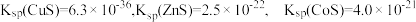 。
。②以氢氧化物形式沉淀时,
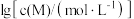 和溶液
和溶液 的关系如图所示。
的关系如图所示。
(1)“酸浸”前,需将废渣磨碎,其目的是
(2)“酸浸”步骤中,
 发生反应的化学方程式是
发生反应的化学方程式是(3)假设“沉铜”后得到的滤液中
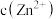 和
和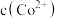 均为
均为 ,向其中加入
,向其中加入 至
至 沉淀完全,此时溶液中
沉淀完全,此时溶液中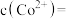
 ,据此判断能否实现
,据此判断能否实现 和
和 的完全分离
的完全分离(4)“沉锰”步骤中,生成
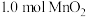 ,产生
,产生 的物质的量为
的物质的量为(5)“沉淀”步骤中,用
 调
调 ,分离出的滤渣是
,分离出的滤渣是(6)“沉钴”步骤中,控制溶液
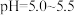 ,加入适量的
,加入适量的 氧化
氧化 ,其反应的离子方程式为
,其反应的离子方程式为(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是
您最近一年使用:0次



