名校
解题方法
1 . 在标准状况下4.48LH2与0.3molCl2混合见光反应后,再全部通入100mLNaOH溶液中,恰好完全反应,无剩余气体逸出。则:
①氢气与氯气混合反应后气体的总体积为__________ L。
②原氢氧化钠溶液浓度为_____ mol/L。
①氢气与氯气混合反应后气体的总体积为
②原氢氧化钠溶液浓度为
您最近一年使用:0次
2020-12-01更新
|
211次组卷
|
2卷引用:安徽省蚌埠第三中学2020-2021学年高一上学期第一次月考化学试题
2 . (1)已知98%的硫酸物质的量浓度为18.4mol/L,则49%的硫酸物质的量浓度______ 9.2mol/L(>,=,<);
(2)3.2gCH4中约含有_________ 个分子、在标准状况下所占的体积约为__________ L;
(3)12gFeX2中含有0.2molX原子,则X原子的摩尔质量为___________ 。
(2)3.2gCH4中约含有
(3)12gFeX2中含有0.2molX原子,则X原子的摩尔质量为
您最近一年使用:0次
名校
3 . 铜制品受到腐蚀后变成铜绿[Cu2(OH)2CO3]。
(1)可以将腐蚀了的铜制品放入烧杯,加入足量的稀盐酸除去铜绿,实验的现象为________________________________________ ,反应的离子反应方程式为 ___________________________ ,现对a g部分被腐蚀的铜(不含其它物质)进行实验,刚好用去b g质量分数为c%的盐酸,则未腐蚀的铜的质量为____________ g。(列出算式即可)
(2)也可以利用加热法测定铜的腐蚀程度,在惰性气氛中对m g的铜制品进行实验,铜绿加热发生分解反应,生成几种氧化物,则反应方程式为_____________________________ ,充分反应后固体剩余n g,则该铜制品中铜绿占比为___________ %。(列出算式即可)
(1)可以将腐蚀了的铜制品放入烧杯,加入足量的稀盐酸除去铜绿,实验的现象为
(2)也可以利用加热法测定铜的腐蚀程度,在惰性气氛中对m g的铜制品进行实验,铜绿加热发生分解反应,生成几种氧化物,则反应方程式为
您最近一年使用:0次
名校
4 . 某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目的分子”,他们设计了如下实验装置并记录相关实验数据。实验装置:

部分实验数据:
请回答下列问题:
(1)4分钟时H2物质的量是______ mol。
(2)该温度下,气体摩尔体积是________ 。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是________ mL。
(4)根据以上实验得出如下结论,其中不正确的是________ 。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L

部分实验数据:
| 温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
| 30℃ | 101 kPa | 0 | 300g | 0 | 0 |
| 30℃ | 101 kPa | 4分钟 | 298.2g | 1.243 L |
请回答下列问题:
(1)4分钟时H2物质的量是
(2)该温度下,气体摩尔体积是
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是
(4)根据以上实验得出如下结论,其中不正确的是
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L
您最近一年使用:0次
解题方法
5 . 将5.6g铁粉与足量的稀盐酸充分反应,所得溶液的体积为10mL。试计算:
(1)生成氢气的体积______ (标准状况)。
(2)所得溶液中金属阳离子的物质的量浓度_______ 。(上述计算均要求写出计算过程)
(1)生成氢气的体积
(2)所得溶液中金属阳离子的物质的量浓度
您最近一年使用:0次
解题方法
6 . 在密闭容器中,将 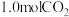 与
与 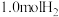 混合加热到800 ℃,发生下列反应:
混合加热到800 ℃,发生下列反应: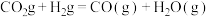 ,一段时间后该反应达到平衡,测得CO的物质的量为
,一段时间后该反应达到平衡,测得CO的物质的量为  。求:
。求:
 达到平衡时
达到平衡时 的体积(标准状况下)
的体积(标准状况下)___ 和该反应的化学平衡常数___ ;
 达到平衡后向该平衡体系中通入
达到平衡后向该平衡体系中通入 水蒸气,达到新的平衡状态时,求
水蒸气,达到新的平衡状态时,求  的物质的量分数。
的物质的量分数。___
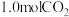 与
与 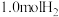 混合加热到800 ℃,发生下列反应:
混合加热到800 ℃,发生下列反应: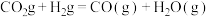 ,一段时间后该反应达到平衡,测得CO的物质的量为
,一段时间后该反应达到平衡,测得CO的物质的量为  。求:
。求: 达到平衡时
达到平衡时 的体积(标准状况下)
的体积(标准状况下) 达到平衡后向该平衡体系中通入
达到平衡后向该平衡体系中通入 水蒸气,达到新的平衡状态时,求
水蒸气,达到新的平衡状态时,求  的物质的量分数。
的物质的量分数。
您最近一年使用:0次
名校
解题方法
7 . (1)系统命名法命名A、B、C、D四种物质:
A. :
:________ ; B. :
:________ ;
C. :
:_______ ; D.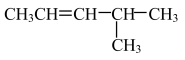 :
:________ ;
(2)某有机物0.3克完全燃烧后生成224毫升(标准状况)二氧化碳和0.18克水。已知该物质的蒸气对氢气的相对密度为30,试求:
①有机物的分子式___________ 。
②试写出该有机物可能的两个结构简式___________ ;_____________ 。
A.
 :
: :
:C.
 :
: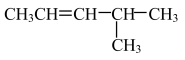 :
:(2)某有机物0.3克完全燃烧后生成224毫升(标准状况)二氧化碳和0.18克水。已知该物质的蒸气对氢气的相对密度为30,试求:
①有机物的分子式
②试写出该有机物可能的两个结构简式
您最近一年使用:0次
名校
解题方法
8 . (1)8.8gCO2在标准状况下的体积为____ L,其中含氧原子的物质的量为___ mol。
(2)4.8g甲烷(CH4)与标准状况下_____ L氨气(NH3)含有相同数目的氢原子。
(3)等质量的SO2和SO3所含的硫原子个数之比为______ ,同温同压下的密度之比为______ 。
(4)19g某二价金属的氯化物ACl2中含有0.4molCl-,A的相对原子质量是________ 。
(5)用10mL的0.1mol·L -1BaCl2溶液恰好可使相同体积的Al2(SO4)3和K2SO4两种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则两种硫酸盐溶液的物质的量浓度之比是________ 。
(2)4.8g甲烷(CH4)与标准状况下
(3)等质量的SO2和SO3所含的硫原子个数之比为
(4)19g某二价金属的氯化物ACl2中含有0.4molCl-,A的相对原子质量是
(5)用10mL的0.1mol·L -1BaCl2溶液恰好可使相同体积的Al2(SO4)3和K2SO4两种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则两种硫酸盐溶液的物质的量浓度之比是
您最近一年使用:0次
2020-11-17更新
|
361次组卷
|
3卷引用:安徽省蚌埠田家炳中学、蚌埠五中2020-2021学年高一上学期期中考试化学试题
安徽省蚌埠田家炳中学、蚌埠五中2020-2021学年高一上学期期中考试化学试题江西省吉安市第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题05 物质的量-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
解题方法
9 . 可逆反应①x(g)+2Y(g) 2z(g)、②2M(g)
2z(g)、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡时有关物理量的变化如下图:反应前,隔板左边加入1mol X和2mol Y,隔板右边加入2mol M;开始时隔板在“3”处,平衡(1)时隔板在“2.8”处,平衡(II)时隔板在“2.6”处。
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡时有关物理量的变化如下图:反应前,隔板左边加入1mol X和2mol Y,隔板右边加入2mol M;开始时隔板在“3”处,平衡(1)时隔板在“2.8”处,平衡(II)时隔板在“2.6”处。
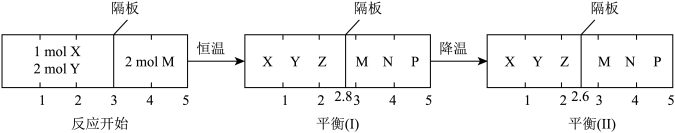
(1)求平衡(I)时,体系的压强与反应开始时体系压强之比______ 。
(2)求平衡(II)时X的转化率______ 。
 2z(g)、②2M(g)
2z(g)、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡时有关物理量的变化如下图:反应前,隔板左边加入1mol X和2mol Y,隔板右边加入2mol M;开始时隔板在“3”处,平衡(1)时隔板在“2.8”处,平衡(II)时隔板在“2.6”处。
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡时有关物理量的变化如下图:反应前,隔板左边加入1mol X和2mol Y,隔板右边加入2mol M;开始时隔板在“3”处,平衡(1)时隔板在“2.8”处,平衡(II)时隔板在“2.6”处。
(1)求平衡(I)时,体系的压强与反应开始时体系压强之比
(2)求平衡(II)时X的转化率
您最近一年使用:0次
名校
10 . 国家标准规定酿造食醋总酸含量不得低于3.5g/100mL,为测定某品牌市售醋酸的浓度,用移液管移取25mL,定容至250mL。取25.00mL溶液,用0.2000 mol∙L−1 NaOH标准溶液滴定至终点。重复实验,数据如下:
已知:常温下,Ka(CH3COOH)=1.8×10−5, =2.236
=2.236
(1)该市售醋酸的含量为______ g/100mL
(2)该市售醋酸c(H+)约等于______ (保留小数点后一位)
| 序号 | 滴定前读数/mL | 滴定终点读数/mL |
| 1 | 0.00 | 19.98 |
| 2 | 2.40 | 22.40 |
| 3 | 1.54 | 21.56 |
已知:常温下,Ka(CH3COOH)=1.8×10−5,
 =2.236
=2.236(1)该市售醋酸的含量为
(2)该市售醋酸c(H+)约等于
您最近一年使用:0次
2020-11-14更新
|
475次组卷
|
8卷引用:安徽省蚌埠第三中学2020-2021学年高二上学期1月教学质量检测化学试题
安徽省蚌埠第三中学2020-2021学年高二上学期1月教学质量检测化学试题浙江省杭州学军中学2021届高三上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高三上】【期中】【HD-LP423】【化学】(已下线)【浙江新东方】120(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)



