名校
解题方法
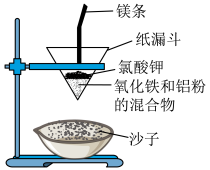
1 . 化学变化总是伴随着能量的变化。“铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如图装置实现:_______ 。
(2)实验中能观察到的现象有(例举两点):_______ 。
(3)可表示铝与氧化铁反应的热效应的图是_______ 。
(2)实验中能观察到的现象有(例举两点):
(3)可表示铝与氧化铁反应的热效应的图是
A.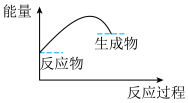 B.
B. C.
C.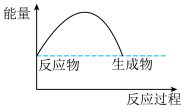
| A.铝还原性较强 | B.锰、钒熔点高 |
| C.铝能形成多种合金 | D.反应放出大量热 |
您最近一年使用:0次
解题方法
2 . Fe/Fe3O4复合物是一种高密度磁记录材料,磁记录材料有记录和存储信息的功能。制备该材料的一种流程如下:
Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为_____ 。该“反应”中通入氩气的原因_____ 。
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
3.已知参加反应的FeCl2溶液浓度为lmol·L−1。由题给信息分析,25℃时,当pH<2时,Fe/Fe3O4产率极低的原因_____ 。
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。_____ 。
通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
6.从绿色化学角度评价该循环过程(说一点)。_____

Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
| A.SO2 | B.铁粉 |
| C.KSCN溶液 | D.KSCN溶液新制氯水 |
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。

通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
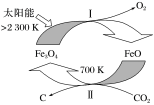
| A.反应物 | B.中间产物 | C.催化剂 | D.产物 |
您最近一年使用:0次
3 . 实验室需配制 的
的 溶液,请回答下列问题:
溶液,请回答下列问题:
(1)需用托盘天平称取 固体的总质量为
固体的总质量为_______ g。
(2)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是_______ (填序号)。
①称量(用托盘天平) ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
(3)配制 的
的 溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有_______ 、_______ 。
(4)配制 的
的 溶液,配制过程中所涉及的下列相关操作正确的是
溶液,配制过程中所涉及的下列相关操作正确的是_______ 。
 的
的 溶液,请回答下列问题:
溶液,请回答下列问题:(1)需用托盘天平称取
 固体的总质量为
固体的总质量为(2)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是
①称量(用托盘天平) ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
(3)配制
 的
的 溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有(4)配制
 的
的 溶液,配制过程中所涉及的下列相关操作正确的是
溶液,配制过程中所涉及的下列相关操作正确的是a. 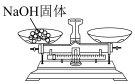 b.
b. 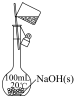 c.
c. 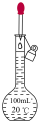 d.
d.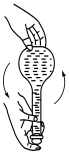
A.用蒸馏水溶解 固体后,立即转入容量瓶中 固体后,立即转入容量瓶中 |
B.称量 固体时,将药品和砝码放反了 固体时,将药品和砝码放反了 |
| C.定容时俯视刻度线 |
| D.定容后发现溶液的凹液面最低点高于刻度线,用胶头滴管将多余的液体吸出 |
您最近一年使用:0次
解题方法
4 . 小明同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。
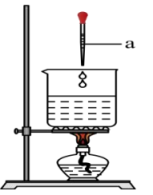
根据所学知识回答下列问题:
(1)仪器a的名称为___________ 。
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为___________ ,反应类型为___________ (填基本反应类型)。
②证明有 胶体生成的方法是
胶体生成的方法是___________ 。(写出具体操作步骤)
③若小明同学制备出的液体呈浑浊状,则可能造成的原因是___________ (任写一种)。
(3)写出下列反应的离子方程式:
①锌和稀盐酸反应制氢气:___________ 。
②大理石和稀盐酸反应制 :
:___________ 。

根据所学知识回答下列问题:
(1)仪器a的名称为
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为
②证明有
 胶体生成的方法是
胶体生成的方法是③若小明同学制备出的液体呈浑浊状,则可能造成的原因是
(3)写出下列反应的离子方程式:
①锌和稀盐酸反应制氢气:
②大理石和稀盐酸反应制
 :
:
您最近一年使用:0次
名校
解题方法
5 . 图是氮循环的一部分:
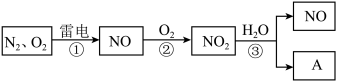
(1)通常状况下,NO2的颜色是_______ 。
(2)反应②的化学方程式是_______ 。
(3)NO2易溶于水,并与水发生化学反应。该反应中,还原剂是_______ 。
(4)化合物A的化学式是_______ 。
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应: 。当生成1molN2时,被氧化的CO为
。当生成1molN2时,被氧化的CO为_______ mol。

(1)通常状况下,NO2的颜色是
(2)反应②的化学方程式是
(3)NO2易溶于水,并与水发生化学反应。该反应中,还原剂是
(4)化合物A的化学式是
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:
 。当生成1molN2时,被氧化的CO为
。当生成1molN2时,被氧化的CO为
您最近一年使用:0次
名校
6 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液(有效成分 );②
);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸(
酒精;⑧过氧乙酸( );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号)。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用导致游泳池藻类快速生长,池水变绿,写出该反应的化学方程式___________ 。
(3)实验室可用 溶液配制消毒液。
溶液配制消毒液。
①需要用托盘天平称量 固体的质量为
固体的质量为___________  ;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有
;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有___________ 。
②下列情况会导致所配制溶液浓度偏高的是___________ (填标号)。
a.称量时所用的砝码生锈
b.移液时,有少量液体浅出
c.定容时,俯视刻度线
(4)高铁酸钠 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为___________ 。用 代替
代替 处理饮用水的优点是
处理饮用水的优点是___________ (只答一条即可)。
 );②
);② (在水中一部分可以电离出阴、阳离子);③漂白粉;④
(在水中一部分可以电离出阴、阳离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦
;⑥碘酒;⑦ 酒精;⑧过氧乙酸(
酒精;⑧过氧乙酸( );⑨高铁酸钠(
);⑨高铁酸钠( )。回答下列问题:
)。回答下列问题:(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用导致游泳池藻类快速生长,池水变绿,写出该反应的化学方程式
(3)实验室可用
 溶液配制消毒液。
溶液配制消毒液。①需要用托盘天平称量
 固体的质量为
固体的质量为 ;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有
;在配制过程中,除托盘天平、烧杯、玻璃棒、胶头滴管外还必需的玻璃仪器有②下列情况会导致所配制溶液浓度偏高的是
a.称量时所用的砝码生锈
b.移液时,有少量液体浅出
c.定容时,俯视刻度线
(4)高铁酸钠
 是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体:
是一种新型净水剂。高铁酸钠在水中可以发生如下反应并生成胶体: 。当反应转移电子的数目是
。当反应转移电子的数目是 时,生成标准状况下
时,生成标准状况下 的体积约为
的体积约为 代替
代替 处理饮用水的优点是
处理饮用水的优点是
您最近一年使用:0次
解题方法
7 . 在中国古代,硫酸被炼丹术士称为“绿矾油”。这是因为生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧后,釜中逸出刺激性气味的气体,同时有油状液体流出,残留固体呈红棕色。

(1)请写出煅烧绿矾过程中发生反应的化学方程式:
①___________ ;
②___________ 。
(2)化学探究小组的同学用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去),其中b为干燥的试管。下列关于该反应说法正确的是___________。

(1)请写出煅烧绿矾过程中发生反应的化学方程式:
①
②
(2)化学探究小组的同学用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去),其中b为干燥的试管。下列关于该反应说法正确的是___________。
A.若将反应后的气体通入 溶液中,产生的沉淀为 溶液中,产生的沉淀为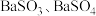 |
B.b中产物用紫色石蕊试液即可检验出其中 和 和 |
C.为检验反应的气态生成物是 ,试管c中应加入的试剂为NaOH溶液 ,试管c中应加入的试剂为NaOH溶液 |
| D.b中所得到的硫酸的质量分数为29.5% |
您最近一年使用:0次
8 . 研究氮及其化合物的性质具有极为重要的意义。
(1)NOx是汽车尾气中的主要污染物之一、NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_______ ,此反应的氧化产物是_______ ,1molNO2反应转移电子_______ mol。
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,写出实验室用固体加热制取NH3的化学方程式为_______ ,用5.35g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为_______ L。(NH4Cl的摩尔质量为53.5g·mol-1)
(3)实验室可以用铜与稀硝酸制取NO,写出该反应的离子方程式:_______ 。
(4)工业上采用氨氧化法制取硝酸,写出在催化剂作用下氨气与氧气反应的化学方程式:__ 。
(5)工业合成氨原料气氢气通过碳与水蒸气反应制取。已知1mol水蒸气和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ 。写出该反应的热化学方程式______ 。
(1)NOx是汽车尾气中的主要污染物之一、NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,写出实验室用固体加热制取NH3的化学方程式为
(3)实验室可以用铜与稀硝酸制取NO,写出该反应的离子方程式:
(4)工业上采用氨氧化法制取硝酸,写出在催化剂作用下氨气与氧气反应的化学方程式:
(5)工业合成氨原料气氢气通过碳与水蒸气反应制取。已知1mol水蒸气和炽热的焦炭反应生成水煤气,反应吸热131.4 kJ 。写出该反应的热化学方程式
您最近一年使用:0次
名校
解题方法
9 . 元素周期表在学习、研究和生产实践中有很重要的作用。下表显示了元素周期表中的短周期,①~⑤代表5种元素。
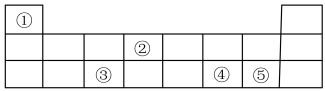
(1)②在元素周期表中的位置是______ 。
(2)⑤的最高价氧化物对应的水化物的化学式是______ 。
(3)①和⑤可形成共价化合物,用电子式表示其形成过程______ 。
(4)①分别与④、⑤形成的化合物中,稳定性强的是______ (用化学式表示)。
(5)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是______ 。
(6)元素 的原子结构示意图为
的原子结构示意图为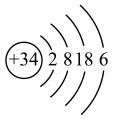 。下列推断错误的是______(填序号)。
。下列推断错误的是______(填序号)。
(7) 在一定条件下可与
在一定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为
溶液反应,生成一种正盐和水,该正盐化学式为______ 。

(1)②在元素周期表中的位置是
(2)⑤的最高价氧化物对应的水化物的化学式是
(3)①和⑤可形成共价化合物,用电子式表示其形成过程
(4)①分别与④、⑤形成的化合物中,稳定性强的是
(5)③和④分别形成的最高价氧化物对应的水化物可以发生反应,离子方程式是
(6)元素
 的原子结构示意图为
的原子结构示意图为 。下列推断错误的是______(填序号)。
。下列推断错误的是______(填序号)。A. 位于第四周期、与④同主族 位于第四周期、与④同主族 | B. 的最低负化合价为-2价 的最低负化合价为-2价 |
C. 具有还原性 具有还原性 | D.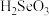 的酸性强于 的酸性强于 |
(7)
 在一定条件下可与
在一定条件下可与 溶液反应,生成一种正盐和水,该正盐化学式为
溶液反应,生成一种正盐和水,该正盐化学式为
您最近一年使用:0次
解题方法
10 . 以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵[(NH4)3Fe(C6H5O7)2]。
(1)Fe基态核外电子排布式为___________ ;[Fe(H2O)6]2+中与Fe2+配位原子是___________ (填元素符号)。
(2)NH3分子中氮原子的杂化轨道类型为___________ ,分子空间构型为___________ ;NH3分子H—N—H键角比PH3分子中的H—P—H键角大,请解释其原因___________
(3)与NH 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
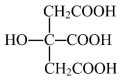
(4)柠檬酸的结构简式如图。1 mol 柠檬酸分子中碳原子与氧形成的σ键的数目为___________ mol,π键的数目为___________ mol。
(1)Fe基态核外电子排布式为
(2)NH3分子中氮原子的杂化轨道类型为
(3)与NH
 互为等电子体的一种分子为
互为等电子体的一种分子为(4)柠檬酸的结构简式如图。1 mol 柠檬酸分子中碳原子与氧形成的σ键的数目为

您最近一年使用:0次



