1 . Ⅰ.汽车让人们的生活越来越便捷。请回答以下问题:
(1)汽车尾气主要含有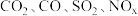 等物质,是造成城市空气污染的主要因素之一;
等物质,是造成城市空气污染的主要因素之一;  和
和 反应生成
反应生成 的能量变化如下图所示,则该反应的热化学方程式为
的能量变化如下图所示,则该反应的热化学方程式为_______________ 。 可作氧化剂,用于氧化火箭推进器中的强还原剂肼
可作氧化剂,用于氧化火箭推进器中的强还原剂肼 ,释放大量的能量,其热化学方程式为:
,释放大量的能量,其热化学方程式为:
①若进行上述反应,放出热量为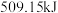 ,则转移电子数目为
,则转移电子数目为_______________  。
。
②已知: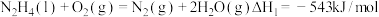

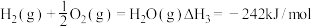
若用氟气代替二氧化氮作氧化剂,则反应释放能量更多,请写出液态肼和氟气反应的热化学方程式:_______________ 。
(3)汽车受到猛烈碰撞时,安全气囊内的 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。
Ⅱ.污染性气体的处理:
(4)以 溶液作为吸收剂,控制溶液的
溶液作为吸收剂,控制溶液的 ,将二氧化硫和一氧化氮转化为
,将二氧化硫和一氧化氮转化为 和
和 去除。
去除。
①在酸性 溶液中,
溶液中, 氧化
氧化 的离子方程式为
的离子方程式为_______________ 。
② 的去除率高于
的去除率高于 的可能原因是
的可能原因是_______________ 。(任写一条)
(5)将 的混合气体共
的混合气体共 (已换算为标准状况,下同)通入水中,气体体积减小
(已换算为标准状况,下同)通入水中,气体体积减小 ,若将该混合气体与一定量
,若将该混合气体与一定量 混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是
混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是_______________ (填序号)。
①混合气体中 的体积分数为
的体积分数为
②所得硝酸溶液物质的量浓度为
③用足量 溶液可将该混合气体完全吸收
溶液可将该混合气体完全吸收
④消耗的 在标准状况下的体积为
在标准状况下的体积为
(1)汽车尾气主要含有
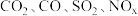 等物质,是造成城市空气污染的主要因素之一;
等物质,是造成城市空气污染的主要因素之一;  和
和 反应生成
反应生成 的能量变化如下图所示,则该反应的热化学方程式为
的能量变化如下图所示,则该反应的热化学方程式为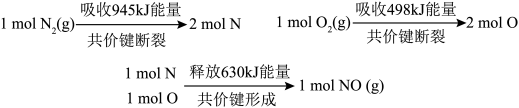
 可作氧化剂,用于氧化火箭推进器中的强还原剂肼
可作氧化剂,用于氧化火箭推进器中的强还原剂肼 ,释放大量的能量,其热化学方程式为:
,释放大量的能量,其热化学方程式为:
①若进行上述反应,放出热量为
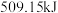 ,则转移电子数目为
,则转移电子数目为 。
。②已知:
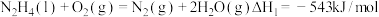

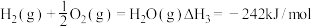
若用氟气代替二氧化氮作氧化剂,则反应释放能量更多,请写出液态肼和氟气反应的热化学方程式:
(3)汽车受到猛烈碰撞时,安全气囊内的
 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示,下列说法错误的是___________。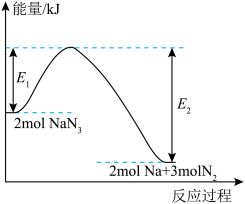
A. 属于离子化合物 属于离子化合物 |
B. 的分解反应属于吸热反应 的分解反应属于吸热反应 |
C. 表示 表示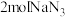 固体具有的能量 固体具有的能量 |
D. 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 |
Ⅱ.污染性气体的处理:
(4)以
 溶液作为吸收剂,控制溶液的
溶液作为吸收剂,控制溶液的 ,将二氧化硫和一氧化氮转化为
,将二氧化硫和一氧化氮转化为 和
和 去除。
去除。①在酸性
 溶液中,
溶液中, 氧化
氧化 的离子方程式为
的离子方程式为②
 的去除率高于
的去除率高于 的可能原因是
的可能原因是(5)将
 的混合气体共
的混合气体共 (已换算为标准状况,下同)通入水中,气体体积减小
(已换算为标准状况,下同)通入水中,气体体积减小 ,若将该混合气体与一定量
,若将该混合气体与一定量 混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是
混合通入水中,所有气体能被完全吸收得到硝酸溶液,下列说法错误的是①混合气体中
 的体积分数为
的体积分数为
②所得硝酸溶液物质的量浓度为

③用足量
 溶液可将该混合气体完全吸收
溶液可将该混合气体完全吸收④消耗的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
2 . 某化学兴趣小组用如图所示装置探究铜与浓硝酸的反应.下列说法错误的是
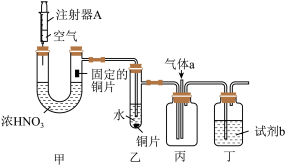
| A.合理控制注射器A可以实现甲处U形管内反应的发生与停止 |
B.乙中可以观察到铜片逐渐溶解,说明发生了反应 |
C.气体a和试剂b可选择 和 和 溶液 溶液 |
D.若甲中反应生成的还原产物只有 由 由 和 和 组成的混合物,则甲中共有 组成的混合物,则甲中共有 铜片参与反应 铜片参与反应 |
您最近一年使用:0次
2024-05-30更新
|
19次组卷
|
2卷引用:内蒙古赤峰市部分学校2023-2024学年高一下学期5月期中联考化学试题
解题方法
3 . 海洋约占地球表面积的71%,其中除含 、
、 外,还含有
外,还含有 、
、 、
、 等多种离子,海水资源具有十分巨大的开发潜力。下图是某工厂对海水资源综合利用的示意图。据图回答问题:
等多种离子,海水资源具有十分巨大的开发潜力。下图是某工厂对海水资源综合利用的示意图。据图回答问题:_______ 。
(2)电解饱和食盐水得到的 、
、 、
、 均是重要的化工原料,可由上述三种物质制备的产品有
均是重要的化工原料,可由上述三种物质制备的产品有_______ 。
A.盐酸 B.“84”消毒液(主要成分 ) C.硫酸
) C.硫酸
(3) 通入含有
通入含有 的母液中生成
的母液中生成 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(4)吸收塔中发生反应的化学方程式为: ,在该反应中
,在该反应中 做
做_______ (填“氧化剂”或“还原剂”)。
(5)利用上述原理每制得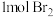 ,理论上需要消耗
,理论上需要消耗_______ 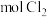 。
。
 、
、 外,还含有
外,还含有 、
、 、
、 等多种离子,海水资源具有十分巨大的开发潜力。下图是某工厂对海水资源综合利用的示意图。据图回答问题:
等多种离子,海水资源具有十分巨大的开发潜力。下图是某工厂对海水资源综合利用的示意图。据图回答问题: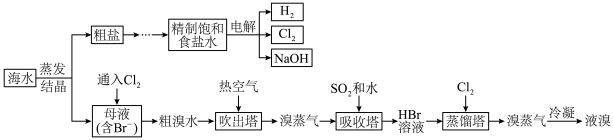
(2)电解饱和食盐水得到的
 、
、 、
、 均是重要的化工原料,可由上述三种物质制备的产品有
均是重要的化工原料,可由上述三种物质制备的产品有A.盐酸 B.“84”消毒液(主要成分
 ) C.硫酸
) C.硫酸(3)
 通入含有
通入含有 的母液中生成
的母液中生成 ,该反应的离子方程式为
,该反应的离子方程式为(4)吸收塔中发生反应的化学方程式为:
 ,在该反应中
,在该反应中 做
做(5)利用上述原理每制得
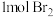 ,理论上需要消耗
,理论上需要消耗 。
。
您最近一年使用:0次
名校
4 . 研究表明,光催化剂Ti-CNO对 与氧化苯乙烯环加成生成碳酸苯乙烯酯表现出优异的光热催化活性和稳定性,其反应机理如图所示(部分微粒未标出):
与氧化苯乙烯环加成生成碳酸苯乙烯酯表现出优异的光热催化活性和稳定性,其反应机理如图所示(部分微粒未标出):
 与氧化苯乙烯环加成生成碳酸苯乙烯酯表现出优异的光热催化活性和稳定性,其反应机理如图所示(部分微粒未标出):
与氧化苯乙烯环加成生成碳酸苯乙烯酯表现出优异的光热催化活性和稳定性,其反应机理如图所示(部分微粒未标出):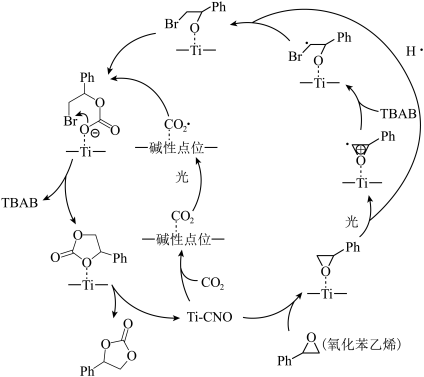
已知:TBAB的结构简式为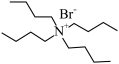 ;—Ph代表苯基。
;—Ph代表苯基。
A.氧化苯乙烯的分子式为 |
| B.TBAB中氮元素显+5价 |
C. 转化 转化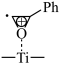 的过程中,碳氢极性键断裂 的过程中,碳氢极性键断裂 |
D.在“碱性点位”上 得电子发生还原反应 得电子发生还原反应 |
您最近一年使用:0次
2024-05-27更新
|
91次组卷
|
2卷引用:专题5 物质结构与性质 元素周期律-分子结构与性质
5 . 我国的冶金工业十分发达,钢铁年产量已达到十亿吨,占世界产量的一半以上,同时有色金属产量也超过了七千万吨。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为___________ 。
(2)铝与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ ;铝的化学性质较活泼,但在空气中不会完全锈蚀,其原因是___________ 。
(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为___________ ,当有 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为___________ 。
②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为___________ 。在碱性的废电解液中通入氯气可以将 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为___________ 。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为
(2)铝与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性
 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的
 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
您最近一年使用:0次
6 . 下列说法正确的是
| A.水的沸点高于硫化氢,这是由于水分子间存在氢键这种化学键 |
B.将氯气通入碘化钾溶液,可以生成碘单质,说明还原性: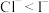 |
C.化学反应 是放热的氧化还原反应 是放热的氧化还原反应 |
D.核素 和 和 互为同位素,单质 互为同位素,单质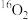 与 与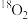 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
7 . SrCO3可用于生产纳米材料,常温下,以天青石矿(主要成分为SrSO4,含少量CaCO3、MgCO3、ZnCO3、Al2O3、Fe2O3及FeO等杂质)为原料制备SrCO3的流程如下: 、
、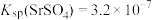 。
。
②该工艺条件下,有关金属离子开始沉淀和完全沉淀以及部分离子的氢氧化物开始溶解的pH见下表:
(1)“盐浸”时,为了提高锶的浸取率可以采取的措施是_______ (写一条即可),采用适当浓度Na2CO3溶液盐浸的目的是_______ (用离子方程式表示)。
(2)“酸浸”时加入H2O2的目的是_______ (用离子方程式表示)。
(3)“第一次调pH”时,需要调pH的范围是_______ ,当Al3+刚好完全沉淀时,溶液中Fe3+的浓度为_______ mol·L-1。
(4)“第三次调pH至12.5”后,需对反应液在95℃水浴中加热,并趁热过滤出“滤渣3”,趁热过滤的目的是_______ 。
(5)“沉锶”时,主要反应的离子方程式为_______ 。
(6)“系列操作”包括_______ (填操作名称)。

 、
、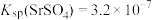 。
。②该工艺条件下,有关金属离子开始沉淀和完全沉淀以及部分离子的氢氧化物开始溶解的pH见下表:
| 金属离子 | Fe3+ | Al3+ | Zn2+ | Mg2+ |
| 开始沉淀的pH(c=1×10-2mol·L-1) | 2.1 | 4.2 | 6.0 | 10.4 |
| 完全沉淀的pH(c=1×10-5mol·L-1) | 4.1 | 5.2 | 8.0 | 12.4 |
| 氢氧化物沉淀开始溶解的pH | - | 7.8 | 10.05 | - |
(1)“盐浸”时,为了提高锶的浸取率可以采取的措施是
(2)“酸浸”时加入H2O2的目的是
(3)“第一次调pH”时,需要调pH的范围是
(4)“第三次调pH至12.5”后,需对反应液在95℃水浴中加热,并趁热过滤出“滤渣3”,趁热过滤的目的是
(5)“沉锶”时,主要反应的离子方程式为
(6)“系列操作”包括
您最近一年使用:0次
名校
解题方法
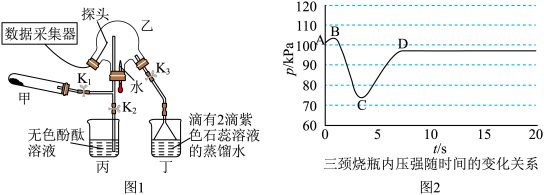
8 . 某化学兴趣小组利用图1装置(加热和夹持装置已省略)制备氨气并进行喷泉实验.
i.氨气的制备:打开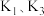 ,关闭
,关闭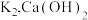 和
和 固体在甲处试管内反应生成
固体在甲处试管内反应生成 .
.
ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备 ,关闭
,关闭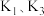 ,打开
,打开 ,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
请回答下列问题:___________________ ;丁处倒置漏斗的作用是______________ ;氨水中含有的分子有 、
、______________ .
(2)C→D过程中,三颈烧瓶中的现象为_____________ ; 能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为
能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为_____________ .
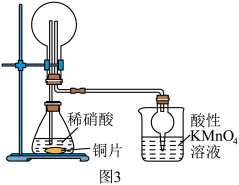
(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验.__________________________ .
②烧杯中发生反应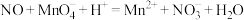 (未配平),该反应的氧化剂为
(未配平),该反应的氧化剂为__________ (填化学式),氧化产物和还原产物的物质的量之比为__________ (填最简整数比).
i.氨气的制备:打开
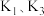 ,关闭
,关闭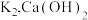 和
和 固体在甲处试管内反应生成
固体在甲处试管内反应生成 .
.ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备
 ,关闭
,关闭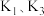 ,打开
,打开 ,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.请回答下列问题:
 、
、(2)C→D过程中,三颈烧瓶中的现象为
 能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为
能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验.
②烧杯中发生反应
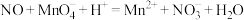 (未配平),该反应的氧化剂为
(未配平),该反应的氧化剂为
您最近一年使用:0次
2024-05-08更新
|
147次组卷
|
5卷引用:内蒙古赤峰市部分学校2023-2024学年高一下学期5月期中联考化学试题
名校
解题方法
9 . 铅酸蓄电池由于其技术成熟、安全性高、电压稳定及价格低廉等优势,在电池市场占据主导地位。以方铅可矿(PbS,含少量 )为原料制取
)为原料制取 的流程如图所示:
的流程如图所示:
(1)“酸浸”时温度一般控制在65~90℃,理由是___________ ,酸浸时发生反应的离子方程式为___________ 。
(2)从“酸浸”所得滤渣中回收的 ,可用于
,可用于___________ (任写两种)。
(3)“氧化”时参加反应的氧化剂与还原剂的物质的量之比为___________ 。
(4)若以100kg方铅矿(PbS的质量分数为70%)为原料,最终制得 59.75kg(假设反应过程中Pb无损失),则
59.75kg(假设反应过程中Pb无损失),则 的产率(产率
的产率(产率 )为
)为___________ (保留一位小数)。
(5)铅酸蓄电池为可充电电池,充放电时反应为 。
。
①放电时 电极的电极反应式为
电极的电极反应式为___________ 。
②充电时 电极发生
电极发生___________ (填“氧化”或“还原”)反应。
 )为原料制取
)为原料制取 的流程如图所示:
的流程如图所示: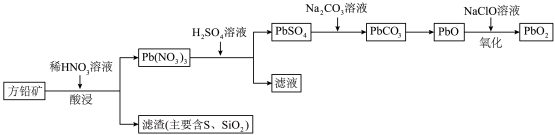
(1)“酸浸”时温度一般控制在65~90℃,理由是
(2)从“酸浸”所得滤渣中回收的
 ,可用于
,可用于(3)“氧化”时参加反应的氧化剂与还原剂的物质的量之比为
(4)若以100kg方铅矿(PbS的质量分数为70%)为原料,最终制得
 59.75kg(假设反应过程中Pb无损失),则
59.75kg(假设反应过程中Pb无损失),则 的产率(产率
的产率(产率 )为
)为(5)铅酸蓄电池为可充电电池,充放电时反应为
 。
。①放电时
 电极的电极反应式为
电极的电极反应式为②充电时
 电极发生
电极发生
您最近一年使用:0次
2024-05-07更新
|
150次组卷
|
4卷引用:内蒙古自治区兴安盟乌兰浩特第一中学2023-2024学年高一下学期期末考试化学试题
10 . 铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为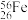 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向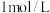 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
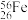 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向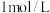 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近一年使用:0次



