名校
1 . 瑞典化学家舍勒最先用软锰矿和浓盐酸制出了一种黄绿色气体,并且知道了这种气体的某些性质,但他却认为,该气体是一种化合物。直到1810年,英国化学家戴维才确认这种气体是一种单质——氯气。
(1)下列关于氯气的叙述错误的是___________。
(2)下列氯化物中,既能由金属和氯气直接制取,又能由金属和盐酸直接制取的是___________。
(3)氯气可以用来给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是___________。
(4)今有 、
、 混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为
混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为___________ mL。为了确认剩余的气体是 还是
还是 ,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:
,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:
①测量剩佘气体的体积,如果剩余112mL,证明有 剩余;理由是
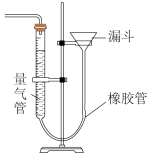
剩余;理由是___________ 。测量过程进行到末读数环节,忘记调节左右液面相平了,液面左高右低(具体如图所示),测得的气体体积___________ (填“偏大”、“偏小”或“不变”)。
②如果上述水洗液有漂白性,证明有 剩余;理由是
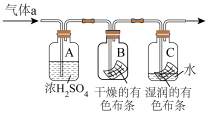
剩余;理由是___________ 。干燥的 没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是
没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是___________ 。不过这一装置设计有缺陷,体现在___________ 。
(5)①一定量的氢气在氯气中燃烧,火焰为___________ 色。
②所得混合物用100mL 的NaOH溶液(密度为
的NaOH溶液(密度为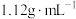 )恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是
)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是___________ mol;
③把NaCl和NaClO统一为通式 (
(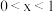 )。根据元素守恒,可知所得溶液中
)。根据元素守恒,可知所得溶液中 的物质的量为
的物质的量为___________ mol。
(1)下列关于氯气的叙述错误的是___________。
| A.氯气能溶于水 | B.氯气是黄绿色气体 |
| C.液氯是氯气的水溶液 | D.单质氯有气、液、固三种状态 |
(2)下列氯化物中,既能由金属和氯气直接制取,又能由金属和盐酸直接制取的是___________。
A. | B. | C. | D. |
(3)氯气可以用来给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是___________。
| A.石蕊 | B. | C.NaOH | D.NaCl |
(4)今有
 、
、 混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为
混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为 还是
还是 ,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:
,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:①测量剩佘气体的体积,如果剩余112mL,证明有
 剩余;理由是
剩余;理由是
②如果上述水洗液有漂白性,证明有
 剩余;理由是
剩余;理由是 没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是
没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是
(5)①一定量的氢气在氯气中燃烧,火焰为
②所得混合物用100mL
 的NaOH溶液(密度为
的NaOH溶液(密度为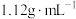 )恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是
)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是③把NaCl和NaClO统一为通式
 (
(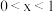 )。根据元素守恒,可知所得溶液中
)。根据元素守恒,可知所得溶液中 的物质的量为
的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 二氧化钛是一种重要的白色颜料,在涂料、催化、造纸等行业有广泛应用。从钛铁精矿 生产二氧化钛的一个重要化工流程称为“硫酸法”,如下所示。
生产二氧化钛的一个重要化工流程称为“硫酸法”,如下所示。

回答下列问题:
(1)钛酸亚铁 中
中 的化合价为
的化合价为___________ 。
(2)“酸解”时,将压缩空气从酸解槽底部送入可起到___________ 的作用;让物料在酸解槽中放置 的目的是
的目的是___________ 。
(3)“还原沉降”后溶液中主要含有 和阳离子
和阳离子___________ (两种);加入废铁屑除去 的目的是
的目的是___________ 。
(4)已知 溶解度随温度升高而增大,则“浓缩”得到
溶解度随温度升高而增大,则“浓缩”得到 晶体的结晶方式是
晶体的结晶方式是___________ 。
(5)“溶液C”水解产生 的离子方程式为
的离子方程式为___________ 。
(6)另一种生产 的短工序方法是“氯化法”:在
的短工序方法是“氯化法”:在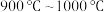 ,钛铁矿中加入少量碳粉,通入氯气对钛铁矿进行选择性氯化,生成
,钛铁矿中加入少量碳粉,通入氯气对钛铁矿进行选择性氯化,生成 、气态
、气态 和
和 。写出相应的化学方程式
。写出相应的化学方程式___________ 。
 生产二氧化钛的一个重要化工流程称为“硫酸法”,如下所示。
生产二氧化钛的一个重要化工流程称为“硫酸法”,如下所示。
回答下列问题:
(1)钛酸亚铁
 中
中 的化合价为
的化合价为(2)“酸解”时,将压缩空气从酸解槽底部送入可起到
 的目的是
的目的是(3)“还原沉降”后溶液中主要含有
 和阳离子
和阳离子 的目的是
的目的是(4)已知
 溶解度随温度升高而增大,则“浓缩”得到
溶解度随温度升高而增大,则“浓缩”得到 晶体的结晶方式是
晶体的结晶方式是(5)“溶液C”水解产生
 的离子方程式为
的离子方程式为(6)另一种生产
 的短工序方法是“氯化法”:在
的短工序方法是“氯化法”:在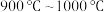 ,钛铁矿中加入少量碳粉,通入氯气对钛铁矿进行选择性氯化,生成
,钛铁矿中加入少量碳粉,通入氯气对钛铁矿进行选择性氯化,生成 、气态
、气态 和
和 。写出相应的化学方程式
。写出相应的化学方程式
您最近一年使用:0次
2024-01-06更新
|
326次组卷
|
3卷引用:上海市宜川中学2023-2024学年高三上学期期中考试卷(化学)
3 . 某实验小组为探究Cl-、I-、 的还原性强弱,甲同学设计实验如下:
的还原性强弱,甲同学设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量新制氯水溶液,溶液立刻变蓝;
实验②:向实验①的溶液中加入亚硫酸钠溶液,发现溶液蓝色褪去。
(1)根据上述实验现象,可以判断Cl-、I-、 还原性由强到弱的顺序为
还原性由强到弱的顺序为___________ 。
乙同学参考教科书知识,提出另一种实验方法,在碘化钾溶液中加入新制氯水后,将碘化钾溶液加入新制氯水后,将溶液转移入分液漏斗,并加入萃取剂,主要操作步骤如图:

(2)根据图中现象,该同学所采用的萃取剂可能是______。
(3)1、2、3三步实验操作中,不正确的是___________ (填“1”、“2”或“3”),理由是___________ 。
(4)在2图的分液漏斗中,下层液体呈___________ 色。
 的还原性强弱,甲同学设计实验如下:
的还原性强弱,甲同学设计实验如下:实验①:在淀粉碘化钾溶液中加入少量新制氯水溶液,溶液立刻变蓝;
实验②:向实验①的溶液中加入亚硫酸钠溶液,发现溶液蓝色褪去。
(1)根据上述实验现象,可以判断Cl-、I-、
 还原性由强到弱的顺序为
还原性由强到弱的顺序为乙同学参考教科书知识,提出另一种实验方法,在碘化钾溶液中加入新制氯水后,将碘化钾溶液加入新制氯水后,将溶液转移入分液漏斗,并加入萃取剂,主要操作步骤如图:

(2)根据图中现象,该同学所采用的萃取剂可能是______。
| A.酒精 | B.苯 | C.CCl4 | D.汽油 |
(3)1、2、3三步实验操作中,不正确的是
(4)在2图的分液漏斗中,下层液体呈
您最近一年使用:0次
名校
解题方法
4 . 无处不在的氧化还原反应
氧化还原反应是指在反应前后元素的氧化数有相应升降变化的化学反应。其由氧化反应和还原反应构成,并遵守电荷守恒定律。
氧化还原反应是一类非常重要的化学反应,广泛应用于工业、农业、生物、能源等领域。因此,认识氧化还原反应的实质与规律
(1)下表各组变化中,后者一定包括前者的是_____。
(2)下列关于氧化还原反应的叙述中正确的是_____。
(3)下列变化中,必须加入氧化剂才能发生的是_____。
(4)工业上制备84消毒液的一个重要反应为:Cl2+2NaOH═NaCl+NaClO+H2O。在此方程式中。氧化剂是_____ ,具有_____ 性:还原剂是_____ ,氧化产物是_____ 。
用单线桥法在下列给出的反应物中标出电子转移方向和数目。
Cl2+2NaOH_____
氧化还原反应是指在反应前后元素的氧化数有相应升降变化的化学反应。其由氧化反应和还原反应构成,并遵守电荷守恒定律。
氧化还原反应是一类非常重要的化学反应,广泛应用于工业、农业、生物、能源等领域。因此,认识氧化还原反应的实质与规律
(1)下表各组变化中,后者一定包括前者的是_____。
| A.氧化还原反应;分解反应 |
| B.置换反应;氧化还原反应 |
| C.氧化还原反应;化合反应 |
| D.分解反应;中和反应 |
(2)下列关于氧化还原反应的叙述中正确的是_____。
| A.失去电子的反应为还原反应 |
| B.含有氧元素的物质一定是氧化剂 |
| C.氧化剂得电子数目和还原剂失电子数目一定相等 |
| D.氧化剂和还原剂不可能是同一种物质 |
(3)下列变化中,必须加入氧化剂才能发生的是_____。
| A.SO2﹣S | B.I-﹣I2 | C.SO3﹣SO2 | D. |
(4)工业上制备84消毒液的一个重要反应为:Cl2+2NaOH═NaCl+NaClO+H2O。在此方程式中。氧化剂是
用单线桥法在下列给出的反应物中标出电子转移方向和数目。
Cl2+2NaOH
您最近一年使用:0次
名校
5 . Ⅰ.某研究性学习小组为了验证臭氧的氧化性强于氧气 ,设计了实验。
(1)a溶液是一种显色剂,用来检验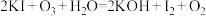 反应确有发生,a物质是
反应确有发生,a物质是___________ 。
(2)已知碘在酒精中的溶解度比在水中大得多,能否用酒精来萃取碘水中的碘___________ (填“能”或“不能”),其理由是___________ 。
(3)向碘水中加入适量的四氯化碳,充分振荡后,观察到的现象是___________。
(4)写出在臭氧消毒柜放电条件下产生 的化学方程式:
的化学方程式:___________ 。这是一个___________ (填“氧化还原”或“非氧化还原”)反应。
(5)在 氧化KI的反应中
氧化KI的反应中
①用单线桥法标出上述反应电子转移的方向和数目_________ 。
②若有9.6g 发生反应,则转移电子的物质的量为
发生反应,则转移电子的物质的量为___________ ,发生氧化反应的元素是___________ ;还原产物为___________ 。
Ⅱ.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如下:
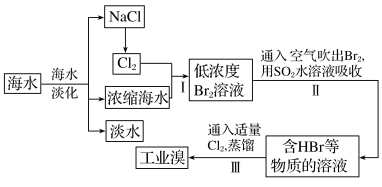
(6)步骤I获得 的反应的离子方程式为
的反应的离子方程式为___________
(7)步骤II用 水溶液吸收
水溶液吸收 ,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为___________ (若反应中生成2molHBr,则消耗lmol )。
)。
(8)根据上述反应可判断出 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是___________ 。
(1)a溶液是一种显色剂,用来检验
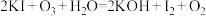 反应确有发生,a物质是
反应确有发生,a物质是(2)已知碘在酒精中的溶解度比在水中大得多,能否用酒精来萃取碘水中的碘
(3)向碘水中加入适量的四氯化碳,充分振荡后,观察到的现象是___________。
| A.溶液分层,上层紫红色,下层接近无色 |
| B.溶液不分层,溶液紫红色 |
| C.溶液分层,上层接近无色,下层紫红色 |
| D.溶液不分层,溶液黄色 |
(4)写出在臭氧消毒柜放电条件下产生
 的化学方程式:
的化学方程式:(5)在
 氧化KI的反应中
氧化KI的反应中
①用单线桥法标出上述反应电子转移的方向和数目
②若有9.6g
 发生反应,则转移电子的物质的量为
发生反应,则转移电子的物质的量为Ⅱ.海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如下:

(6)步骤I获得
 的反应的离子方程式为
的反应的离子方程式为(7)步骤II用
 水溶液吸收
水溶液吸收 ,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为
,使溴蒸气转化为氢溴酸以达到富集的目的,其反应的化学方程式为 )。
)。(8)根据上述反应可判断出
 、
、 、
、 三种物质氧化性由强到弱的顺序是
三种物质氧化性由强到弱的顺序是
您最近一年使用:0次
名校
6 . 肼(N2H4)又名联氨,是一种强还原性的高能物质,在航天、能源等领域有广泛应用。肼 分子结构如图所示。

(1)关于 N2H4 分子说法正确的是_______。
(2)N2H4 的相对分子质量与 CH2=CH2 接近,但沸点远高于 CH2=CH2,原因是_______。
(3)发射卫星时可用 N2H4 为燃料,N2O4 为助燃剂,这两种物质反应放出大量能量,生成无毒无害的物质。此过程中氧化剂与还原剂的物质的量之比为___________ 。
(4)实验室可用如下装置,在碱性条件下合成 N2H4:

①完成装置 B 中发生反应的离子方程式(化学计量数为 1 则省略):
i.___________ ;
ii. □NH3 + □ClO- = □N2H4 + □_______+ □_______;_________ 。
②装置 A 试管中的试剂为___________ ;仪器 a 的作用是___________ 。
③装置 C 中每生成 112 mL(折算至标准状况)气体,转移电子数目为___________ ; 仪器 b 的导管作用为___________ 。
④上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是___________ 。

(1)关于 N2H4 分子说法正确的是_______。
| A.只含有极性键的极性分子 | B.含有非极性键的极性分子 |
| C.只含有极性键的非极性分子 | D.有非极性键的非极性分子 |
(2)N2H4 的相对分子质量与 CH2=CH2 接近,但沸点远高于 CH2=CH2,原因是_______。
| A.N2H4 分子内可形成氢键 | B.N2H4 分子间可形成氢键 |
| C.N2H4 分子中共价键键能更大 | D.N2H4 分子能形成内盐 |
(3)发射卫星时可用 N2H4 为燃料,N2O4 为助燃剂,这两种物质反应放出大量能量,生成无毒无害的物质。此过程中氧化剂与还原剂的物质的量之比为
(4)实验室可用如下装置,在碱性条件下合成 N2H4:

①完成装置 B 中发生反应的离子方程式(化学计量数为 1 则省略):
i.
ii. □NH3 + □ClO- = □N2H4 + □_______+ □_______;
②装置 A 试管中的试剂为
③装置 C 中每生成 112 mL(折算至标准状况)气体,转移电子数目为
④上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是
您最近一年使用:0次
名校
解题方法
7 . 含氯化合物在生产生活中应用广泛。以下是一些含氯物质的制备。
工业上通过乙烯氯氧化法制备氯乙烯,工艺过程包括两步。完成下列填空:
(1)第一步,乙烯氯氧化
2CH2=CH2(g)+4HCl(g)+O2(g) 2ClCH2CH2Cl(g)+2H2O(g) (1)
2ClCH2CH2Cl(g)+2H2O(g) (1)
在一定温度下的2L密闭容器中,起始时气体总的物质的量为1mol,反应10min,气体总的物质的量变为原来的70%,则0~10min内,CH2=CH2的平均反应速率v=_______ 。
(2)第二步,脱氯化氢制氯乙烯
ClCH2CH2Cl(g) CH2=CHCl(g)+HCl(g) (2)
CH2=CHCl(g)+HCl(g) (2)
反应(2)的平衡常数K=_______ ,若其他条件相同,分别在P1、P2压强下发生反应(2),达到平衡时,ClCH2CH2Cl(g)的转化根据图像判断:P1_______ P2(选填“>”或“<”);反应(2)是_______ 反应(选填“放热”或“吸热”)。

(3)次氯酸钠是最普通的含氯消毒剂,可用氯气与氢氧化钠反应制取,产品中往往混有氯酸盐,发生的反应有:
Cl2+2NaOH=NaCl+NaClO+H2O
3Cl2+6NaOH(热溶液)=5NaCl+NaClO3+3H2O
上述反应都是放热反应,若要制备纯度较高的NaClO,须控制反应温度,写出一种可采取的措施_______ 。
(4)含氯消毒剂的消毒效果用有效氯表示,有效氯:含氯消毒剂与浓盐酸反应产生Cl2的质量与原消毒剂质量的比值。某品牌消毒液中含有质量分数10%的NaClO,计算该消毒液的有效氯为_______ 。
(5)次氯酸钠还可以用于去除废水的铵态氮。配平反应方程式:_______ 。
_______NH +_______ClO- =_______Cl-+_______H++_______N2↑+_______H2O
+_______ClO- =_______Cl-+_______H++_______N2↑+_______H2O
工业上通过乙烯氯氧化法制备氯乙烯,工艺过程包括两步。完成下列填空:
(1)第一步,乙烯氯氧化
2CH2=CH2(g)+4HCl(g)+O2(g)
 2ClCH2CH2Cl(g)+2H2O(g) (1)
2ClCH2CH2Cl(g)+2H2O(g) (1)在一定温度下的2L密闭容器中,起始时气体总的物质的量为1mol,反应10min,气体总的物质的量变为原来的70%,则0~10min内,CH2=CH2的平均反应速率v=
(2)第二步,脱氯化氢制氯乙烯
ClCH2CH2Cl(g)
 CH2=CHCl(g)+HCl(g) (2)
CH2=CHCl(g)+HCl(g) (2)反应(2)的平衡常数K=

(3)次氯酸钠是最普通的含氯消毒剂,可用氯气与氢氧化钠反应制取,产品中往往混有氯酸盐,发生的反应有:
Cl2+2NaOH=NaCl+NaClO+H2O
3Cl2+6NaOH(热溶液)=5NaCl+NaClO3+3H2O
上述反应都是放热反应,若要制备纯度较高的NaClO,须控制反应温度,写出一种可采取的措施
(4)含氯消毒剂的消毒效果用有效氯表示,有效氯:含氯消毒剂与浓盐酸反应产生Cl2的质量与原消毒剂质量的比值。某品牌消毒液中含有质量分数10%的NaClO,计算该消毒液的有效氯为
(5)次氯酸钠还可以用于去除废水的铵态氮。配平反应方程式:
_______NH
 +_______ClO- =_______Cl-+_______H++_______N2↑+_______H2O
+_______ClO- =_______Cl-+_______H++_______N2↑+_______H2O
您最近一年使用:0次
名校
解题方法
8 . 氮化铝(AlN)是一种高性能陶瓷材料。Al4C3和NH3反应可制备AlN:Al4C3+4NH3 4AlN+3CH4。
4AlN+3CH4。
(1)碳原子核外未成对电子数为_______ ,NH3的电子式为_______ 。
(2)氮化铝(AlN)和氮化硼(BN)晶体结构中,微粒之间均以共价键结合,且硬度大,熔点高,其中_______ (填AlN、BN)熔点更高。请用结构知识说明理由_______ 。
(3)上述反应中,部分元素的原子可形成相同电子层结构的简单离子,这些简单离子的半径从大到小的顺序是_______ 。
(4)下列事实能说明氮的非金属性比碳强的是_______。
(5)已知氨气也可以和氯气反应:8NH3+3Cl2=N2+6NH4Cl,该反应可以检查管道少量的氯气泄漏,下列叙述正确的是_______。
(6)写出Al投入NaOH溶液中的离子方程式_______ ,标准状况下,若生成的气体为5.6L,则转移的电子数目为_______ 。
(7)AlN在水中发生反应:AlN+4H2O Al(OH)3+NH3·H2O。实验表明,其他条件相同时,AlN分别在80℃和90℃下完全水解,反应后溶液的pH:pH(80℃)>pH(90℃)。用平衡原理说明pH(80℃)>pH(90℃)的原因(不考虑氢氧化铝的溶解和电离以及水的离子积的变化)
Al(OH)3+NH3·H2O。实验表明,其他条件相同时,AlN分别在80℃和90℃下完全水解,反应后溶液的pH:pH(80℃)>pH(90℃)。用平衡原理说明pH(80℃)>pH(90℃)的原因(不考虑氢氧化铝的溶解和电离以及水的离子积的变化) _______ 。
 4AlN+3CH4。
4AlN+3CH4。(1)碳原子核外未成对电子数为
(2)氮化铝(AlN)和氮化硼(BN)晶体结构中,微粒之间均以共价键结合,且硬度大,熔点高,其中
(3)上述反应中,部分元素的原子可形成相同电子层结构的简单离子,这些简单离子的半径从大到小的顺序是
(4)下列事实能说明氮的非金属性比碳强的是_______。
| A.硝酸是强酸,碳酸是弱酸 | B.氮的最高价为+5,碳的最高价为+4 |
| C.硝酸氧化性强,碳酸氧化性弱 | D.H3C—NH2中C—N键共用电子对偏向于N |
| A.可以检验氯气泄漏的现象是产生无色气体 |
| B.NH4Cl既是氧化产物又是还原产物 |
| C.被氧化的NH3占全部NH3的25% |
| D.转移0.3mol电子,生成6.72L氮气(标准状况下) |
(7)AlN在水中发生反应:AlN+4H2O
 Al(OH)3+NH3·H2O。实验表明,其他条件相同时,AlN分别在80℃和90℃下完全水解,反应后溶液的pH:pH(80℃)>pH(90℃)。用平衡原理说明pH(80℃)>pH(90℃)的原因(不考虑氢氧化铝的溶解和电离以及水的离子积的变化)
Al(OH)3+NH3·H2O。实验表明,其他条件相同时,AlN分别在80℃和90℃下完全水解,反应后溶液的pH:pH(80℃)>pH(90℃)。用平衡原理说明pH(80℃)>pH(90℃)的原因(不考虑氢氧化铝的溶解和电离以及水的离子积的变化)
您最近一年使用:0次
名校
9 . S2Cl2和SCl2均为重要的化工产品。
(1)二氯化二硫是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。S2Cl2的结构式为______ ,其化学键类型有______ (填“极性键”或“非极性键”)。
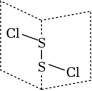
(2)S2Cl2中硫的化合价为______ ,S2Cl2分子中中心S原子的杂化轨道空间分布为______ ,S原子有______ 对孤电子对,S2Cl2是______ (填“极性”或“非极性”)分子。
(3)S2Cl2易发生水解反应,产生无色有刺激性气味的气体,同时生成淡黄色沉淀,该反应的化学方程式为______ 。
(4)实验室在111~140℃的温度下加热氯气和硫蒸气的混合物可制得S2Cl2,为检测所得物质中否纯净,某同学认为只要通过设计实验检测到有氯和硫两种元素存在,即可认为所得物质为纯净物的二氯化二硫。试从元素的价态分析并判断该同学的实验方案是否可行。______ 。
(1)二氯化二硫是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示。S2Cl2的结构式为

(2)S2Cl2中硫的化合价为
(3)S2Cl2易发生水解反应,产生无色有刺激性气味的气体,同时生成淡黄色沉淀,该反应的化学方程式为
(4)实验室在111~140℃的温度下加热氯气和硫蒸气的混合物可制得S2Cl2,为检测所得物质中否纯净,某同学认为只要通过设计实验检测到有氯和硫两种元素存在,即可认为所得物质为纯净物的二氯化二硫。试从元素的价态分析并判断该同学的实验方案是否可行。
您最近一年使用:0次
10 . 水是清洁、可持续的氢能来源。利用太阳能从水中获取氢气符合可持续发展的理念。“太阳能直接热分解水制氢”通过集中阳光产生2000K以上高温,促使 分解为
分解为 和
和 ;若温度进一步升高至5000K,
;若温度进一步升高至5000K, 与
与 会分解为气态原子。
会分解为气态原子。
(1) 分解过程中断裂的化学键属于
分解过程中断裂的化学键属于___________ 。
A.离子键 B.极性共价键 C.非极性共价键
(2)在相同条件下,同时存在如下两个过程:
i.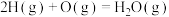 ii.
ii.
比较下列量的相对大小(均从选项中选择):①放出热量___________ ;②反应速率___________ 。
A.i>ii B.i=ii C.i<ii
“太阳能光催化分解水制氢”原理可以表示为: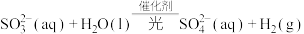 。
。
(3)已知 呈平面正三角形结构,推测
呈平面正三角形结构,推测 的立体构型为
的立体构型为___________ 。
A.平面正三角形 B.正四面体型 C.三角锥型
(4)能说明氯的非金属性比硫强的事实是___________。
(5) 与
与 结构相似,但
结构相似,但 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
(6)反应开始一段时间后,取出一定量溶液,写出检验溶液中 的操作方法:
的操作方法:________ 。
“太阳能热化学循环制氢”是将太阳能转化成化学能,通过多个化学过程产生 。如常见的铁氧化物循环制氢过程如图所示。
。如常见的铁氧化物循环制氢过程如图所示。
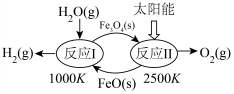
(7)写出反应I的化学方程式:___________ ;若该反应生成标准状况下 氢气,转移电子数目为
氢气,转移电子数目为___________ 。
(8)科学家想要用组成相似的钴氧化物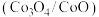 代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的
代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的 值随温度
值随温度 变化如图所示。
变化如图所示。
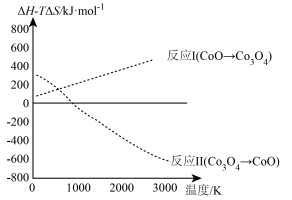
结合图像判断能否用钴氧化物代替铁氧化物进行热化学循环制氢?若可行,举出采用钴氧化物的一个优势;若不可行,说明理由___________ 。
(9)除了上述“直接热分解”、“光催化分解”和“热化学循环”外,请再设计一种利用太阳能从水中获取氢气的方法:___________ (简述即可,不必展开)。
 分解为
分解为 和
和 ;若温度进一步升高至5000K,
;若温度进一步升高至5000K, 与
与 会分解为气态原子。
会分解为气态原子。(1)
 分解过程中断裂的化学键属于
分解过程中断裂的化学键属于A.离子键 B.极性共价键 C.非极性共价键
(2)在相同条件下,同时存在如下两个过程:
i.
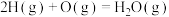 ii.
ii.
比较下列量的相对大小(均从选项中选择):①放出热量
A.i>ii B.i=ii C.i<ii
“太阳能光催化分解水制氢”原理可以表示为:
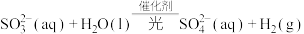 。
。(3)已知
 呈平面正三角形结构,推测
呈平面正三角形结构,推测 的立体构型为
的立体构型为A.平面正三角形 B.正四面体型 C.三角锥型
(4)能说明氯的非金属性比硫强的事实是___________。
A.溶解性: | B.氧化性: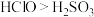 |
C.热稳定性: | D.酸性: |
(5)
 与
与 结构相似,但
结构相似,但 的沸点高于
的沸点高于 ,原因是
,原因是(6)反应开始一段时间后,取出一定量溶液,写出检验溶液中
 的操作方法:
的操作方法:“太阳能热化学循环制氢”是将太阳能转化成化学能,通过多个化学过程产生
 。如常见的铁氧化物循环制氢过程如图所示。
。如常见的铁氧化物循环制氢过程如图所示。
(7)写出反应I的化学方程式:
 氢气,转移电子数目为
氢气,转移电子数目为(8)科学家想要用组成相似的钴氧化物
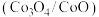 代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的
代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的 值随温度
值随温度 变化如图所示。
变化如图所示。
结合图像判断能否用钴氧化物代替铁氧化物进行热化学循环制氢?若可行,举出采用钴氧化物的一个优势;若不可行,说明理由
(9)除了上述“直接热分解”、“光催化分解”和“热化学循环”外,请再设计一种利用太阳能从水中获取氢气的方法:
您最近一年使用:0次



