名校
1 .  转化和利用是实现碳中和的有效途径,通过电催化或光催化将
转化和利用是实现碳中和的有效途径,通过电催化或光催化将 转化为
转化为 和
和 产物(如
产物(如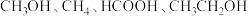 被认为是最有效的路径。请回答下列问题:
被认为是最有效的路径。请回答下列问题:
(1)二氧化碳可通过电催化合成 (如图1),生成的
(如图1),生成的 可直接用于燃料电池(如图2),相关原理如图所示。已知:图1和图2装置中的电解液均显酸性,质子交换膜只允许
可直接用于燃料电池(如图2),相关原理如图所示。已知:图1和图2装置中的电解液均显酸性,质子交换膜只允许 通过。
通过。___________ 能
___________ 能。
②图2装置中负极的电极反应式为___________
③图1装置发生的总反应与图2装置发生的总反应是否互为可逆反应?___________ (填“是”或“否”)。
(2)一定条件下,在催化剂表面将 转化为
转化为 ,其原理如图所示:
,其原理如图所示:___________ 。
(3)太阳能驱动以 为原料合成人工食品山梨糖,为克服自然光合作用的局限性提供了一条有前景的途径。
为原料合成人工食品山梨糖,为克服自然光合作用的局限性提供了一条有前景的途径。 中含有的官能团名称为
中含有的官能团名称为___________ 。
②山梨糖的分子式为___________ 。
(4)写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
 转化和利用是实现碳中和的有效途径,通过电催化或光催化将
转化和利用是实现碳中和的有效途径,通过电催化或光催化将 转化为
转化为 和
和 产物(如
产物(如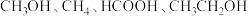 被认为是最有效的路径。请回答下列问题:
被认为是最有效的路径。请回答下列问题:(1)二氧化碳可通过电催化合成
 (如图1),生成的
(如图1),生成的 可直接用于燃料电池(如图2),相关原理如图所示。已知:图1和图2装置中的电解液均显酸性,质子交换膜只允许
可直接用于燃料电池(如图2),相关原理如图所示。已知:图1和图2装置中的电解液均显酸性,质子交换膜只允许 通过。
通过。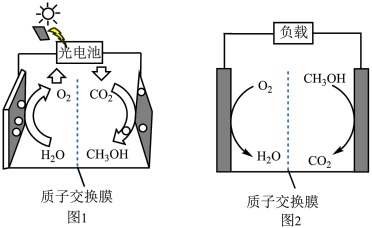

②图2装置中负极的电极反应式为
③图1装置发生的总反应与图2装置发生的总反应是否互为可逆反应?
(2)一定条件下,在催化剂表面将
 转化为
转化为 ,其原理如图所示:
,其原理如图所示:
(3)太阳能驱动以
 为原料合成人工食品山梨糖,为克服自然光合作用的局限性提供了一条有前景的途径。
为原料合成人工食品山梨糖,为克服自然光合作用的局限性提供了一条有前景的途径。 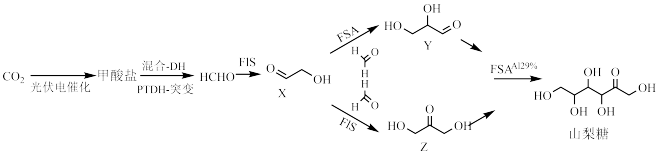
查阅资料: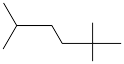 代表
代表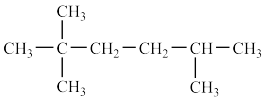 ,其中线表示化学键,线的端点、折点或交点表示碳原子,碳原子剩余的化合价用氢原子补足,这样的表示方法叫键线式,如图中
,其中线表示化学键,线的端点、折点或交点表示碳原子,碳原子剩余的化合价用氢原子补足,这样的表示方法叫键线式,如图中 代表
代表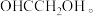
 中含有的官能团名称为
中含有的官能团名称为②山梨糖的分子式为
(4)写出
 与
与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
2024-07-04更新
|
84次组卷
|
2卷引用:河南省南阳市六校联考2023-2024学年高一下学期6月期末考试化学试题
2 . 硒酸( )及其盐可用于镀微裂纹铬电解液中,亦可用作镀铑的添加剂,其过程涉及如下反应:
)及其盐可用于镀微裂纹铬电解液中,亦可用作镀铑的添加剂,其过程涉及如下反应:
反应①: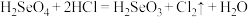
反应②: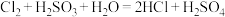
反应③: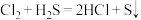
下列有关说法错误的是
 )及其盐可用于镀微裂纹铬电解液中,亦可用作镀铑的添加剂,其过程涉及如下反应:
)及其盐可用于镀微裂纹铬电解液中,亦可用作镀铑的添加剂,其过程涉及如下反应:反应①:
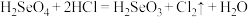
反应②:
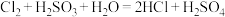
反应③:
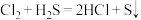
下列有关说法错误的是
A. 中Se的化合价为 中Se的化合价为 价 价 | B.反应①的还原产物是 |
C.氧化性: | D. 与 与 能发生反应 能发生反应 |
您最近一年使用:0次
2024-07-04更新
|
426次组卷
|
2卷引用:河南省濮阳市南乐县2023-2024学年高一下学期7月期末考试化学试题
解题方法
3 . 锗是半导体材料。以含锗废料(主要成分是 ,含少量FeO、SiO2、Ag2O和PbO等)为原料提取锗的流程如下:
,含少量FeO、SiO2、Ag2O和PbO等)为原料提取锗的流程如下: 时认为该离子沉淀完全。
时认为该离子沉淀完全。
② 。常温下,几种难溶电解质的溶度积数据如下:
。常温下,几种难溶电解质的溶度积数据如下:
请回答下列问题:
(1)“酸浸”之前,先粉碎含锗废料,其目的是_____ ;实验室中进行“灼烧”操作时,盛装固体的仪器是_____ (填名称)。
(2)试剂X可能是ZnO、Zn(OH) 2、ZnCO3、Zn(OH) 2CO3等,滤渣2的主要成分是_____ (填化学式)。
(3)“调pH”后,溶液中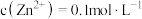 ,则调pH的范围为
,则调pH的范围为_____ 。
(4)“水解”过程中GeCl4水解的化学方程式为_____ 。
(5)“还原”时常在加热条件下通入适量H2,“还原”反应的化学方程式为_____ ,当该反应中转移2mol电子时,理论上制备单质锗的质量为_____ g。
 ,含少量FeO、SiO2、Ag2O和PbO等)为原料提取锗的流程如下:
,含少量FeO、SiO2、Ag2O和PbO等)为原料提取锗的流程如下: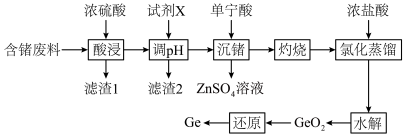
 时认为该离子沉淀完全。
时认为该离子沉淀完全。②
 。常温下,几种难溶电解质的溶度积数据如下:
。常温下,几种难溶电解质的溶度积数据如下:| 氢氧化物 | Pb(OH) 2 | Zn(OH) 2 | Fe(OH) 2 | Fe(OH) 3 |
| pKsp | 19.8 | 16.2 | 16.4 | 38.6 |
(1)“酸浸”之前,先粉碎含锗废料,其目的是
(2)试剂X可能是ZnO、Zn(OH) 2、ZnCO3、Zn(OH) 2CO3等,滤渣2的主要成分是
(3)“调pH”后,溶液中
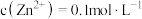 ,则调pH的范围为
,则调pH的范围为(4)“水解”过程中GeCl4水解的化学方程式为
(5)“还原”时常在加热条件下通入适量H2,“还原”反应的化学方程式为
您最近一年使用:0次
名校
解题方法
4 . GaN是一种重要的半导体材料,利用铝土矿(成分为 、
、 、
、 )制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是
)制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是
 、
、 、
、 )制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是
)制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是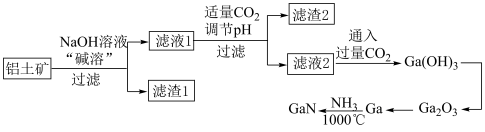
| A.过滤时需用到的硅酸盐材质仪器为烧杯、漏斗、玻璃棒 |
B.滤液1中主要含有的阴离子为 、 、 、 、 |
C.滤液2中得到 时发生反应的离子方程式为 时发生反应的离子方程式为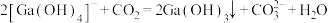 |
D.Ga与 反应生成GaN时,参与反应的氧化剂与还原剂的物质的量之比为1∶1 反应生成GaN时,参与反应的氧化剂与还原剂的物质的量之比为1∶1 |
您最近一年使用:0次
2024-06-29更新
|
456次组卷
|
5卷引用:河南省创新发展联盟2023-2024学年高一下学期5月月考化学试题
5 . 高锰酸盐指数是我国地表水的主要污染指标之一,反映水体受耗氧有机物污染的程度。我国现行标准采用水浴加热一滴定法测定高锰酸盐指数。具体操作步骤:按图1所示处理水样30分钟后取出锥形瓶,趁热加入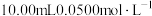 草酸钠溶液,充分反应后再用
草酸钠溶液,充分反应后再用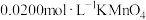 溶液滴定至终点。记录数据,计算高锰酸盐指数。
溶液滴定至终点。记录数据,计算高锰酸盐指数。
(1)现利用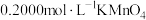 标准贮备液配制
标准贮备液配制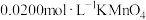 溶液,不需要使用的仪器有
溶液,不需要使用的仪器有______ (填标号)。
aA.烧杯 B.圆底烧瓶 C.玻璃棒 D.量筒 E.容量瓶
(2)滴定时发生反应的离子方程式为______ 。
(3)本实验所用 溶液的配制过程:将
溶液的配制过程:将 浓硫酸缓慢加入
浓硫酸缓慢加入 水中并不断搅拌,趁热逐滴加入
水中并不断搅拌,趁热逐滴加入 溶液直至溶液呈粉红色。加入
溶液直至溶液呈粉红色。加入 溶液的主要目的为
溶液的主要目的为______ 。
(4)高锰酸盐指数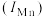 以每升样品消耗毫克氧数来表示
以每升样品消耗毫克氧数来表示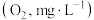 。
。 水样在滴定过程中消耗
水样在滴定过程中消耗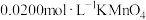 溶液
溶液 ,该水样的
,该水样的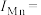
______  (用含
(用含 的表达式表示)。
的表达式表示)。
(5)若在水浴加热的过程中加上球形冷凝管,高锰酸盐指数会偏高,主要原因为______ 。
(6)利用分光光度法研究水样中有机物浓度(以物质X计, )和加热时间
)和加热时间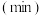 对测定高锰酸盐指数的影响。在本实验条件下吸光度与
对测定高锰酸盐指数的影响。在本实验条件下吸光度与 浓度成正比,实验结果如图2所示。
浓度成正比,实验结果如图2所示。 后,吸光度数值迅速降低,反应速率有变快的趋势,主要原因为
后,吸光度数值迅速降低,反应速率有变快的趋势,主要原因为______ 。
②利用水浴加热一滴定法测定地表水高锰酸盐指数时,需要控制水浴加热时间为 ,主要原因为
,主要原因为______ 。
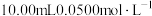 草酸钠溶液,充分反应后再用
草酸钠溶液,充分反应后再用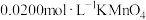 溶液滴定至终点。记录数据,计算高锰酸盐指数。
溶液滴定至终点。记录数据,计算高锰酸盐指数。
图1
回答下列问题:(1)现利用
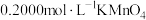 标准贮备液配制
标准贮备液配制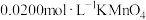 溶液,不需要使用的仪器有
溶液,不需要使用的仪器有aA.烧杯 B.圆底烧瓶 C.玻璃棒 D.量筒 E.容量瓶
(2)滴定时发生反应的离子方程式为
(3)本实验所用
 溶液的配制过程:将
溶液的配制过程:将 浓硫酸缓慢加入
浓硫酸缓慢加入 水中并不断搅拌,趁热逐滴加入
水中并不断搅拌,趁热逐滴加入 溶液直至溶液呈粉红色。加入
溶液直至溶液呈粉红色。加入 溶液的主要目的为
溶液的主要目的为(4)高锰酸盐指数
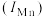 以每升样品消耗毫克氧数来表示
以每升样品消耗毫克氧数来表示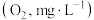 。
。 水样在滴定过程中消耗
水样在滴定过程中消耗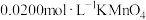 溶液
溶液 ,该水样的
,该水样的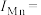
 (用含
(用含 的表达式表示)。
的表达式表示)。(5)若在水浴加热的过程中加上球形冷凝管,高锰酸盐指数会偏高,主要原因为
(6)利用分光光度法研究水样中有机物浓度(以物质X计,
 )和加热时间
)和加热时间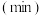 对测定高锰酸盐指数的影响。在本实验条件下吸光度与
对测定高锰酸盐指数的影响。在本实验条件下吸光度与 浓度成正比,实验结果如图2所示。
浓度成正比,实验结果如图2所示。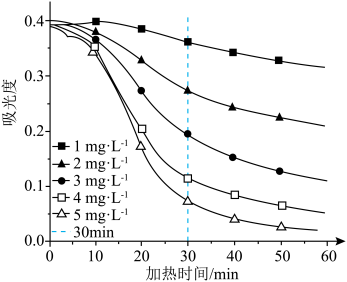
图2
①加热 后,吸光度数值迅速降低,反应速率有变快的趋势,主要原因为
后,吸光度数值迅速降低,反应速率有变快的趋势,主要原因为②利用水浴加热一滴定法测定地表水高锰酸盐指数时,需要控制水浴加热时间为
 ,主要原因为
,主要原因为
您最近一年使用:0次
名校
解题方法
6 . 铈(Ce)及其化合物在现代工业中具有极为重要的用途,某化工厂以废旧的液晶显示器(含有 、
、 、
、 等物质)为原料制备三氯化铈、氢氧化铈的流程如下:
等物质)为原料制备三氯化铈、氢氧化铈的流程如下: 具有强氧化性,一般不与常见的无机酸反应。
具有强氧化性,一般不与常见的无机酸反应。
请回答下列问题:
(1)酸浸前原料要粉碎,其目的是______________ (答出两点),料渣Ⅰ的成分是_____________ 。
(2)“还原”过程中发生反应的离子方程式为___________________ ,该过程不宜在较高温度下进行,原因是___________________ 。
(3)“氧化”过程中发生反应的离子方程式为__________________ 。
(4)得到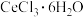 的实验操作是(在HCl氛围中)
的实验操作是(在HCl氛围中)___________ 、________ 、过滤、洗涤等。
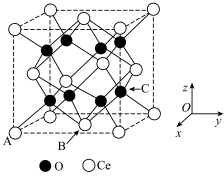
(5)二氧化铈晶胞结构如图所示,又知晶胞参数为a pm。若A、B两处微粒的原子分数坐标分别为 、
、 ,则C处微粒的原子分数坐标为
,则C处微粒的原子分数坐标为__________ ,晶体的密度为_______  。
。
 、
、 、
、 等物质)为原料制备三氯化铈、氢氧化铈的流程如下:
等物质)为原料制备三氯化铈、氢氧化铈的流程如下: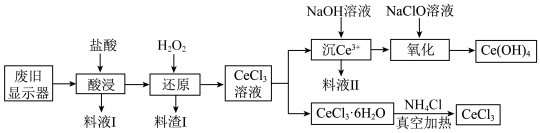
 具有强氧化性,一般不与常见的无机酸反应。
具有强氧化性,一般不与常见的无机酸反应。请回答下列问题:
(1)酸浸前原料要粉碎,其目的是
(2)“还原”过程中发生反应的离子方程式为
(3)“氧化”过程中发生反应的离子方程式为
(4)得到
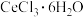 的实验操作是(在HCl氛围中)
的实验操作是(在HCl氛围中)(5)二氧化铈晶胞结构如图所示,又知晶胞参数为a pm。若A、B两处微粒的原子分数坐标分别为
 、
、 ,则C处微粒的原子分数坐标为
,则C处微粒的原子分数坐标为 。
。
您最近一年使用:0次
2024-06-28更新
|
133次组卷
|
2卷引用:2024届湘豫名校高三下学期考前保温卷理综试题-高中化学
7 . 化合物甲、乙的部分结构如图所示,其中a、b、c、d、e是原子序数依次增大的五种短周期主族元素,下列说法正确的是
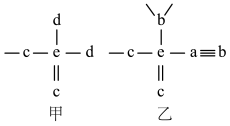
| A.五种元素中,d的最高价氧化物对应水化物的酸性最强 |
| B.第一电离能:d>c>b>a |
C.将铜加入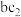 的水溶液(稀)中,反应中氧化剂与还原剂的物质的量之比为2∶3 的水溶液(稀)中,反应中氧化剂与还原剂的物质的量之比为2∶3 |
D.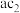 、 、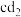 分子中中心原子发生sp杂化,分子构型都是直线形 分子中中心原子发生sp杂化,分子构型都是直线形 |
您最近一年使用:0次
名校
解题方法
8 .  是常见的亚硫酸盐,在潮湿的空气中易被氧化,在工业生产和实验室都有广泛的应用。
是常见的亚硫酸盐,在潮湿的空气中易被氧化,在工业生产和实验室都有广泛的应用。
(1)某兴趣小组为探究 溶液的性质,配制了100 mL 0.1 mol⋅L
溶液的性质,配制了100 mL 0.1 mol⋅L
 溶液。
溶液。
①在实验室中配制溶液需要用到的玻璃仪器有玻璃棒、烧杯、量筒、_______ 。
②同学依据S元素的化合价推测 具有氧化性,将0.1 mol⋅L
具有氧化性,将0.1 mol⋅L
 溶液和
溶液和 溶液混合,滴加适量稀硫酸,有乳白色浑浊出现,该反应的离子方程式为
溶液混合,滴加适量稀硫酸,有乳白色浑浊出现,该反应的离子方程式为_______ 。
(2)工业上利用 将废水中的Cr(Ⅵ)转化为Cr(Ⅲ)(
将废水中的Cr(Ⅵ)转化为Cr(Ⅲ)(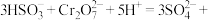
 ),然后加入石灰乳转化为
),然后加入石灰乳转化为 沉淀。转化过程中测得相同时间内废水中残留的Cr(Ⅵ)浓度与废水pH的关系如图所示。
沉淀。转化过程中测得相同时间内废水中残留的Cr(Ⅵ)浓度与废水pH的关系如图所示。 具有
具有_____ (填“氧化性”或“还原性”)。
②废水的pH比较小时,不利于Cr(Ⅵ)转化为Cr(Ⅲ),是由于溶液中 发生了副反应,该副反应的离子方程式为
发生了副反应,该副反应的离子方程式为______ ;废水的pH大于2.5时,残留Cr(Ⅵ)的浓度升高,其原因可能是______ 。
(3)亚硫酸氢钠纯度的测定。
Ⅰ.在250 mL碘量瓶中加入30.00 mL 0.1000 mol⋅L
 溶液和5 mL稀盐酸。
溶液和5 mL稀盐酸。
Ⅱ.称取0.2500 g 样品,快速加入250 mL碘量瓶中,立即盖上瓶塞,在暗处放置5 min。
样品,快速加入250 mL碘量瓶中,立即盖上瓶塞,在暗处放置5 min。
Ⅲ.向碘量瓶中逐滴加入0.1000 mol⋅L
 溶液至20.00 mL恰好反应。
溶液至20.00 mL恰好反应。
已知步骤Ⅲ发生的反应为 。
。
①步骤Ⅱ中发生反应的离子方程式为______ 。
②该亚硫酸氢钠样品的纯度为_______ 。
 是常见的亚硫酸盐,在潮湿的空气中易被氧化,在工业生产和实验室都有广泛的应用。
是常见的亚硫酸盐,在潮湿的空气中易被氧化,在工业生产和实验室都有广泛的应用。(1)某兴趣小组为探究
 溶液的性质,配制了100 mL 0.1 mol⋅L
溶液的性质,配制了100 mL 0.1 mol⋅L
 溶液。
溶液。①在实验室中配制溶液需要用到的玻璃仪器有玻璃棒、烧杯、量筒、
②同学依据S元素的化合价推测
 具有氧化性,将0.1 mol⋅L
具有氧化性,将0.1 mol⋅L
 溶液和
溶液和 溶液混合,滴加适量稀硫酸,有乳白色浑浊出现,该反应的离子方程式为
溶液混合,滴加适量稀硫酸,有乳白色浑浊出现,该反应的离子方程式为(2)工业上利用
 将废水中的Cr(Ⅵ)转化为Cr(Ⅲ)(
将废水中的Cr(Ⅵ)转化为Cr(Ⅲ)(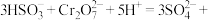
 ),然后加入石灰乳转化为
),然后加入石灰乳转化为 沉淀。转化过程中测得相同时间内废水中残留的Cr(Ⅵ)浓度与废水pH的关系如图所示。
沉淀。转化过程中测得相同时间内废水中残留的Cr(Ⅵ)浓度与废水pH的关系如图所示。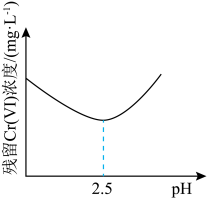
 具有
具有②废水的pH比较小时,不利于Cr(Ⅵ)转化为Cr(Ⅲ),是由于溶液中
 发生了副反应,该副反应的离子方程式为
发生了副反应,该副反应的离子方程式为(3)亚硫酸氢钠纯度的测定。
Ⅰ.在250 mL碘量瓶中加入30.00 mL 0.1000 mol⋅L

 溶液和5 mL稀盐酸。
溶液和5 mL稀盐酸。Ⅱ.称取0.2500 g
 样品,快速加入250 mL碘量瓶中,立即盖上瓶塞,在暗处放置5 min。
样品,快速加入250 mL碘量瓶中,立即盖上瓶塞,在暗处放置5 min。Ⅲ.向碘量瓶中逐滴加入0.1000 mol⋅L

 溶液至20.00 mL恰好反应。
溶液至20.00 mL恰好反应。已知步骤Ⅲ发生的反应为
 。
。①步骤Ⅱ中发生反应的离子方程式为
②该亚硫酸氢钠样品的纯度为
您最近一年使用:0次
解题方法
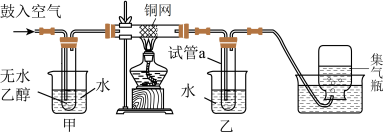
9 . 某创新实验小组设计如图装置进行乙醇催化氧化的实验探究。已知:乙醇、乙醛的沸点分别为78.5℃,20.8℃。请根据所学知识回答下列问题:_______ 。
(2)根据实验目的和题目信息,给甲、乙两处选择合适的水浴方式。
甲:_______ (填标号,下同);乙:_______ 。
A.热水浴 B.冷水浴
(3)经查阅资料得知,乙醇的催化氧化分两步进行,第一步反应为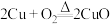 ;第二步反应为
;第二步反应为_______ 。
(4)若试管a中有三种有机成分,可用_______ 法将有机成分分离,集气瓶中收集到的气体中含量最高的为_______ (填化学式)。
(5)经检测,试管a中液体的 ,试推测其可能的原因:
,试推测其可能的原因:_______ ;写出该反应的化学方程式_______ 。
(2)根据实验目的和题目信息,给甲、乙两处选择合适的水浴方式。
甲:
A.热水浴 B.冷水浴
(3)经查阅资料得知,乙醇的催化氧化分两步进行,第一步反应为
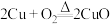 ;第二步反应为
;第二步反应为(4)若试管a中有三种有机成分,可用
(5)经检测,试管a中液体的
 ,试推测其可能的原因:
,试推测其可能的原因:
您最近一年使用:0次
2024-06-24更新
|
36次组卷
|
2卷引用:河南省创新发展联盟2023-2024学年高一下学期4月期中考试化学试题
10 . 利用 还原
还原 可以有效缓解大气污染。实验室研究烟气(含
可以有效缓解大气污染。实验室研究烟气(含 、
、 、
、 等)脱硝的实验装置如下图:
等)脱硝的实验装置如下图:
(1)装置A为制备氨气的发生装置,可选择下列装置。___________ (填序号)。
②若选择装置Ⅱ,则选择的药品是___________ (填名称)。
③若选择氯化铵、熟石灰制备氨气,则选择的装置是___________ (填序号);写出该反应的化学方程式:___________ 。
(2)装置D中 溶液可以吸收未除尽的
溶液可以吸收未除尽的 尾气,
尾气, 与
与 、
、 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
(3)若烟气中含有少量 ,会生成
,会生成 堵塞催化剂孔道。写出该反应的化学方程式:
堵塞催化剂孔道。写出该反应的化学方程式:___________ 。
(4)将烟气中 的体积分数检测后,再经过装置C气体检测测得
的体积分数检测后,再经过装置C气体检测测得 的转化率随反应温度变化的曲线如图所示。
的转化率随反应温度变化的曲线如图所示。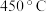 时,
时, 的转化率经降低为负值,其可能原因是
的转化率经降低为负值,其可能原因是___________ 。
 还原
还原 可以有效缓解大气污染。实验室研究烟气(含
可以有效缓解大气污染。实验室研究烟气(含 、
、 、
、 等)脱硝的实验装置如下图:
等)脱硝的实验装置如下图: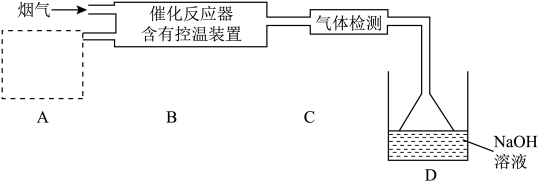
(1)装置A为制备氨气的发生装置,可选择下列装置。
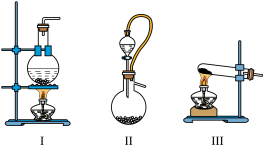
②若选择装置Ⅱ,则选择的药品是
③若选择氯化铵、熟石灰制备氨气,则选择的装置是
(2)装置D中
 溶液可以吸收未除尽的
溶液可以吸收未除尽的 尾气,
尾气, 与
与 、
、 反应生成
反应生成 的离子方程式为
的离子方程式为(3)若烟气中含有少量
 ,会生成
,会生成 堵塞催化剂孔道。写出该反应的化学方程式:
堵塞催化剂孔道。写出该反应的化学方程式:(4)将烟气中
 的体积分数检测后,再经过装置C气体检测测得
的体积分数检测后,再经过装置C气体检测测得 的转化率随反应温度变化的曲线如图所示。
的转化率随反应温度变化的曲线如图所示。
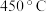 时,
时, 的转化率经降低为负值,其可能原因是
的转化率经降低为负值,其可能原因是
您最近一年使用:0次



