1 . 锂和铍是重要的稀有金属,被国内外视为战略性资源。一种从尾矿(主要含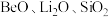 及
及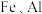 元素)中回收锂、铍、铝的工艺流程如图:
元素)中回收锂、铍、铝的工艺流程如图:
(1)“浸渣”中主要成分的晶体类型为_____ 。
(2)“沉铁”中生成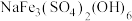 沉淀,其中
沉淀,其中 元素的化合价为
元素的化合价为_____ ,该反应的离子方程式为_____ 。
(3)“萃取”时,以 为萃取剂、
为萃取剂、 为协萃剂,溶液中的
为协萃剂,溶液中的 可与
可与 结合成
结合成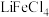 而被
而被 萃取。“反萃取”时,加入浓盐酸,发生
萃取。“反萃取”时,加入浓盐酸,发生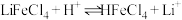 。
。
①“萃取”时还需要加入 ,其作用是
,其作用是_____ 。
②取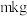 尾矿(其中
尾矿(其中 的质量分数为
的质量分数为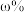 ),“反萃取”后所得
),“反萃取”后所得 水相中
水相中 ,则该过程
,则该过程 的回收率为
的回收率为_____ (用含相关物理量字母的代数式表示)。
(4)实验室提纯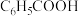 的方法是
的方法是_____ 。
(5)为了得到较高的空间利用率,离子晶体中的阴离子(通常半径较大)会尽可能紧密堆积,阳离子(通常半径较小)填入阴离子形成的空隙中,这种模型称为离子晶体的“堆积-填隙模型”。
已知常见的 型离子晶体的离子半径比和配位数的关系如下表:
型离子晶体的离子半径比和配位数的关系如下表:
表中离子半径比的临界值是由“堆积—填隙模型”中阴阳离子的几何关系确定的,例如配位数为8时,阳离子进入阴离子形成的正方体空隙,正方体8个顶点处的阴离了相切,空隙处(正方体体心)的阳离子与8个阴离子也相切,此时可由相关几何关系求得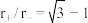 。
。
①
_____ 。
② 晶胞为立方
晶胞为立方 型,而
型,而 等的晶胞为
等的晶胞为 型。请结合上表,解释出现此结果的原因:
型。请结合上表,解释出现此结果的原因:_____ 。
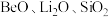 及
及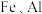 元素)中回收锂、铍、铝的工艺流程如图:
元素)中回收锂、铍、铝的工艺流程如图: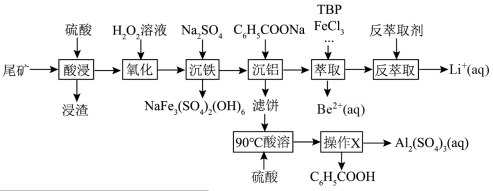
(1)“浸渣”中主要成分的晶体类型为
(2)“沉铁”中生成
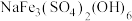 沉淀,其中
沉淀,其中 元素的化合价为
元素的化合价为(3)“萃取”时,以
 为萃取剂、
为萃取剂、 为协萃剂,溶液中的
为协萃剂,溶液中的 可与
可与 结合成
结合成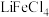 而被
而被 萃取。“反萃取”时,加入浓盐酸,发生
萃取。“反萃取”时,加入浓盐酸,发生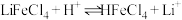 。
。①“萃取”时还需要加入
 ,其作用是
,其作用是②取
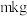 尾矿(其中
尾矿(其中 的质量分数为
的质量分数为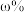 ),“反萃取”后所得
),“反萃取”后所得 水相中
水相中 ,则该过程
,则该过程 的回收率为
的回收率为(4)实验室提纯
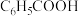 的方法是
的方法是(5)为了得到较高的空间利用率,离子晶体中的阴离子(通常半径较大)会尽可能紧密堆积,阳离子(通常半径较小)填入阴离子形成的空隙中,这种模型称为离子晶体的“堆积-填隙模型”。
已知常见的
 型离子晶体的离子半径比和配位数的关系如下表:
型离子晶体的离子半径比和配位数的关系如下表: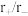 | 配位数 | 晶胞类型 |
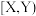 | 4 | 立方 |
 | 6 |  |
 | 8 |  |
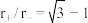 。
。①

②
 晶胞为立方
晶胞为立方 型,而
型,而 等的晶胞为
等的晶胞为 型。请结合上表,解释出现此结果的原因:
型。请结合上表,解释出现此结果的原因:
您最近一年使用:0次
2024-06-05更新
|
112次组卷
|
2卷引用:2024届河南省信阳高级中学高三下学期考前最后一卷理科综合试题-高中化学
2 . 以金红石(主要成分为 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: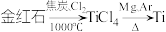 。下列叙述错误的是
。下列叙述错误的是
 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: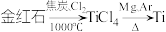 。下列叙述错误的是
。下列叙述错误的是A.利用碳氯化工艺制备 的化学方程式为 的化学方程式为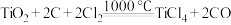 |
B.粗 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 |
C.制备Ti的主要过程中的 用 用 代替,会影响 代替,会影响 的产率和纯度 的产率和纯度 |
| D.将金红石和焦炭充分混合研磨后,再通入氯气可以提高反应速率 |
您最近一年使用:0次
名校
解题方法
3 . 用某复合金属作电极电解催化还原 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是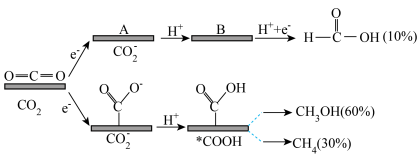
| A.过程中有极性键和非极性的断裂和形成 |
B.中间体B的结构简式为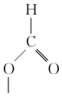 |
C. |
D.若有 完全转化,反应中转移的电子数为3.8mol 完全转化,反应中转移的电子数为3.8mol |
您最近一年使用:0次
2024-06-01更新
|
82次组卷
|
3卷引用:2024届河南省郑州市名校教研联盟高三下学期模拟预测理综试题-高中化学
解题方法
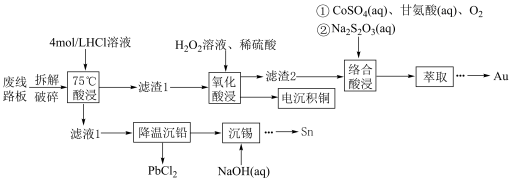
4 . 废旧手机的废线路板中富含Cu、Sn、Ni、Pb等金属和少量Ag、Au,具有较高的回收价值,其中部分金属的回收工艺流程如下: 微溶于水,可与
微溶于水,可与 结合生成
结合生成 配离子:
配离子: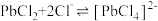 。
。
②25℃时,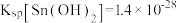 ,
,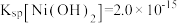 。
。
回答下列问题:
(1)“拆解破碎”的目的是_______ 。
(2)“75℃酸浸”中,金属Sn与盐酸反应的离子方程式为_______ ,选用浓度较大的4 mol·L 盐酸可提高铅元素的浸出率,理由是
盐酸可提高铅元素的浸出率,理由是_______ (从平衡移动角度分析)。
(3)“滤渣1”的主要成分是_______ (填化学式),“氧化酸浸”中,生成Cu²⁺反应的离子方程式为_______ 。
(4) 的排放标准为
的排放标准为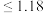 mg·L
mg·L 。“沉锡”残余液排放前应调节溶液的pH范围为
。“沉锡”残余液排放前应调节溶液的pH范围为_____ 。
(5)“络合酸浸”中,Co2+作催化剂,催化Au浸出,化学方程式为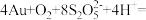
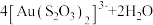 ,其反应过程按如下步骤进行:
,其反应过程按如下步骤进行:
① 先与甘氨酸根(简写为
先与甘氨酸根(简写为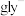 )形成配合物
)形成配合物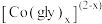 (
(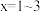 )。
)。
②在氧气作用下,Co(Ⅱ)被氧化成Co(Ⅲ):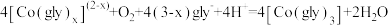 。
。
③Au溶解。
④加入硫代硫酸钠溶液,发生反应: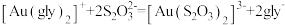 。
。
步骤③Au溶解的离子方程式为_______ 。
(6)锡有白锡和灰锡两种单质。白锡晶体中锡原子的堆积方式如图所示,该六棱柱底边边长为a pm,高为c pm,阿伏加德罗常数的值为 ,白锡晶体的密度为
,白锡晶体的密度为_______  (列出计算式)。
(列出计算式)。
 微溶于水,可与
微溶于水,可与 结合生成
结合生成 配离子:
配离子: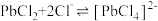 。
。②25℃时,
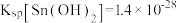 ,
,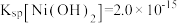 。
。回答下列问题:
(1)“拆解破碎”的目的是
(2)“75℃酸浸”中,金属Sn与盐酸反应的离子方程式为
 盐酸可提高铅元素的浸出率,理由是
盐酸可提高铅元素的浸出率,理由是(3)“滤渣1”的主要成分是
(4)
 的排放标准为
的排放标准为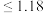 mg·L
mg·L 。“沉锡”残余液排放前应调节溶液的pH范围为
。“沉锡”残余液排放前应调节溶液的pH范围为(5)“络合酸浸”中,Co2+作催化剂,催化Au浸出,化学方程式为
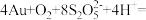
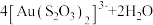 ,其反应过程按如下步骤进行:
,其反应过程按如下步骤进行:①
 先与甘氨酸根(简写为
先与甘氨酸根(简写为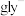 )形成配合物
)形成配合物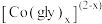 (
(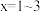 )。
)。②在氧气作用下,Co(Ⅱ)被氧化成Co(Ⅲ):
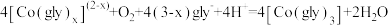 。
。③Au溶解。
④加入硫代硫酸钠溶液,发生反应:
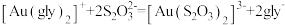 。
。步骤③Au溶解的离子方程式为
(6)锡有白锡和灰锡两种单质。白锡晶体中锡原子的堆积方式如图所示,该六棱柱底边边长为a pm,高为c pm,阿伏加德罗常数的值为
 ,白锡晶体的密度为
,白锡晶体的密度为 (列出计算式)。
(列出计算式)。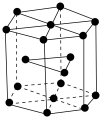
您最近一年使用:0次
2024-05-28更新
|
83次组卷
|
2卷引用:2024届河南省名校联盟高三下学期5月联考(三模)理综试题-高中化学
名校
5 . 二氧化铈( )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示:
(1)“焙烧”时,通入空气的主要目的是_________________ 。
(2)滤渣的主要成分是___________________ (填化学式)。
(3)“还原、脱氟”时,先加入硫脲(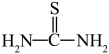 ),目的是将溶液中的
),目的是将溶液中的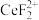 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_________________ [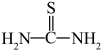 被氧化为
被氧化为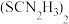 ,生成物还有HF和
,生成物还有HF和 ]。
]。
(4)“沉铈”时反应的离子方程式为__________________ 。若用 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是________________ 。
(5)若常温下,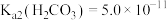 ,
,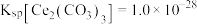 ,
, 恰好沉淀完全
恰好沉淀完全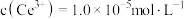 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中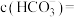
_____________  。
。
(6)二氧化铈作为一种SCR脱硝催化剂,能在 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物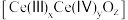 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为____________ 。
 )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示: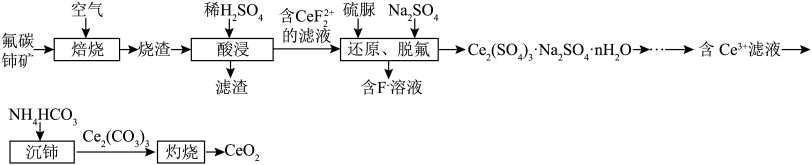
(1)“焙烧”时,通入空气的主要目的是
(2)滤渣的主要成分是
(3)“还原、脱氟”时,先加入硫脲(
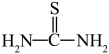 ),目的是将溶液中的
),目的是将溶液中的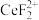 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式: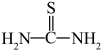 被氧化为
被氧化为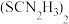 ,生成物还有HF和
,生成物还有HF和 ]。
]。(4)“沉铈”时反应的离子方程式为
 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是(5)若常温下,
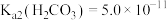 ,
,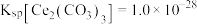 ,
, 恰好沉淀完全
恰好沉淀完全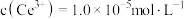 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中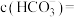
 。
。(6)二氧化铈作为一种SCR脱硝催化剂,能在
 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物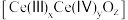 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为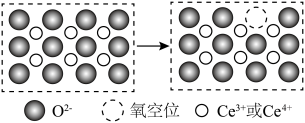
您最近一年使用:0次
2024-05-27更新
|
131次组卷
|
3卷引用:2024届河南省信阳市高三下学期高考考前押题理科综合试卷-高中化学
6 . 碘酸钙[ ]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备
]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备 实验步骤如下:
实验步骤如下:
Ⅰ.将一定质量的 、
、 和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;
和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;
Ⅱ.步骤Ⅰ反应完毕后,将烧瓶内的混合液倒入烧杯中,滴入KOH溶液调节pH=10,然后用滴管逐滴加入1 的
的 溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;
溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;
Ⅲ.碘酸钙粗品纯度:准确称取a g碘酸钙粗品于烧杯中,加入10mL 将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL
将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL  、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用
、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用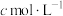 的
的 溶液滴定,平行三次,平均消耗
溶液滴定,平行三次,平均消耗 溶液的体积为V mL(
溶液的体积为V mL( )
)
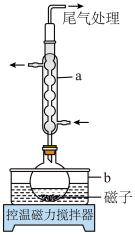
(1)仪器a的名称为___________ ,b中应盛放的最佳传热介质是___________ 。
(2)步骤Ⅰ中反应生成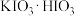 、
、 等,写出反应的化学方程式:
等,写出反应的化学方程式:___________ 。反应过程中,在烧瓶瓶颈或仪器a下口处可能会看到___________ (填物质名称)析出,其原因是___________ 。
(3)步骤Ⅱ“一系列操作”包括静置、___________ 、洗涤、干燥,其中洗涤所用较佳试剂为___________ (填“水”或“乙醇”)。
(4)碘酸钙粗晶纯度为___________ %(用含a、c、V的代数式表示),下列情况导致产品纯度测定结果偏低的是___________ (填字母)。
A.所配待测溶液中含有 少量沉淀 B.定容时俯视读数
少量沉淀 B.定容时俯视读数
C.盛放 溶液的滴定管未润洗 D.滴定后俯视读数
溶液的滴定管未润洗 D.滴定后俯视读数
 ]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备
]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备 实验步骤如下:
实验步骤如下:Ⅰ.将一定质量的
 、
、 和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;
和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;Ⅱ.步骤Ⅰ反应完毕后,将烧瓶内的混合液倒入烧杯中,滴入KOH溶液调节pH=10,然后用滴管逐滴加入1
 的
的 溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;
溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;Ⅲ.碘酸钙粗品纯度:准确称取a g碘酸钙粗品于烧杯中,加入10mL
 将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL
将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL  、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用
、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用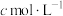 的
的 溶液滴定,平行三次,平均消耗
溶液滴定,平行三次,平均消耗 溶液的体积为V mL(
溶液的体积为V mL( )
)
(1)仪器a的名称为
(2)步骤Ⅰ中反应生成
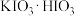 、
、 等,写出反应的化学方程式:
等,写出反应的化学方程式:(3)步骤Ⅱ“一系列操作”包括静置、
(4)碘酸钙粗晶纯度为
A.所配待测溶液中含有
 少量沉淀 B.定容时俯视读数
少量沉淀 B.定容时俯视读数C.盛放
 溶液的滴定管未润洗 D.滴定后俯视读数
溶液的滴定管未润洗 D.滴定后俯视读数
您最近一年使用:0次
2024-05-27更新
|
183次组卷
|
3卷引用:2024届河南省九师联盟2023-2024学年高三下学期4月联考理综试题-高中化学
7 . 硫酸亚硝酰合铁(Ⅱ)在现代化工行业有着广泛的应用,其一种工业制备流程如图所示。回答下列问题:

(1)“洗涤”的具体操作是将废铁屑置于 溶液中并加热至沸腾一段时间,加热至沸腾的好处是
溶液中并加热至沸腾一段时间,加热至沸腾的好处是___________ ,请写出“酸浸”副产物的一种用途:___________ 。
(2)“合成”阶段可在如图所示的装置中完成(加热及夹持装置略)。___________ ,向圆底烧瓶中加入稀硫酸前需要先通入一段时间的 ,否则易出现的不良后果是
,否则易出现的不良后果是___________ 。
②装置 中有
中有 生成,反应的离子方程式为
生成,反应的离子方程式为___________ ,装置 的作用是
的作用是___________ 。
③硫酸亚硝酰合铁(Ⅱ)化学式的确定。
(3)取一定量产品溶于水配制成 溶液,进行实验:
溶液,进行实验:
ⅰ.取 配制的溶液于试管中,加入足量
配制的溶液于试管中,加入足量 溶液,最终可得到
溶液,最终可得到 干燥纯净的白色沉淀。
干燥纯净的白色沉淀。
ⅱ.取 配制的溶液于试管中,用
配制的溶液于试管中,用 酸性
酸性 溶液滴定,滴定至终点时消耗酸性
溶液滴定,滴定至终点时消耗酸性 溶液
溶液 (最终氮元素全部以
(最终氮元素全部以 形式存在)。
形式存在)。
①“步骤ⅱ”滴定终点时的现象为___________ ,产品中
___________ 。
②若要确定产品化学式,则还需要获得一个数据,该数据是___________ 。

(1)“洗涤”的具体操作是将废铁屑置于
 溶液中并加热至沸腾一段时间,加热至沸腾的好处是
溶液中并加热至沸腾一段时间,加热至沸腾的好处是(2)“合成”阶段可在如图所示的装置中完成(加热及夹持装置略)。

 ,否则易出现的不良后果是
,否则易出现的不良后果是②装置
 中有
中有 生成,反应的离子方程式为
生成,反应的离子方程式为 的作用是
的作用是③硫酸亚硝酰合铁(Ⅱ)化学式的确定。
(3)取一定量产品溶于水配制成
 溶液,进行实验:
溶液,进行实验:ⅰ.取
 配制的溶液于试管中,加入足量
配制的溶液于试管中,加入足量 溶液,最终可得到
溶液,最终可得到 干燥纯净的白色沉淀。
干燥纯净的白色沉淀。ⅱ.取
 配制的溶液于试管中,用
配制的溶液于试管中,用 酸性
酸性 溶液滴定,滴定至终点时消耗酸性
溶液滴定,滴定至终点时消耗酸性 溶液
溶液 (最终氮元素全部以
(最终氮元素全部以 形式存在)。
形式存在)。①“步骤ⅱ”滴定终点时的现象为

②若要确定产品化学式,则还需要获得一个数据,该数据是
您最近一年使用:0次
解题方法
8 . 元素周期表可以用于探寻各种元素间的内在联系。
(1)下列关于元素周期表的说法错误的是______ 。
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是______ 。
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式_______ 。
②写出Si在元素周期表中的位置_______ 。由碳族元素结构特点,可推测Pb3O4中Pb的化合价为_____ 。
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为______ 。
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=____ 。向其中通入一定量的氯气发生反应,当c(Fe2+):c(Cl﹣)=1:4时,离子方程式为_____ 。
(1)下列关于元素周期表的说法错误的是
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式
②写出Si在元素周期表中的位置
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=
您最近一年使用:0次
9 . 下列实验方案一定能达到预期目的的是
| 选项 | 实验方案及现象 | 实验目的 |
| A | 向 溶液中依次加入几滴 溶液中依次加入几滴 溶液、几滴无色酚酞溶液,有白色沉淀生成及溶液变红色 溶液、几滴无色酚酞溶液,有白色沉淀生成及溶液变红色 | 探究该溶液中是否含有KOH |
| B | 向分子组成为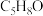 的醛类物质中加入溴水,溴水颜色消失 的醛类物质中加入溴水,溴水颜色消失 | 探究有机物中是否含有碳碳不饱和键 |
| C | 向含有淀粉的 溶液中滴加几滴溴水,振荡,得到蓝色溶液 溶液中滴加几滴溴水,振荡,得到蓝色溶液 | 探究还原性: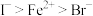 |
| D | 将石蜡油隔绝空气加强热,产生的气体通入 的 的 溶液中,溶液红棕色褪去 溶液中,溶液红棕色褪去 | 探究石蜡油分解生成不饱和烃气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 锑白 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的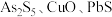 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: ;
;
②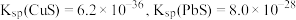 。
。
回答下列问题:
(1)“粉碎”辉锑矿的目的是___________ 。
(2)“滤渣Ⅰ”的主要成分除不溶性杂质外还有S、___________ (填化学式); 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为___________ 。
(3)“除砷”时,反应中氧化剂与还原剂的物质的量之比为___________ (P转化为最高价态)。
(4)若浸取液中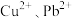 的浓度均为
的浓度均为 ,则c(S2-)≥
,则c(S2-)≥___________  才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时
才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时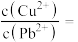
___________ 。
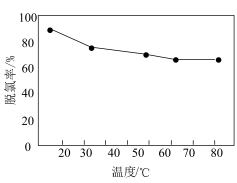
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:___________ 。
(6)锑可用于制备超亮光电极材料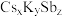 ,其晶胞结构如图所示,晶体a的化学式为
,其晶胞结构如图所示,晶体a的化学式为___________ ,晶体b中与 距离最近的
距离最近的 的个数为
的个数为___________ 。
 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的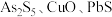 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: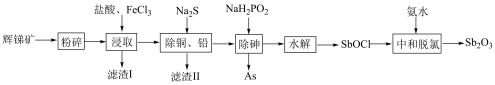
 ;
;②
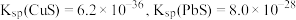 。
。回答下列问题:
(1)“粉碎”辉锑矿的目的是
(2)“滤渣Ⅰ”的主要成分除不溶性杂质外还有S、
 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为(3)“除砷”时,反应中氧化剂与还原剂的物质的量之比为
(4)若浸取液中
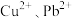 的浓度均为
的浓度均为 ,则c(S2-)≥
,则c(S2-)≥ 才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时
才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时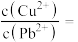
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:
(6)锑可用于制备超亮光电极材料
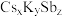 ,其晶胞结构如图所示,晶体a的化学式为
,其晶胞结构如图所示,晶体a的化学式为 距离最近的
距离最近的 的个数为
的个数为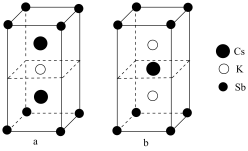
您最近一年使用:0次



