名校
解题方法
1 . 关注化学反应中的物质和能量变化是认识和研究化学反应的重要视角。
(1)在2.0 L恒温恒容密闭容器中充入2.0 mol 和6.0 mol
和6.0 mol  ,发生反应:
,发生反应:
 ,反应t min时测得
,反应t min时测得 的物质的量为3.6 mol。
的物质的量为3.6 mol。
①0~t min内,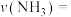
______ mol⋅L ⋅min
⋅min (用含t的代数式表示)。
(用含t的代数式表示)。
②反应至t min时,容器内压强与反应初始时压强之比为______ ;
(2)甲烷可以消除氮氧化物的污染: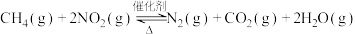 。
。
①在不改变初始浓度的条件下,加快反应速率的措施有______ (填一条)。
②若在恒温恒容密闭容器中充入1 mol 和2 mol
和2 mol  发生上述反应,下列叙述能说明反应达到平衡状态的是
发生上述反应,下列叙述能说明反应达到平衡状态的是______ (填字母)。
A. 、
、 、
、 的物质的量之比为1∶1∶2
的物质的量之比为1∶1∶2
B.混合气体中 的物质的量分数保持不变
的物质的量分数保持不变
C.混合气体的密度不再改变
D.混合气体的压强不再改变
(3)在催化剂作用下,利用含 的废气协同处理烟气中的
的废气协同处理烟气中的 ,转化为无污染气体的同时得到S单质,该反应的化学方程式为
,转化为无污染气体的同时得到S单质,该反应的化学方程式为____________ 。
(4) 催化剂可以催化
催化剂可以催化 脱除烟气中的NO。将
脱除烟气中的NO。将 和
和 按物质的量之比为4∶1通入烟气中,NO被还原为无污染气体。
按物质的量之比为4∶1通入烟气中,NO被还原为无污染气体。
①该反应中氧化剂与还原剂的物质的量之比为______ 。
②将模拟烟气以一定流速通过催化剂反应管,反应相同时间,测得NO的转化率随温度的变化如图所示。反应温度高于380℃时,NO的转化率下降的原因可能为______ (填一条)。
(1)在2.0 L恒温恒容密闭容器中充入2.0 mol
 和6.0 mol
和6.0 mol  ,发生反应:
,发生反应:
 ,反应t min时测得
,反应t min时测得 的物质的量为3.6 mol。
的物质的量为3.6 mol。①0~t min内,
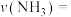
 ⋅min
⋅min (用含t的代数式表示)。
(用含t的代数式表示)。②反应至t min时,容器内压强与反应初始时压强之比为
(2)甲烷可以消除氮氧化物的污染:
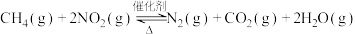 。
。①在不改变初始浓度的条件下,加快反应速率的措施有
②若在恒温恒容密闭容器中充入1 mol
 和2 mol
和2 mol  发生上述反应,下列叙述能说明反应达到平衡状态的是
发生上述反应,下列叙述能说明反应达到平衡状态的是A.
 、
、 、
、 的物质的量之比为1∶1∶2
的物质的量之比为1∶1∶2B.混合气体中
 的物质的量分数保持不变
的物质的量分数保持不变C.混合气体的密度不再改变
D.混合气体的压强不再改变
(3)在催化剂作用下,利用含
 的废气协同处理烟气中的
的废气协同处理烟气中的 ,转化为无污染气体的同时得到S单质,该反应的化学方程式为
,转化为无污染气体的同时得到S单质,该反应的化学方程式为(4)
 催化剂可以催化
催化剂可以催化 脱除烟气中的NO。将
脱除烟气中的NO。将 和
和 按物质的量之比为4∶1通入烟气中,NO被还原为无污染气体。
按物质的量之比为4∶1通入烟气中,NO被还原为无污染气体。①该反应中氧化剂与还原剂的物质的量之比为
②将模拟烟气以一定流速通过催化剂反应管,反应相同时间,测得NO的转化率随温度的变化如图所示。反应温度高于380℃时,NO的转化率下降的原因可能为

您最近一年使用:0次
2024-04-24更新
|
258次组卷
|
2卷引用:河南省新乡市多校联考2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
2 . 某校研究性学习小组设计实验,验证草酸受热分解的产物。已知:①草酸是一种弱酸,草酸晶体(H2C2O4·2H2O)易溶于水,受热易熔化、气化和分解。②草酸分解产生 和
和 。③草酸钙
。③草酸钙 是白色固体,难溶于水。
是白色固体,难溶于水。
(1)草酸中含有的化学键类型是____________ ,草酸晶体分解的化学方程式是____________ 。
(2)验证草酸分解的产物用到下列仪器,仪器的连接顺序是____________ (仪器可重复使用);A装置的作用是____________ ,该套装置___________ (填“是”或“否”)完善,说明理由____________ 。 的仪器名称是
的仪器名称是___________ 。
(4)证明有 生成的现象是
生成的现象是___________ 。
 和
和 。③草酸钙
。③草酸钙 是白色固体,难溶于水。
是白色固体,难溶于水。(1)草酸中含有的化学键类型是
(2)验证草酸分解的产物用到下列仪器,仪器的连接顺序是
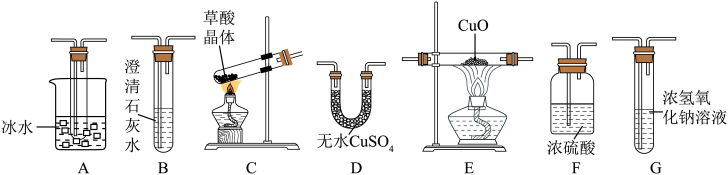
 的仪器名称是
的仪器名称是(4)证明有
 生成的现象是
生成的现象是
您最近一年使用:0次
2024-04-23更新
|
62次组卷
|
2卷引用:河南省安阳市林州市第一中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
3 . 氯化六氨合钴{ }是合成多种钴基功能材料和催化剂的中间体。已知:
}是合成多种钴基功能材料和催化剂的中间体。已知: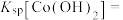
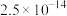 、
、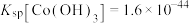 、
、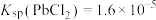 ;电对的标准电极电势(
;电对的标准电极电势( )越大,在水溶液中越容易发生还原反应,
)越大,在水溶液中越容易发生还原反应,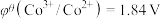 、
、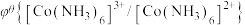
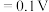 。某学习小组在实验室中制备氯化六氨合钴的步骤如下:
。某学习小组在实验室中制备氯化六氨合钴的步骤如下:
步骤一:称取3.0g CoCl2·6H2O,研磨后与4.0g NH4Cl混匀后溶于适量蒸馏水中,加入1.5g活性炭,搅拌均匀并冷却至室温;
步骤二;继续加入7mL浓氨水充分反应,再冷却至10℃后逐滴加入7mL 6%的双氧水,控制温度55℃充分反应;
步骤三:将反应后所得体系迅速冷却至2℃,过滤、洗涤;所得沉淀转入烧杯,加入20mL 80℃蒸馏水和1mL浓盐酸,趁热过滤,收集滤液;
步骤四:将滤液浓缩后加入3.5mL浓盐酸,并迅速冷却至2℃,抽滤、乙醇洗涤、干燥,收集得1.9g产品。
回答下列问题:
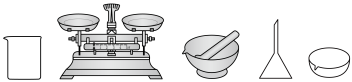
(1)步骤一中,下列仪器不需要使用的是___________ (填仪器名称)。___________ ;控制反应温度在55℃的原因为___________ 。
(3)相同条件下,氯化六氨合钴在稀盐酸中的溶解度___________ (填“大于”“小于”或“等于”)在浓盐酸中的。
(4)与步骤三中过滤相比,步骤四中抽滤的优点为___________ 。
(5)制备产品的总反应方程式为___________ ;步骤二中双氧水可用PbO2或KMnO4代替,其中更适合选用___________ (填化学式)代替双氧水,原因为___________ 。
(6)本实验所得产品的产率为___________ (列出计算式)。
 }是合成多种钴基功能材料和催化剂的中间体。已知:
}是合成多种钴基功能材料和催化剂的中间体。已知: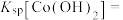
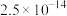 、
、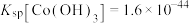 、
、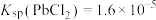 ;电对的标准电极电势(
;电对的标准电极电势( )越大,在水溶液中越容易发生还原反应,
)越大,在水溶液中越容易发生还原反应,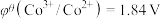 、
、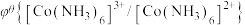
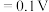 。某学习小组在实验室中制备氯化六氨合钴的步骤如下:
。某学习小组在实验室中制备氯化六氨合钴的步骤如下:步骤一:称取3.0g CoCl2·6H2O,研磨后与4.0g NH4Cl混匀后溶于适量蒸馏水中,加入1.5g活性炭,搅拌均匀并冷却至室温;
步骤二;继续加入7mL浓氨水充分反应,再冷却至10℃后逐滴加入7mL 6%的双氧水,控制温度55℃充分反应;
步骤三:将反应后所得体系迅速冷却至2℃,过滤、洗涤;所得沉淀转入烧杯,加入20mL 80℃蒸馏水和1mL浓盐酸,趁热过滤,收集滤液;
步骤四:将滤液浓缩后加入3.5mL浓盐酸,并迅速冷却至2℃,抽滤、乙醇洗涤、干燥,收集得1.9g产品。
回答下列问题:
(1)步骤一中,下列仪器不需要使用的是
(3)相同条件下,氯化六氨合钴在稀盐酸中的溶解度
(4)与步骤三中过滤相比,步骤四中抽滤的优点为
(5)制备产品的总反应方程式为
(6)本实验所得产品的产率为
您最近一年使用:0次
2024-04-19更新
|
193次组卷
|
5卷引用:2024届河南省高三下学期4月模拟考试理科综合试题-高中化学
解题方法
4 . 用锌窑渣回收Cu和 。已知锌窑渣主要成分有Fe、
。已知锌窑渣主要成分有Fe、 、
、 、FeS、CuS、
、FeS、CuS、 等。其流程如下图所示:
等。其流程如下图所示:
(1)滤渣的主要成分是_______ ,试剂1的化学式为_______ 。
(2)一般的矿物质用盐酸浸出的速率要比硫酸高,但在实际工业生产中一般用硫酸对矿物质进行酸浸。其原因除了盐酸比硫酸价格高外,你认为还有的原因是______ (填一种原因即可)。
(3)为了得到目标产物,对沉淀1的处理方法为_______ ,
_______ 。
(4)氧化酸浸装置中,氧气的分压对Cu、Fe的溶出率的影响如图所示。_______ 。
②Fe溶出率随氧气分压增大而增大的原因是_______ 。
 。已知锌窑渣主要成分有Fe、
。已知锌窑渣主要成分有Fe、 、
、 、FeS、CuS、
、FeS、CuS、 等。其流程如下图所示:
等。其流程如下图所示: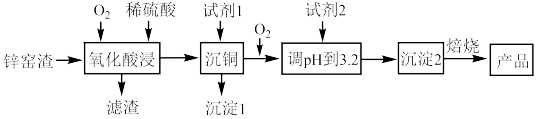
(1)滤渣的主要成分是
(2)一般的矿物质用盐酸浸出的速率要比硫酸高,但在实际工业生产中一般用硫酸对矿物质进行酸浸。其原因除了盐酸比硫酸价格高外,你认为还有的原因是
(3)为了得到目标产物,对沉淀1的处理方法为
(4)氧化酸浸装置中,氧气的分压对Cu、Fe的溶出率的影响如图所示。
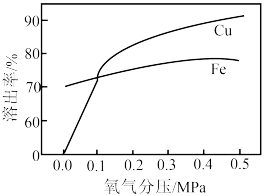
②Fe溶出率随氧气分压增大而增大的原因是
您最近一年使用:0次
解题方法
5 . 某兴趣小组探究电镀银实验。回答下列问题:
I.实验准备。
(1)用 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是___________ (填字母)。___________ 。
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与 浓度有关。
浓度有关。
【查阅资料】
络合反应: ,
, 。
。
【设计实验】
【问题讨论】
(3)实验a中,溶液变红色的可能原因是 和
和___________ (用离子方程式表示,已知氧化性: )。
)。
(4)①实验a、b的阴极都伴随有气泡,其原因是___________ (写电极反应式)。
②实验b比实验a产生的镀层光亮、致密,其原理是___________ 。
③一段时间后,实验b中 平衡不移动,其原因是
平衡不移动,其原因是___________ 。
【实验结论】
其他条件不变, 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。
Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与
 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。
表2:其他条件不变,温度对镀层外观的影响。
(5)表1中 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是___________ ;
表2中温度为 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是___________ 。
Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。
(6)使用新配方可以达到同样的目的,其原理是___________ 。已知: 。
。
I.实验准备。
(1)用
 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是A. B.
B. C.
C. D.
D. E.
E.
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与
 浓度有关。
浓度有关。【查阅资料】
络合反应:
 ,
, 。
。【设计实验】
| 实验 | 装置 | 现象 |
| a |
 的 的 溶液(含少量 溶液(含少量 ) ) | 阴极表面有疏松的黑色物质生成并伴随有无色气泡,一段时间后,取阴极区电解质溶液于试管,滴加 溶液,溶液变为红色。 溶液,溶液变为红色。 |
| b |
 的 的 与过量 与过量 混合(含少量 混合(含少量 ) ) | 阴极表面有光亮、致密的银白色物质生成,仍然有少量无色气泡。一段时间后,取少量阴极区溶液于试管,滴加 溶液,溶液不变红。 溶液,溶液不变红。 |
(3)实验a中,溶液变红色的可能原因是
 和
和 )。
)。(4)①实验a、b的阴极都伴随有气泡,其原因是
②实验b比实验a产生的镀层光亮、致密,其原理是
③一段时间后,实验b中
 平衡不移动,其原因是
平衡不移动,其原因是【实验结论】
其他条件不变,
 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与

 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。 含量( 含量( ) ) | 镀层外观表象 |
| 10 | 镀层模糊,无光泽 |
| 25 | 镀层呈雾状,光泽不足 |
| 50 | 镀层光亮、致密 |
温度/ | 镀层外观表象 |
| 25 | 光亮 |
| 35 | 光亮 |
| 40 | 光亮 |
| 55 | 光亮不均匀 |
(5)表1中
 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是表2中温度为
 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由
 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。(6)使用新配方可以达到同样的目的,其原理是
 。
。
您最近一年使用:0次
2024-04-16更新
|
337次组卷
|
5卷引用:2024届河南省TOP二十名校联考高三下学期5月猜题(一)理科综合试卷-高中化学
2024届河南省TOP二十名校联考高三下学期5月猜题(一)理科综合试卷-高中化学2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学2024届青海省玉树州高三下学期第四次联考理综试题-高中化学(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
6 . 古代青铜器的出土,体现了古代中国对人类物质文明的巨大贡献。青铜器埋藏会产生多种锈蚀产物,其中 结构致密,可以阻止内部青铜继续被腐蚀,而
结构致密,可以阻止内部青铜继续被腐蚀,而 结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:不正确 的是
 结构致密,可以阻止内部青铜继续被腐蚀,而
结构致密,可以阻止内部青铜继续被腐蚀,而 结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
结构疏松膨胀,可使锈蚀很快蔓延。青铜锈蚀过程大致如下:
A.青铜锈蚀Ⅰ过程属于电化学腐蚀,负极的电极反应方程式为: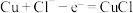 |
B.青铜锈蚀Ⅰ过程中 浓度越大,腐蚀趋势越大 浓度越大,腐蚀趋势越大 |
C.青铜锈蚀Ⅲ生成 的方程式为: 的方程式为: |
| D.青铜器修复可用碳酸钠溶液浸泡一段时间,使其保存更长久 |
您最近一年使用:0次
2024-04-15更新
|
399次组卷
|
5卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期5月月考化学试题
名校
解题方法
7 . 根据要求完成下列方程式。
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。
①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式___________ 。
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式___________ 。
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式___________ 。
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式___________ 。
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式___________ 。(提示:反应中价态不变)
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式___________ 。(已知:氯气遇到黄血盐可以得到赤血盐)
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3]
 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式
您最近一年使用:0次
8 . Na2SO3固体在隔绝空气强热过程中质量不变。待固体冷却后溶于水,溶液的碱性比Na2SO3 溶液强,所得固体成分可能是
| A.Na2S Na2O Na2SO3 | B.Na2SO4 Na2O Na2SO3 |
| C.Na2O Na2S Na2SO4 | D.Na2S Na2SO4 Na2SO3 |
您最近一年使用:0次
解题方法
9 . 钯(Pd)是航天、航空等高科技领域不可缺少的关键材料。一种从铂钯精矿[含有Pt、Pd、Au、Cu、Bi]中分离提取钯的工艺流程如图所示:
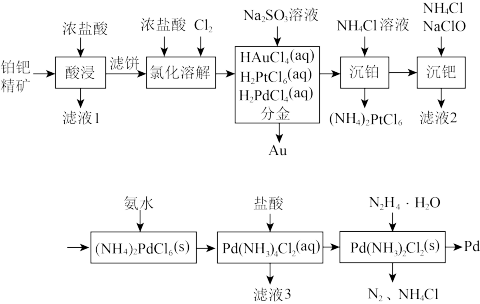
(1)“滤液1”中含有 和
和 ,
, 中Cu的化合价为
中Cu的化合价为________ ;Bi与As在周期表中位于同一主族,基态As原子的简化电子排布式为________ 。
(2)“氯化溶解”时氯气的作用是_________ 。
(3)“分金”时, 的氧化性
的氧化性____ (填“大于”或“小于”)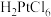 ,理由是
,理由是_____ 。
(4)“沉铂”时发生反应的化学方程式为_________ 。
(5)“沉钯”时反应的化学方程式为___________ 。“滤液3”可以进入到________ 中循环利用。
(6) (水合肼)将
(水合肼)将 还原为金属钯时,还原剂与氧化剂的物质的量之比为
还原为金属钯时,还原剂与氧化剂的物质的量之比为________ 。

(1)“滤液1”中含有
 和
和 ,
, 中Cu的化合价为
中Cu的化合价为(2)“氯化溶解”时氯气的作用是
(3)“分金”时,
 的氧化性
的氧化性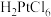 ,理由是
,理由是(4)“沉铂”时发生反应的化学方程式为
(5)“沉钯”时反应的化学方程式为
(6)
 (水合肼)将
(水合肼)将 还原为金属钯时,还原剂与氧化剂的物质的量之比为
还原为金属钯时,还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
2024-04-09更新
|
283次组卷
|
3卷引用:河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题
名校
解题方法
10 . 锡酸钠 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为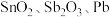 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体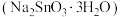 的工艺流程如下:
的工艺流程如下:
②锡酸钠晶体易溶于水,难溶于乙醇。
回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为___________ 。
(2)“高温真空蒸发”控制温度在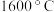 左右,目的是
左右,目的是___________ 。
(3)“高温碱熔”时,单质 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(4)已知“溶浸”后溶液中的阴离子主要为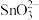 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为___________ 。
(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、___________ (填试剂名称)洗涤、___________ (填“低温”或“高温”)干燥。
(6)利用焦炭在 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为___________  。
。
 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为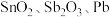 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体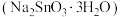 的工艺流程如下:
的工艺流程如下: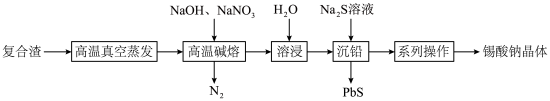
| 物质 |  |  |  |  |
沸点 | 1800 | 2260 | 1550 | 1740 |
回答下列问题:
(1)
 元素在周期表中的位置为
元素在周期表中的位置为(2)“高温真空蒸发”控制温度在
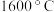 左右,目的是
左右,目的是(3)“高温碱熔”时,单质
 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(4)已知“溶浸”后溶液中的阴离子主要为
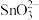 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、
(6)利用焦炭在
 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为 。
。
您最近一年使用:0次
2024-04-07更新
|
255次组卷
|
3卷引用:河南省漯河市高级中学2023-2024学年高三下学期4月月考化学试题