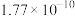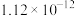1 . 下列实验方案一定能达到预期目的的是
| 选项 | 实验方案及现象 | 实验目的 |
| A | 向 溶液中依次加入几滴 溶液中依次加入几滴 溶液、几滴无色酚酞溶液,有白色沉淀生成及溶液变红色 溶液、几滴无色酚酞溶液,有白色沉淀生成及溶液变红色 | 探究该溶液中是否含有KOH |
| B | 向分子组成为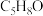 的醛类物质中加入溴水,溴水颜色消失 的醛类物质中加入溴水,溴水颜色消失 | 探究有机物中是否含有碳碳不饱和键 |
| C | 向含有淀粉的 溶液中滴加几滴溴水,振荡,得到蓝色溶液 溶液中滴加几滴溴水,振荡,得到蓝色溶液 | 探究还原性: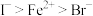 |
| D | 将石蜡油隔绝空气加强热,产生的气体通入 的 的 溶液中,溶液红棕色褪去 溶液中,溶液红棕色褪去 | 探究石蜡油分解生成不饱和烃气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 锑白 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的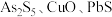 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: ;
;
②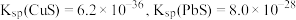 。
。
回答下列问题:
(1)“粉碎”辉锑矿的目的是___________ 。
(2)“滤渣Ⅰ”的主要成分除不溶性杂质外还有S、___________ (填化学式); 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为___________ 。
(3)“除砷”时,反应中氧化剂与还原剂的物质的量之比为___________ (P转化为最高价态)。
(4)若浸取液中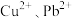 的浓度均为
的浓度均为 ,则c(S2-)≥
,则c(S2-)≥___________  才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时
才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时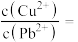
___________ 。
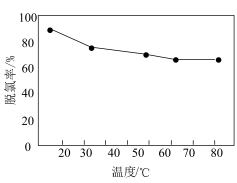
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:___________ 。
(6)锑可用于制备超亮光电极材料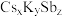 ,其晶胞结构如图所示,晶体a的化学式为
,其晶胞结构如图所示,晶体a的化学式为___________ ,晶体b中与 距离最近的
距离最近的 的个数为
的个数为___________ 。
 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的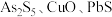 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: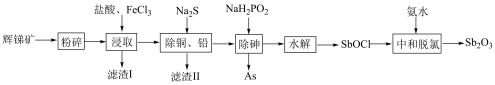
 ;
;②
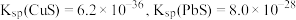 。
。回答下列问题:
(1)“粉碎”辉锑矿的目的是
(2)“滤渣Ⅰ”的主要成分除不溶性杂质外还有S、
 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为(3)“除砷”时,反应中氧化剂与还原剂的物质的量之比为
(4)若浸取液中
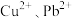 的浓度均为
的浓度均为 ,则c(S2-)≥
,则c(S2-)≥ 才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时
才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时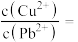
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:
(6)锑可用于制备超亮光电极材料
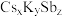 ,其晶胞结构如图所示,晶体a的化学式为
,其晶胞结构如图所示,晶体a的化学式为 距离最近的
距离最近的 的个数为
的个数为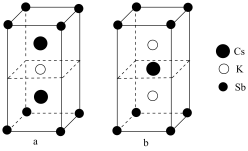
您最近一年使用:0次
名校
解题方法
3 . 用某复合金属作电极电解催化还原 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是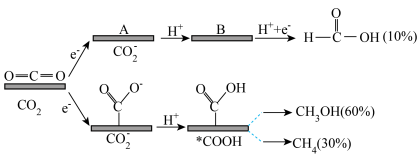
| A.过程中有极性键和非极性的断裂和形成 |
B.中间体B的结构简式为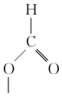 |
C. |
D.若有 完全转化,反应中转移的电子数为3.8mol 完全转化,反应中转移的电子数为3.8mol |
您最近一年使用:0次
2024-05-23更新
|
137次组卷
|
4卷引用:2024届河南省郑州市名校教研联盟高三下学期模拟预测理综试题-高中化学
2024届河南省郑州市名校教研联盟高三下学期模拟预测理综试题-高中化学河北省秦皇岛市部分示范高中2024届高三下学期三模化学试题2024届安徽省名校教研联盟高三下学期3月月考化学试卷 (已下线)专题2 化学计量及应用-物质的量在化学方程式计算中的应用
4 . 宋代《千里江山图》中大量使用两种含铜的矿物颜料。对于如图所示转化关系,下列说法正确的是

| A.反应①②③均为氧化还原反应 |
| B.孔雀石颜料和蓝铜矿颜料受热都可能变为黑色 |
| C.保存古画需控制温度和湿度,目的是防止孔雀石颜料等被氧化 |
| D.孔雀石颜料、蓝铜矿颜料耐酸碱腐蚀 |
您最近一年使用:0次
名校
5 . 碘酸钾 是常用的食盐加碘剂,用
是常用的食盐加碘剂,用 氧化
氧化 得到
得到 溶液,再经一系列步骤得到
溶液,再经一系列步骤得到 产品。
产品。 是一种白色晶体,在水中溶解度随温度升高而增大。
是一种白色晶体,在水中溶解度随温度升高而增大。
下列说法错误的是
 是常用的食盐加碘剂,用
是常用的食盐加碘剂,用 氧化
氧化 得到
得到 溶液,再经一系列步骤得到
溶液,再经一系列步骤得到 产品。
产品。
 是一种白色晶体,在水中溶解度随温度升高而增大。
是一种白色晶体,在水中溶解度随温度升高而增大。下列说法错误的是
A.水浴加热时发生反应的离子方程式为 |
| B.滴入适量乙醇的作用是除去多余的高锰酸钾 |
| C.为提高洗涤效果,可用热水进行洗涤 |
| D.在冷却结晶时,温度过低可能导致产品的纯度降低 |
您最近一年使用:0次
2024-05-23更新
|
306次组卷
|
3卷引用:河南省信阳高级中学2023-2024学年高一下学期6月月考化学试题
名校
6 . 从海带浸泡液(碘元素主要以 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。 的作用为
的作用为_______ (填“氧化剂”或“还原剂”)。
(2)为提高①的化学反应速率,可采取的措施是_______ (写出一条即可)。
(3)补全②的离子方程式:_______ 。
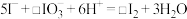
(4)②中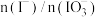 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。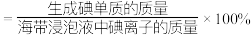
分析图中信息,选择最佳条件:_______ 。
 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。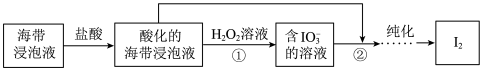
 的作用为
的作用为(2)为提高①的化学反应速率,可采取的措施是
(3)补全②的离子方程式:
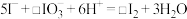
(4)②中
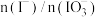 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。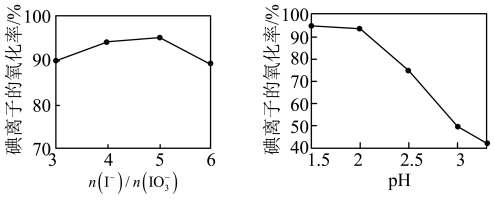
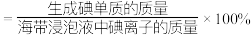
分析图中信息,选择最佳条件:
您最近一年使用:0次
2024-05-22更新
|
229次组卷
|
3卷引用:河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期6月月考化学试题
解题方法
7 .  是生产金属钛及其化合物的重要中间体,常温下为液体且有毒,暴露在空气中会发烟,极易水解。模拟工业上以
是生产金属钛及其化合物的重要中间体,常温下为液体且有毒,暴露在空气中会发烟,极易水解。模拟工业上以 、木炭和
、木炭和 为原料制备
为原料制备 的装置如图(夹持装置略)。
的装置如图(夹持装置略)。 的制备
的制备
(ⅰ)连接仪器,检验装置的气密性,盛装药品;(ⅱ)打开 ,……(ⅲ)打开
,……(ⅲ)打开 ,加入适量浓盐酸,接通冷凝装置,加热管式炉开始反应。回答下列问题:
,加入适量浓盐酸,接通冷凝装置,加热管式炉开始反应。回答下列问题:
(1)操作(ⅱ)的后续操作为________________ 。
(2)装置D的产物均为有毒化合物,则该反应的化学方程式为________________ ;判断该反应结束的实验现象是________________ 。
(3)A中反应结束后,再通入适量 的目的是
的目的是________________ ;图示装置存在的两处缺陷是________________ 。
Ⅱ. 含量的测定
含量的测定
将m g样品的水解液配成 溶液,取
溶液,取 于锥形瓶中,滴加2~3滴
于锥形瓶中,滴加2~3滴 溶液为指示剂,用
溶液为指示剂,用 的
的 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液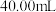 。
。
已知:
(4)该产品纯度为________ 。
(5)下列实验操作会导致产品纯度测定结果偏低的有________(填字母)。
 是生产金属钛及其化合物的重要中间体,常温下为液体且有毒,暴露在空气中会发烟,极易水解。模拟工业上以
是生产金属钛及其化合物的重要中间体,常温下为液体且有毒,暴露在空气中会发烟,极易水解。模拟工业上以 、木炭和
、木炭和 为原料制备
为原料制备 的装置如图(夹持装置略)。
的装置如图(夹持装置略)。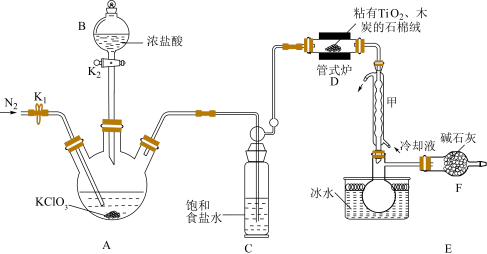
 的制备
的制备(ⅰ)连接仪器,检验装置的气密性,盛装药品;(ⅱ)打开
 ,……(ⅲ)打开
,……(ⅲ)打开 ,加入适量浓盐酸,接通冷凝装置,加热管式炉开始反应。回答下列问题:
,加入适量浓盐酸,接通冷凝装置,加热管式炉开始反应。回答下列问题:(1)操作(ⅱ)的后续操作为
(2)装置D的产物均为有毒化合物,则该反应的化学方程式为
(3)A中反应结束后,再通入适量
 的目的是
的目的是Ⅱ.
 含量的测定
含量的测定将m g样品的水解液配成
 溶液,取
溶液,取 于锥形瓶中,滴加2~3滴
于锥形瓶中,滴加2~3滴 溶液为指示剂,用
溶液为指示剂,用 的
的 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液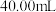 。
。已知:
难溶物 |
|
|
颜色 | 白 | 砖红 |
|
|
|
(4)该产品纯度为
(5)下列实验操作会导致产品纯度测定结果偏低的有________(填字母)。
| A.用待测液润洗锥形瓶 | B.样品暴露在空气中时间较长 |
| C.滴定终点时仰视读数 | D.滴加指示剂的量过多 |
您最近一年使用:0次
解题方法
8 . 中华文化博大精深,蕴含着丰富且深邃的化学知识。下列说法正确的是
| A.“凡石灰经火焚炼为用”,其反应原理可用于制备生石灰 |
B.“高奴县有洧水可燃”,“洧水”完全燃烧的产物只有 和 和 |
C.“曾青涂铁,铁赤如铜”,涉及的反应能证明氧化性: |
| D.“有硒水者,剪银塊投之,则旋而为水”,“硒水”在实验室中保存在无色瓶中 |
您最近一年使用:0次
解题方法
9 . 硫脲 易溶于水,有较强的还原性,温度较高时能发生异构化,常用作橡胶促进剂和医药合成的原料.实验室先制备
易溶于水,有较强的还原性,温度较高时能发生异构化,常用作橡胶促进剂和医药合成的原料.实验室先制备 ,
, 再与
再与 反应制备硫脲,装置(夹持及加热装置略)如下图所示.
反应制备硫脲,装置(夹持及加热装置略)如下图所示.
(1)仪器a的名称为__________ ;试剂X为__________ 。
(2)关闭 、
、 ,打开
,打开 ,开启搅拌器,充分反应,装置C中发生的主要反应的离子方程式为
,开启搅拌器,充分反应,装置C中发生的主要反应的离子方程式为__________ 。
(3)关闭 ,打开
,打开 ,通入
,通入 一段时间,目的是
一段时间,目的是__________ 。
(4)关闭 ,撤走搅拌器,打开
,撤走搅拌器,打开 ,控制仪器a中温度为
,控制仪器a中温度为 发生反应,反应一段时间后,将反应混合物过滤后低温蒸发,减压过滤、洗涤,干燥,得粗产品.采用低温蒸发的原因为
发生反应,反应一段时间后,将反应混合物过滤后低温蒸发,减压过滤、洗涤,干燥,得粗产品.采用低温蒸发的原因为__________ ;为减少氧化,减压过滤和干燥时最好采用的仪器是__________ 。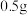 产品配成
产品配成 溶液,取
溶液,取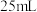 加入碘量瓶中,再加入
加入碘量瓶中,再加入 碘标准溶液和
碘标准溶液和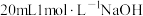 溶液,发生反应:
溶液,发生反应: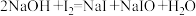 ;
;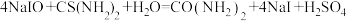 .充分反应后加稀硫酸至酸性,滴加两滴淀粉溶液,用
.充分反应后加稀硫酸至酸性,滴加两滴淀粉溶液,用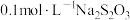 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: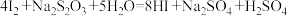 .至终点时消耗
.至终点时消耗 标准溶液
标准溶液 .达到滴定终点的现象为
.达到滴定终点的现象为__________ ;粗产品中硫脲的质量分数为__________ (用含V的代数式表示)。
 易溶于水,有较强的还原性,温度较高时能发生异构化,常用作橡胶促进剂和医药合成的原料.实验室先制备
易溶于水,有较强的还原性,温度较高时能发生异构化,常用作橡胶促进剂和医药合成的原料.实验室先制备 ,
, 再与
再与 反应制备硫脲,装置(夹持及加热装置略)如下图所示.
反应制备硫脲,装置(夹持及加热装置略)如下图所示.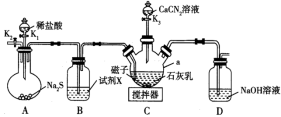
(1)仪器a的名称为
(2)关闭
 、
、 ,打开
,打开 ,开启搅拌器,充分反应,装置C中发生的主要反应的离子方程式为
,开启搅拌器,充分反应,装置C中发生的主要反应的离子方程式为(3)关闭
 ,打开
,打开 ,通入
,通入 一段时间,目的是
一段时间,目的是(4)关闭
 ,撤走搅拌器,打开
,撤走搅拌器,打开 ,控制仪器a中温度为
,控制仪器a中温度为 发生反应,反应一段时间后,将反应混合物过滤后低温蒸发,减压过滤、洗涤,干燥,得粗产品.采用低温蒸发的原因为
发生反应,反应一段时间后,将反应混合物过滤后低温蒸发,减压过滤、洗涤,干燥,得粗产品.采用低温蒸发的原因为
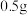 产品配成
产品配成 溶液,取
溶液,取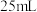 加入碘量瓶中,再加入
加入碘量瓶中,再加入 碘标准溶液和
碘标准溶液和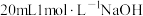 溶液,发生反应:
溶液,发生反应: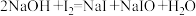 ;
;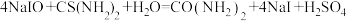 .充分反应后加稀硫酸至酸性,滴加两滴淀粉溶液,用
.充分反应后加稀硫酸至酸性,滴加两滴淀粉溶液,用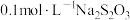 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: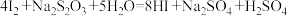 .至终点时消耗
.至终点时消耗 标准溶液
标准溶液 .达到滴定终点的现象为
.达到滴定终点的现象为
您最近一年使用:0次
10 . 磷酸铁锂前驱体磷酸铁是一种重要的化工原料,被广泛用于汽车电池。用浓硫酸浸取钛铁矿(主要成分为 ),得到含
),得到含 的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下:
的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下:___________ 。
(2)先加入磷酸,再加入NaOH,调节pH约为2,生成磷酸铁沉淀。若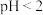 ,会导致
,会导致___________ ;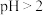 ,会导致
,会导致___________ 。
(3)经陈化、过滤后,所得滤液除少量磷酸铁外还含有的主要成分是___________ 。将滤液收集用于溶解步骤,其目的是___________ (答出两条即可)。
(4)在该流程中,以 、
、 、
、 和NaOH为反应物制得水合磷酸铁
和NaOH为反应物制得水合磷酸铁 总反应的离子方程式为
总反应的离子方程式为___________ 。
(5)煅烧水合磷酸铁过程中的TG(热重)及DSC(反映体系热量变化况,数值已省略)曲线如下图。样品在50~120℃有少量失重,可能是样品吸潮引起的少量游离水的损失(0.7%左右),从120℃开始有明显的失重,到200℃时失重达19.98%,则x值为___________ 。 为正交晶系结构,其晶胞参数为
为正交晶系结构,其晶胞参数为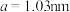 、
、 、
、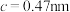 ,
, 。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为
。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为___________  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 ),得到含
),得到含 的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下:
的钛白副产物和硫酸亚铁。净化除杂后的硫酸亚铁可用于制备磷酸铁,其工艺流程如下: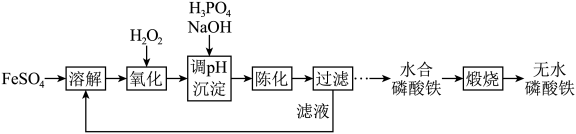
(2)先加入磷酸,再加入NaOH,调节pH约为2,生成磷酸铁沉淀。若
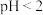 ,会导致
,会导致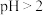 ,会导致
,会导致(3)经陈化、过滤后,所得滤液除少量磷酸铁外还含有的主要成分是
(4)在该流程中,以
 、
、 、
、 和NaOH为反应物制得水合磷酸铁
和NaOH为反应物制得水合磷酸铁 总反应的离子方程式为
总反应的离子方程式为(5)煅烧水合磷酸铁过程中的TG(热重)及DSC(反映体系热量变化况,数值已省略)曲线如下图。样品在50~120℃有少量失重,可能是样品吸潮引起的少量游离水的损失(0.7%左右),从120℃开始有明显的失重,到200℃时失重达19.98%,则x值为

 为正交晶系结构,其晶胞参数为
为正交晶系结构,其晶胞参数为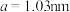 、
、 、
、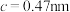 ,
, 。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为
。其晶胞结构如图所示,其中O围绕Fe和P分别形成正八面体和正四面体。则该晶体的密度为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。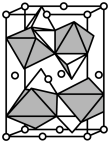
您最近一年使用:0次
2024-05-14更新
|
115次组卷
|
2卷引用:2024届河南省平许济洛四市高三下学期第四次质量检测理科综合试题-高中化学