1 . 已知硫酸酸化的K2Cr2O7溶液能与KI反应:aH2SO4+bK2Cr2O7+cKI=mK2SO4+nI2+pCr2(SO4)3+qH2O,下列说法错误的是
| A.a=7 |
| B.K2Cr2O7也可用盐酸酸化 |
| C.每生成1molCr2(SO4)3,转移6mole- |
| D.由上述反应可知,I-的还原性强于Cr3+的还原性 |
您最近一年使用:0次
2021-10-01更新
|
274次组卷
|
4卷引用:甘肃省会宁县第三中学2021-2022学年高三上学期第三次月考化学试题
2 . 由下列实验操作及现象能得出相应结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性: |
| B | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| C | 用pH计测定pH:①NaHCO3溶液②CH3COONa溶液 | pH:①>② | H2CO3酸性弱于CH3COOH |
| D | 把水滴入盛有少量Na2O2的试管中,立即把带火星木条放在试管口 | 木条复燃 | 反应生成了O2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-09-13更新
|
9430次组卷
|
25卷引用:甘肃省天水市田家炳中学2021-2022学年高三上学期第一阶段考试化学试题
甘肃省天水市田家炳中学2021-2022学年高三上学期第一阶段考试化学试题2021年新高考辽宁化学高考真题(已下线)第二单元 化学物质及其变化(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)2021年辽宁高考化学试题变式题1-102021年海南高考化学试题变式题11-19(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)秘籍05 微型实验方案设计与评价-备战2022年高考化学抢分秘籍(全国通用)(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)微专题08 氧化性和还原性强弱的实验探究及应用-备战2023年高考化学一轮复习考点微专题湖北省枣阳市第一中学2022-2023学年高三上学期8月化学月考试题山东省青岛市即墨区第一中学2022-2023学年高三上学期10月月考化学试题辽宁省北镇市满族高级中学2022-2023学年高三上学期第一次质量检测化学试题新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年高三上学期第二次月考化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)考点09 钠及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)实验03 探究氧化钠和过氧化钠的性质-【同步实验课】2023-2024学年高一化学教材实验大盘点(人教版2019必修第一册)(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)热点题型特训 实验方案中逻辑关系的匹配判断黑龙江省大庆市肇州县第二中学2023-2024学年高三上学期11月月考化学试题浙江省2023-2024学年高三上学期2月 模拟选考化学试题新疆喀什市第五中学2023-2024学年高三上学期12月大联考化学预测卷(已下线)压轴题09 微型化学实验设计与评价(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
名校
解题方法
3 . 叶蛇纹石是一种富镁硅酸盐矿物[主要成分为Mg6(Si4O10)(OH)8,还含有Al2O3、Fe2O3、FeO等杂质],利用该矿物生产铁红(Fe2O3)和碱式碳酸镁的工艺流程如图所示:
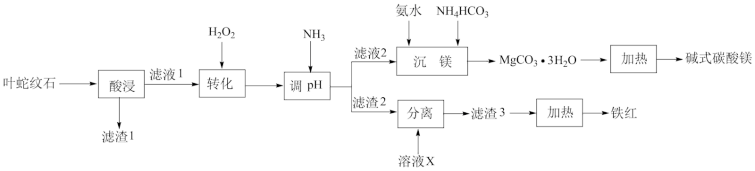
回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是___________ 。
(2)“调pH”时,产生滤渣2的反应离子方程式为___________ 。
(3)X通常选用___________ (填化学式)。
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是___________ 。
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=___________ 写出由MgCO3·3H2O生成产品的化学方程式:___________ 。
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:___________ 。(写出一点即可)。

回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是
(2)“调pH”时,产生滤渣2的反应离子方程式为
(3)X通常选用
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:
您最近一年使用:0次
2021-09-04更新
|
565次组卷
|
6卷引用:甘肃省武威市凉州区2021-2022学年高三下学期质量检测理综化学试题
名校
4 . 写出下列反应的离子方程式:
(1)向AlCl3溶液中加入过量NaOH溶液:_______
(2)向FeI2溶液中通入完全过量的氯气:_______
(3)向1L1mol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液:_______
(4) 与
与 水溶液混合后恰好沉淀完全的离子方程式
水溶液混合后恰好沉淀完全的离子方程式_______
(5)用ClO2进行饮用水处理比使用Cl2具有更高的优越性,不仅杀菌消毒效率高,不产生致癌的有机氯代物,而且还能除去水中的Fe2+,Mn2+。请写出用ClO2除去饮用水中Mn2+的离子方程式:_______ (已知Mn2+转变为MnO2,ClO2转变为 )
)
(6)Fe的一种含氧酸根离子 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式为:
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式为:_______
(1)向AlCl3溶液中加入过量NaOH溶液:
(2)向FeI2溶液中通入完全过量的氯气:
(3)向1L1mol/L的NH4Al(SO4)2溶液中滴加2L等浓度的Ba(OH)2溶液:
(4)
 与
与 水溶液混合后恰好沉淀完全的离子方程式
水溶液混合后恰好沉淀完全的离子方程式(5)用ClO2进行饮用水处理比使用Cl2具有更高的优越性,不仅杀菌消毒效率高,不产生致癌的有机氯代物,而且还能除去水中的Fe2+,Mn2+。请写出用ClO2除去饮用水中Mn2+的离子方程式:
 )
)(6)Fe的一种含氧酸根离子
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式为:
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式为:
您最近一年使用:0次
2021-09-01更新
|
323次组卷
|
2卷引用:甘肃省天水市一中2022届高三上学期8月第一次考试化学试题
解题方法
5 . 某工厂以废料(主要含 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备碳酸铈、氯化铈等铈产品的流程如下:
)为原料制备碳酸铈、氯化铈等铈产品的流程如下:
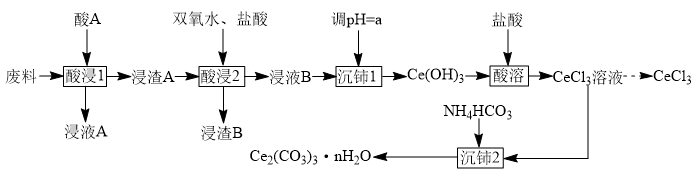
已知: 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。
回答下列问题:
(1)为加快“酸浸1”的速率,可采取的措施是___________ (写一条即可)。
(2)检验“浸液 ”中含有
”中含有 的试剂是
的试剂是___________ (填化学式,下同)溶液,“浸渣 ”的主要成分为
”的主要成分为___________ 。
(3)“酸浸2”中双氧水的作用是___________ (用离子方程式回答)。
(4)获得 的方法:将
的方法:将 和
和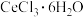 混合灼烧,得到
混合灼烧,得到 并放出能使品红溶液褪色的气体。加入
并放出能使品红溶液褪色的气体。加入 的原因是
的原因是___________ 。
(5)已知醋酸铵溶液呈中性,则 溶液中:
溶液中:
___________ (填“ ”、“
”、“ ”或“
”或“ ”)
”)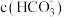 。
。
(6)测定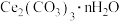 的纯度:
的纯度:
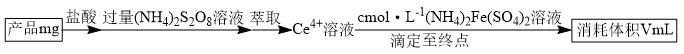
①已知 与
与 反应后的产物为
反应后的产物为 ,则该反应中氧化产物(
,则该反应中氧化产物( )与还原产物(
)与还原产物( )的物质的量之比为
)的物质的量之比为___________ 。
② 的纯度为
的纯度为___________  。[已知:
。[已知: 的摩尔质量为
的摩尔质量为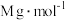 ]
]
③若其他操作均正确,滴定后俯视读数,则测得 的纯度
的纯度___________ (填“偏高”“偏低”或“无影响”)。
 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备碳酸铈、氯化铈等铈产品的流程如下:
)为原料制备碳酸铈、氯化铈等铈产品的流程如下:
已知:
 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。回答下列问题:
(1)为加快“酸浸1”的速率,可采取的措施是
(2)检验“浸液
 ”中含有
”中含有 的试剂是
的试剂是 ”的主要成分为
”的主要成分为(3)“酸浸2”中双氧水的作用是
(4)获得
 的方法:将
的方法:将 和
和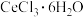 混合灼烧,得到
混合灼烧,得到 并放出能使品红溶液褪色的气体。加入
并放出能使品红溶液褪色的气体。加入 的原因是
的原因是(5)已知醋酸铵溶液呈中性,则
 溶液中:
溶液中:
 ”、“
”、“ ”或“
”或“ ”)
”)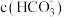 。
。(6)测定
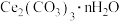 的纯度:
的纯度: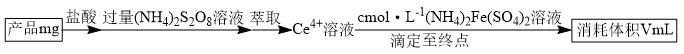
①已知
 与
与 反应后的产物为
反应后的产物为 ,则该反应中氧化产物(
,则该反应中氧化产物( )与还原产物(
)与还原产物( )的物质的量之比为
)的物质的量之比为②
 的纯度为
的纯度为 。[已知:
。[已知: 的摩尔质量为
的摩尔质量为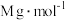 ]
]③若其他操作均正确,滴定后俯视读数,则测得
 的纯度
的纯度
您最近一年使用:0次
2021-08-30更新
|
275次组卷
|
4卷引用:甘肃省靖远县2021-2022学年高三上学期开学考试化学试题
解题方法
6 . 炼铁高炉的烟尘中主要含有Fe2O3和FeO,还含有少量的CuO、ZnO、SiO2等物质。通过图1步骤可从烟尘中得到有用物质。
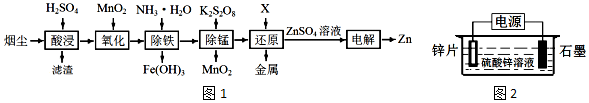
已知:25℃,Ksp[Fe(OH)3]=4×10-38 Kb(NH3∙H2O)=1.75×10-5
(1)“酸浸”步骤中所用的硫酸浓度太高会产生SO2有害气体,但也不能太低,理由是___ 。
(2)已知“氧化”步骤中1molMnO2得到2mole-,写出反应的离子方程式___ 。能判断氧化是否完全的试剂是___ (填标号)。
A. 氯水 B. 硫氰酸钾溶液 C. 高锰酸钾酸性溶液 D. 氢氧化钠溶液
(3)“除铁”步骤中用氨水将溶液的pH调节到5,若温度为25℃,溶液中c(Fe3+)=___ mol∙L-1, =
=___ 。
(4)“除锰”步骤中还原产物为K2SO4,则反应中氧化剂与还原剂的物质的量之比为___ 。
(5)“还原”步骤中X是___ 。
(6)电解ZnSO4溶液的装置如图2所示。阳极的电极反应式是___ 。

已知:25℃,Ksp[Fe(OH)3]=4×10-38 Kb(NH3∙H2O)=1.75×10-5
(1)“酸浸”步骤中所用的硫酸浓度太高会产生SO2有害气体,但也不能太低,理由是
(2)已知“氧化”步骤中1molMnO2得到2mole-,写出反应的离子方程式
A. 氯水 B. 硫氰酸钾溶液 C. 高锰酸钾酸性溶液 D. 氢氧化钠溶液
(3)“除铁”步骤中用氨水将溶液的pH调节到5,若温度为25℃,溶液中c(Fe3+)=
 =
=(4)“除锰”步骤中还原产物为K2SO4,则反应中氧化剂与还原剂的物质的量之比为
(5)“还原”步骤中X是
(6)电解ZnSO4溶液的装置如图2所示。阳极的电极反应式是
您最近一年使用:0次
名校
解题方法
7 . 某化学兴趣小组为探究酸性高锰酸钾与铜的反应,设计实验如下,在培养皿中加入足量的酸性高锰酸钾溶液,放入铜珠,实验结果如下:
已知: 在酸性溶液中不能稳定存在:
在酸性溶液中不能稳定存在: ,下列说法正确的是
,下列说法正确的是
| 实验 | 现象 |
 | 一段时间后,培养皿中由铜珠向外侧依次呈现: Ⅰ区澄清且紫色褪色明显 Ⅱ区底部覆盖棕黑色固体 Ⅲ区澄清且紫色变浅 |
 在酸性溶液中不能稳定存在:
在酸性溶液中不能稳定存在: ,下列说法正确的是
,下列说法正确的是A.Ⅰ区铜反应后的主要产物,可能是 、也可能是 、也可能是 |
B.Ⅱ区棕黑色固体是 ,由铜和酸性高锰酸钾反应产生 ,由铜和酸性高锰酸钾反应产生 |
C.Ⅲ区紫色变浅说明在Ⅲ区 也发生了氧化还原反应 也发生了氧化还原反应 |
D.如果酸性高锰酸钾大大过量,所有反应完全后,产物中可能没有 |
您最近一年使用:0次
2021-08-23更新
|
1788次组卷
|
10卷引用:甘肃省张掖市高台县第一中学2022-2023学年高三上学期第三次检测化学试题
甘肃省张掖市高台县第一中学2022-2023学年高三上学期第三次检测化学试题北京市十一学校2022 届高三上学期开学考试(暑期学习检测)化学试题湖南省长沙市第一中学2021-2022高一上学期第一次月考化学试卷河南省濮阳市第一高级中学2021-2022学年高一上学期期中化学(B)试题河北省衡水市2021-2022学年高三上学期三调化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)2022年湖南卷高考真题变式题(11-14)湖北省武汉市洪山高级中学2021-2022高一上学期9月月考化学试题(已下线)易错点3对实验原理分析不透彻而出错福建省厦门第六中学2023-2024学年高一上学期1月月考化学试题
名校
解题方法
8 . 近期央视播放了一套“大型文博探索节目”《国家宝藏》深受观众喜爱,其中由故宫博物院展出的《千里江山图卷》更是气象磅礴,吞吐山河,该卷长11.91米,颜色绚丽,由石绿,雌黄,赭石,砗磲,朱砂等颜料绘制而成,了解颜料的主要问题,回答以下问题:
(1)赭石,暗棕红色矿石,主要成分是氧化铁,遇盐酸可溶解, 工业炼铁常用含有氧化铁的赤铁矿为原料,在此过程中,炼铁的主要设备是________ ,炼铁的原料包括________ (填字母);
A.焦炭 B.铁矿石 C.烧碱 D.热空气
(2)用CO还原赤铁矿的主要原理是________ (用化学方程式表示)
(3)下列矿石主要成分为FeS2的是________ 。(填字母)
A.赤铁矿 B.磁铁矿 C.黄铁矿
(1)赭石,暗棕红色矿石,主要成分是氧化铁,遇盐酸可溶解, 工业炼铁常用含有氧化铁的赤铁矿为原料,在此过程中,炼铁的主要设备是
A.焦炭 B.铁矿石 C.烧碱 D.热空气
(2)用CO还原赤铁矿的主要原理是
(3)下列矿石主要成分为FeS2的是
A.赤铁矿 B.磁铁矿 C.黄铁矿
您最近一年使用:0次
名校
9 . 乙醇与酸性 溶液混合可发生反应:
溶液混合可发生反应: (未配平)。下列叙述不正确的是
(未配平)。下列叙述不正确的是
 溶液混合可发生反应:
溶液混合可发生反应: (未配平)。下列叙述不正确的是
(未配平)。下列叙述不正确的是A. 中Cr元素的化合价为+6 中Cr元素的化合价为+6 |
B.氧化产物为 |
C. 溶液常用硫酸酸化 溶液常用硫酸酸化 |
D.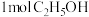 发生上述反应转移 发生上述反应转移 |
您最近一年使用:0次
2021-08-05更新
|
301次组卷
|
7卷引用:甘肃省武威第十八中学2020届高三上学期第一次诊断考试化学试题
甘肃省武威第十八中学2020届高三上学期第一次诊断考试化学试题2017届安徽省合肥市高三上学期第一次教学质量检测(一模)化学试卷福建省泉州市泉港区第一中学2016-2017学年高二下学期期末考试化学试题【全国百强校】江西省高安中学2017-2018学年高二下学期期末考试化学试题(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (题型专练)重庆市第三十七中学校 2021-2022学年(2022届)高三上学期 7月月考化学试题(已下线)第5讲 氧化还原反应方程式的配平与计算
名校
解题方法
10 . 电解精炼铜的阳极泥中含有 、
、 、
、 、
、 、
、 、
、 、
、 等,从其中提取
等,从其中提取 、
、 、
、 、
、 的单质的流程如图所示,回答下列问题:
的单质的流程如图所示,回答下列问题:
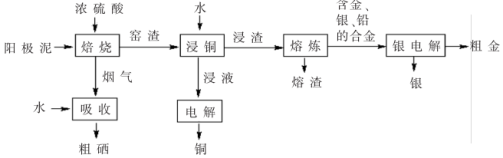
(1)粗铜中含有 、
、 两种元素的单质,但在阳极泥中几乎检测不到,原因是
两种元素的单质,但在阳极泥中几乎检测不到,原因是___________ 。
(2)已知阳极泥进行“硫酸化(隔绝空气)焙烧”,烟气中含有 ,
, 等。
等。
①写出“焙烧”过程中 与浓硫酸反应的化学方程式:
与浓硫酸反应的化学方程式:___________ 。
②将 、
、 通入水中即可生成单质硒,该反应的离子方程式为
通入水中即可生成单质硒,该反应的离子方程式为___________ 。
③实验室中将粗硒从溶液中分离出来的操作为___________ 。
(3)用惰性电极电解“浸液”时,溶液中发生的总反应离子方程式为___________ 。
(4)“银电解”时,阳极材料是___________ 。
(5)上述流程中,可以循环利用的物质是___________ (填写化学式)。
 、
、 、
、 、
、 、
、 、
、 、
、 等,从其中提取
等,从其中提取 、
、 、
、 、
、 的单质的流程如图所示,回答下列问题:
的单质的流程如图所示,回答下列问题:
(1)粗铜中含有
 、
、 两种元素的单质,但在阳极泥中几乎检测不到,原因是
两种元素的单质,但在阳极泥中几乎检测不到,原因是(2)已知阳极泥进行“硫酸化(隔绝空气)焙烧”,烟气中含有
 ,
, 等。
等。①写出“焙烧”过程中
 与浓硫酸反应的化学方程式:
与浓硫酸反应的化学方程式:②将
 、
、 通入水中即可生成单质硒,该反应的离子方程式为
通入水中即可生成单质硒,该反应的离子方程式为③实验室中将粗硒从溶液中分离出来的操作为
(3)用惰性电极电解“浸液”时,溶液中发生的总反应离子方程式为
(4)“银电解”时,阳极材料是
(5)上述流程中,可以循环利用的物质是
您最近一年使用:0次
2021-07-16更新
|
101次组卷
|
2卷引用:甘肃省白银市靖远县第一中学2023-2024学年高二上学期12月期末考试化学试题



