1 . 在酸性溶液中,FeS2催化氧化的物质转化关系如图所示。

下列有关叙述正确的是

下列有关叙述正确的是
| A.Fe2+是该反应的催化剂 |
| B.反应中,FeS2作氧化剂 |
| C.反应过程中须不断加入NO和O2 |
D.每消耗7molO2,溶液中最多增加4mol |
您最近一年使用:0次
2022-05-26更新
|
606次组卷
|
3卷引用:甘肃省武威市银科致远补习学校2023-2024学年高三上学期第三次调研化学试题
甘肃省武威市银科致远补习学校2023-2024学年高三上学期第三次调研化学试题天津市南开区2022届高三下学期第三次模拟化学试题(已下线)第06讲 氧化还原反应(练)-2023年高考化学一轮复习讲练测(全国通用)
名校
2 . 按要求回答下列问题。
I.黑火药爆炸的化学方程式为: S+ 2KNO3+ 3C K2S + N2↑+ CO2↑。回答下列问题:
K2S + N2↑+ CO2↑。回答下列问题:
(1)碳元素中,作为考古断代用的一种核素的原子符号为_______ ; 硫元素在周期表的位置是_______ ; 氨气的电子式为_______ ,氮气的结构式_______ ;该反应中S被_______ (“氧化”或“还原”)。
Ⅱ.可通过周期表预测元素的性质(由递变规律推测)
(2)推测未知元素的某些性质,如:已知Ca(OH)2微溶,Mg(OH)2难溶,可推知Be(OH)2_______ 溶(填易、微、难)。
(3)已知卤族元素(氟、氯、溴、碘)的性质递变规律,可推知元素砹(At)与氢_______ 化合(填易、难),AgAt_______ 于水(填溶、不溶)。
Ⅲ.材料是人类赖以生存和发展的物质基础。利用所学关于无机非金属材料的知识,回答下列相关问题。
(4)制造普通玻璃的原料为_______ ,将原料经过混合、粉碎,在玻璃窑中高温熔融,生成Na2SiO3的化学方程式为_______ 。
I.黑火药爆炸的化学方程式为: S+ 2KNO3+ 3C
 K2S + N2↑+ CO2↑。回答下列问题:
K2S + N2↑+ CO2↑。回答下列问题:(1)碳元素中,作为考古断代用的一种核素的原子符号为
Ⅱ.可通过周期表预测元素的性质(由递变规律推测)
(2)推测未知元素的某些性质,如:已知Ca(OH)2微溶,Mg(OH)2难溶,可推知Be(OH)2
(3)已知卤族元素(氟、氯、溴、碘)的性质递变规律,可推知元素砹(At)与氢
Ⅲ.材料是人类赖以生存和发展的物质基础。利用所学关于无机非金属材料的知识,回答下列相关问题。
(4)制造普通玻璃的原料为
您最近一年使用:0次
名校
3 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。下图是有关氮的循环示意图。请回答:
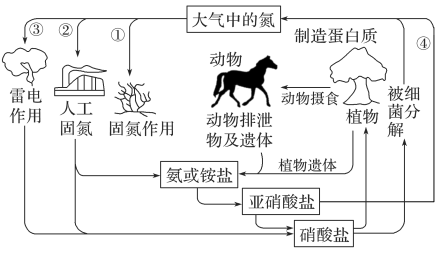
(1)请写出②中实现人工固氮的化学方程式:_______ 。
(2)氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。某科研小组研究发现在一定条件下氨气可用来将氮氧化物转化为无污染的物质,请写出氨气和二氧化氮在一定条件下反应的化学方程式_______ 。

(1)请写出②中实现人工固氮的化学方程式:
(2)氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。某科研小组研究发现在一定条件下氨气可用来将氮氧化物转化为无污染的物质,请写出氨气和二氧化氮在一定条件下反应的化学方程式
您最近一年使用:0次
4 . K3[Fe(C2O4)3]·3H2O常用作感光纸的光敏物质,为亮绿色晶体,易溶于水,难溶于乙醇。以废铁屑(含C和SiO2)为原料制备K3[Fe(C2O4)3]·3H2O的工艺流程如图所示。

(1)“溶解”过程中废渣的主要成分为____ (填化学式)。
(2)“沉铁”过程中获得黄色沉淀FeC2O4·2H2O,该反应的离子方程式为____ 。
(3)“转化”过程中体系中除了生成K3[Fe(C2O4)3]以外,还有Fe(OH)3生成,请写出“转化”过程中发生反应的化学方程式____ 。
(4)“转化”过程中检验H2O2是否足量的方法是____ 。
(5)“转化”过程中体系温度需保持在40℃的原因是____ 。
(6)“调pH”的目的是____ 。
(7)获得K3[Fe(C2O4)3]·3H2O晶体的“一系列操作”包括:趁热过滤,然后向滤液中加入____ (填物质名称),____ (填操作),过滤,洗涤,干燥。

(1)“溶解”过程中废渣的主要成分为
(2)“沉铁”过程中获得黄色沉淀FeC2O4·2H2O,该反应的离子方程式为
(3)“转化”过程中体系中除了生成K3[Fe(C2O4)3]以外,还有Fe(OH)3生成,请写出“转化”过程中发生反应的化学方程式
(4)“转化”过程中检验H2O2是否足量的方法是
(5)“转化”过程中体系温度需保持在40℃的原因是
(6)“调pH”的目的是
(7)获得K3[Fe(C2O4)3]·3H2O晶体的“一系列操作”包括:趁热过滤,然后向滤液中加入
您最近一年使用:0次
2022-04-20更新
|
2474次组卷
|
5卷引用:甘肃省兰州市2022届高三一诊理综化学试题
甘肃省兰州市2022届高三一诊理综化学试题(已下线)微专题25 化学工艺流程题-----原料的预处理-备战2023年高考化学一轮复习考点微专题(已下线)微专题26 化学工艺流程题-----核心反应与条件控制-备战2023年高考化学一轮复习考点微专题(已下线)微专题27 化学工艺流程题-----物质的分离与提纯-备战2023年高考化学一轮复习考点微专题四川省泸县第四中学2022-2023学年高二下学期6月期末考试化学试题
5 . 过二硫酸钾( )是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
)是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
实验(一):探究过二硫酸钾的强氧化性。
探究 溶液与
溶液与 溶液反应,实验操作与现象如下:
溶液反应,实验操作与现象如下:
(1)同学甲用碰撞理论分析,实验Ⅰ中 和
和 反应很慢的主要原因是
反应很慢的主要原因是___________
(2)同学乙猜想实验Ⅱ中 起催化作用,其总反应分两步进行:
起催化作用,其总反应分两步进行:
(ⅰ)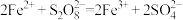 ;(ⅱ)___________。
;(ⅱ)___________。
①补充反应(ⅱ):___________ 。
②请你设计实验证明同学乙的猜想:___________ 。
(3)查阅文献知,氧化性: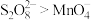 。在稀硫酸酸化的
。在稀硫酸酸化的 溶液中滴加1滴
溶液中滴加1滴 溶液作催化剂,再滴加
溶液作催化剂,再滴加 溶液,实验现象是
溶液,实验现象是___________ ,该反应的离子方程式为___________ 。
实验(二):探究过二硫酸钾的热稳定性。
已知几种气体的熔点、沸点如下表所示:
取适量的 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
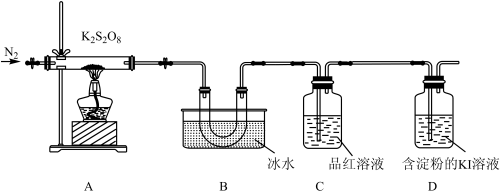
(4)加热之前,先通入一段时间 ,当观察到D中
,当观察到D中___________ (填实验现象)时点燃酒精灯。
(5)B中U形管收集的物质是___________ (填化学式)。
(6)当A中硬质玻璃管中固体完全分解,停止加热,残留的固体产物只有一种。待冷却至室温时取少量残留固体于试管,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。A中 完全分解发生反应的化学方程式为
完全分解发生反应的化学方程式为___________ 。
 )是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
)是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。实验(一):探究过二硫酸钾的强氧化性。
探究
 溶液与
溶液与 溶液反应,实验操作与现象如下:
溶液反应,实验操作与现象如下:| 实验 | 操作 | 现象 |
| Ⅰ | 在10L含淀粉的 的 的 溶液中滴加 溶液中滴加   溶液 溶液 | 一段时间后,溶液缓慢变蓝 |
| Ⅱ | 在 含淀粉的 含淀粉的 的 的 溶液中先滴几滴 溶液中先滴几滴 的 的 溶液,再滴加 溶液,再滴加   溶液 溶液 | 溶液迅速变蓝 |
 和
和 反应很慢的主要原因是
反应很慢的主要原因是(2)同学乙猜想实验Ⅱ中
 起催化作用,其总反应分两步进行:
起催化作用,其总反应分两步进行:(ⅰ)
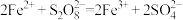 ;(ⅱ)___________。
;(ⅱ)___________。①补充反应(ⅱ):
②请你设计实验证明同学乙的猜想:
(3)查阅文献知,氧化性:
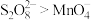 。在稀硫酸酸化的
。在稀硫酸酸化的 溶液中滴加1滴
溶液中滴加1滴 溶液作催化剂,再滴加
溶液作催化剂,再滴加 溶液,实验现象是
溶液,实验现象是实验(二):探究过二硫酸钾的热稳定性。
已知几种气体的熔点、沸点如下表所示:
| 气体 |  |  |  |
| 熔点/℃ | 16.8 | -72.7 | -218.4 |
| 沸点/℃ | 44.8 | -10 | -182.9 |
 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
(4)加热之前,先通入一段时间
 ,当观察到D中
,当观察到D中(5)B中U形管收集的物质是
(6)当A中硬质玻璃管中固体完全分解,停止加热,残留的固体产物只有一种。待冷却至室温时取少量残留固体于试管,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。A中
 完全分解发生反应的化学方程式为
完全分解发生反应的化学方程式为
您最近一年使用:0次
2022-04-13更新
|
536次组卷
|
5卷引用:甘肃省平凉市2022届高三下学期第二次模拟考试理科综合化学试题
甘肃省平凉市2022届高三下学期第二次模拟考试理科综合化学试题甘肃省兰州第一中学2022-2023学年高三上学期期中考试化学试题陕西省榆林市2022届高三第二次联考化学试题(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)热点1物质性质探究类实验
6 . 二氧化氯 是国际上公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,极易溶于水,高浓度时极易爆炸,低浓度时爆炸性降低。某化学兴趣小组设计如图装置制备二氧化氯。回答下列问题:
是国际上公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,极易溶于水,高浓度时极易爆炸,低浓度时爆炸性降低。某化学兴趣小组设计如图装置制备二氧化氯。回答下列问题:
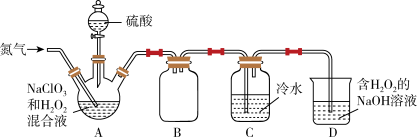
(1)装置B的作用是_______ ;制备 时,还有一种气体产生,该气体是
时,还有一种气体产生,该气体是_______ ;装置C使用冷水吸收二氧化氯的目的是_______ 。
(2)向装置A中通入氮气时流速不能过快,也不能过慢,其原因是_______ 。
(3)装置D吸收尾气,其产物之一是 。该反应的化学方程式为
。该反应的化学方程式为_______ 。
(4)测定装置C中二氧化氯溶液的浓度,步骤如下:
第一步:取20.00mL装置C中的溶液于锥形瓶中,向其中加入过量酸性KI溶液,发生反应: 。
。
第二步:加入淀粉作指示剂,向其中逐滴加入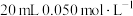 的
的 溶液至达到滴定终点,发生反应:
溶液至达到滴定终点,发生反应: 。
。
①第二步中滴定终点的标志是_______ 。
②装置C中二氧化氯溶液浓度为_______  。
。
③第二步若使用的 溶液配制已久,则测定的结果可能会
溶液配制已久,则测定的结果可能会_______ (填“偏低”、“偏高”或“无影响”)。
 是国际上公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,极易溶于水,高浓度时极易爆炸,低浓度时爆炸性降低。某化学兴趣小组设计如图装置制备二氧化氯。回答下列问题:
是国际上公认的一种安全、低毒的绿色消毒剂。熔点为-59.5℃,沸点为11.0℃,极易溶于水,高浓度时极易爆炸,低浓度时爆炸性降低。某化学兴趣小组设计如图装置制备二氧化氯。回答下列问题:
(1)装置B的作用是
 时,还有一种气体产生,该气体是
时,还有一种气体产生,该气体是(2)向装置A中通入氮气时流速不能过快,也不能过慢,其原因是
(3)装置D吸收尾气,其产物之一是
 。该反应的化学方程式为
。该反应的化学方程式为(4)测定装置C中二氧化氯溶液的浓度,步骤如下:
第一步:取20.00mL装置C中的溶液于锥形瓶中,向其中加入过量酸性KI溶液,发生反应:
 。
。第二步:加入淀粉作指示剂,向其中逐滴加入
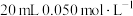 的
的 溶液至达到滴定终点,发生反应:
溶液至达到滴定终点,发生反应: 。
。①第二步中滴定终点的标志是
②装置C中二氧化氯溶液浓度为
 。
。③第二步若使用的
 溶液配制已久,则测定的结果可能会
溶液配制已久,则测定的结果可能会
您最近一年使用:0次
2022-04-12更新
|
418次组卷
|
3卷引用:甘肃省武威第七中学2022届高三下学期第七次质量检测化学试题
名校
7 . 硫代硫酸钠晶体(Na2S2O3•5H2O)俗称海波,广泛应用于照相定影及纺织业等领域。实验室利用“3SO2+2Na2S=3S↓+2Na2SO3,S+Na2SO3=Na2S2O3”原理制备Na2S2O3溶液,装置如图:

下列说法错误的是

下列说法错误的是
| A.制取SO2的反应体现了浓硫酸的酸性和氧化性 |
| B.装置B的作用是安全瓶,防倒吸 |
| C.为提高原子利用率,C中Na2S与Na2SO3物质的量之比为2:1 |
| D.该实验不足之处是缺少尾气处理装置 |
您最近一年使用:0次
2022-03-07更新
|
526次组卷
|
2卷引用:甘肃省张掖市第二中学 2021-2022学年高一下学期3月月考化学试题
名校
解题方法
8 . 某新型纳米材料氧缺位铁酸盐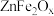 (3<x<4),能在常温下将工业废气中的
(3<x<4),能在常温下将工业废气中的 、
、 等转化为单质而除去,由锌灰(含ZnO及少量PbO、CuO、
等转化为单质而除去,由锌灰(含ZnO及少量PbO、CuO、 等)和
等)和 为原料制备氧缺位铁酸盐及其转化废气流程如图:
为原料制备氧缺位铁酸盐及其转化废气流程如图:

下列说法正确的是
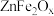 (3<x<4),能在常温下将工业废气中的
(3<x<4),能在常温下将工业废气中的 、
、 等转化为单质而除去,由锌灰(含ZnO及少量PbO、CuO、
等转化为单质而除去,由锌灰(含ZnO及少量PbO、CuO、 等)和
等)和 为原料制备氧缺位铁酸盐及其转化废气流程如图:
为原料制备氧缺位铁酸盐及其转化废气流程如图:
下列说法正确的是
| A.浸取时,为了提高酸浸效率,可以延长浸取时间或将稀硫酸换成浓硫酸 |
B.“除杂”过程中有加入足量锌粉等操作,与锌粉反应的离子只有 和 和 |
C.除去 时, 时,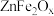 在反应中表现了氧化性 在反应中表现了氧化性 |
D. 与 与 反应制得 反应制得 时转移电子 时转移电子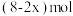 |
您最近一年使用:0次
2022-03-06更新
|
474次组卷
|
2卷引用:甘肃省张掖市第二中学 2021-2022学年高一下学期3月月考化学试题
名校
解题方法
9 . 锰锌铁氧体软磁材料(Fe2O3-MnO-ZnO)作为一种重要的电子材料在信息通讯等领域有广泛的应用,用软锰矿(主要成分 ,含
,含 、FeO、
、FeO、 、CaO、MgO等杂质)为主要原料制备软磁材料的工艺流程如下。
、CaO、MgO等杂质)为主要原料制备软磁材料的工艺流程如下。

回答下列问题:
(1)滤渣①的主要成分是_______ 。
(2)“酸浸”过程中加入过量铁粉的主要目的是_______ 。
(3)当溶液中某离子浓度小于 时,可认为该离子沉淀完全。“除钙、镁”时,加入
时,可认为该离子沉淀完全。“除钙、镁”时,加入 除尽
除尽 、
、 ,溶液中
,溶液中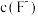 至少应为
至少应为_______ 。(已知: 和
和 的
的 分别为
分别为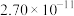 和
和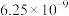 )
)
(4)“碳化”中生成碳酸锰沉淀的离子方程式为_______ 。一定条件下, 的沉淀率与温度关系如图所示。为了使
的沉淀率与温度关系如图所示。为了使 沉淀完全,最适宜的温度是
沉淀完全,最适宜的温度是_______ 。“碳化”时加入过量的 和
和 ,除了使
,除了使 沉淀完全外,其它原因是
沉淀完全外,其它原因是_______ 。

(5)“煅烧”时,碳酸亚铁发生反应的化学方程式为_______ 。
 ,含
,含 、FeO、
、FeO、 、CaO、MgO等杂质)为主要原料制备软磁材料的工艺流程如下。
、CaO、MgO等杂质)为主要原料制备软磁材料的工艺流程如下。
回答下列问题:
(1)滤渣①的主要成分是
(2)“酸浸”过程中加入过量铁粉的主要目的是
(3)当溶液中某离子浓度小于
 时,可认为该离子沉淀完全。“除钙、镁”时,加入
时,可认为该离子沉淀完全。“除钙、镁”时,加入 除尽
除尽 、
、 ,溶液中
,溶液中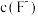 至少应为
至少应为 和
和 的
的 分别为
分别为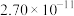 和
和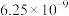 )
)(4)“碳化”中生成碳酸锰沉淀的离子方程式为
 的沉淀率与温度关系如图所示。为了使
的沉淀率与温度关系如图所示。为了使 沉淀完全,最适宜的温度是
沉淀完全,最适宜的温度是 和
和 ,除了使
,除了使 沉淀完全外,其它原因是
沉淀完全外,其它原因是
(5)“煅烧”时,碳酸亚铁发生反应的化学方程式为
您最近一年使用:0次
2022-03-04更新
|
694次组卷
|
5卷引用:甘肃省张掖市2021-2022学年高三第二次全市联考(3月)理综化学试题
甘肃省张掖市2021-2022学年高三第二次全市联考(3月)理综化学试题福建省莆田市2022届高三下学期第二次质量检测化学试题山西省名校2021-2022学年高一下学期期中联合考试化学试题(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)(已下线)秘籍18 工艺流程新情景方程式书写-备战2022年高考化学抢分秘籍(全国通用)
10 . 钒不同价态的化合物广泛用于电池等行业。根据反应: +5VO2++H2O=______+Mn2++5VO
+5VO2++H2O=______+Mn2++5VO 。下列说法正确的是
。下列说法正确的是
 +5VO2++H2O=______+Mn2++5VO
+5VO2++H2O=______+Mn2++5VO 。下列说法正确的是
。下列说法正确的是| A.上述方程式空白处应填入“2OH-” |
B.VO2+是氧化剂,VO 是还原剂 是还原剂 |
| C.VO2+是还原剂,1molVO2+转移电子的物质的量为1mol |
D. 是常见氧化剂,酸性条件下被氧化成Mn2+ 是常见氧化剂,酸性条件下被氧化成Mn2+ |
您最近一年使用:0次
2022-01-24更新
|
222次组卷
|
5卷引用:甘肃省兰州西北师范大学附属中学2022-2023学年高一上学期期中考试化学试题



