1 . 如图是某化学反应的微观示意图。下列有关说法正确的是


| A.该反应是复分解反应 |
B.反应方程式为NH3+O2 H2O+N2 H2O+N2 |
| C.生成物丙、丁的质量比为9:14 |
| D.反应前后只有一种元素的化合价不变 |
您最近一年使用:0次
2021-08-31更新
|
198次组卷
|
6卷引用:陕西省宝鸡市千阳县中学2022-2023学年新高一开学考试化学试题
2 . 由废铅蓄电池的铅膏采用氯盐法制备PbCl2的工艺流程如图:
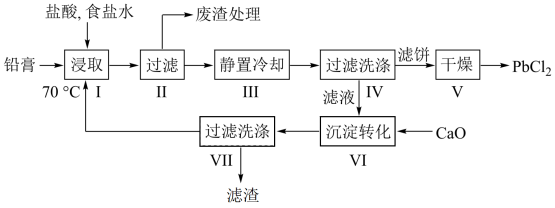
已知:①铅膏的组成如表:
②PbCl2是白色结晶性粉末,微溶于冷水,易溶于热水、浓盐酸和氢氧化钠溶液。
回答下列问题:
(1)铅膏“浸取”时浓盐酸与水的配比(浓盐酸和水的体积比)及氯化钠的浓度均对铅浸取率有较大影响(如图所示):
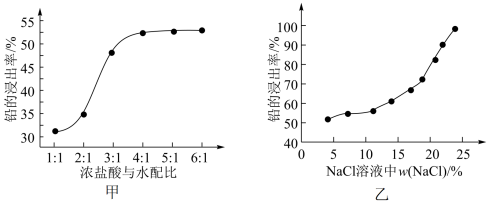
①由图甲确定适宜的配比为_______ 。
②已知70 °C时,NaCl的溶解度为37.8 g,由图乙可知铅的浸出率与NaCl质量分数的关系是_______ ,工业上采用质量分数约为24%的食盐水,不能采用无限制提高w(NaCl)来提高铅的浸出率,其原因是_______ 。
③提高铅的浸出率除浓盐酸与水的配比和w(NaC)外,还可采取的措施有_______ (至少写2种)。
(2)步骤Ⅵ加入CaCl2的目的是_______ .步骤Ⅶ滤液中溶质的主要成分为_______ 。
(3)“浸取”时会发生一系列反应。
①硫酸铅溶于氯化钠生成PbCl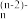 的离子方程式为
的离子方程式为_______ 。
②产生氯气的化学方程式为_______ 。

已知:①铅膏的组成如表:
| 物相 | PbO | PbO2 | PbSO4 | Pb | 总铅 |
| 质量分数/% | 15.89 | 4.86 | 33.74 | 34.03 | 76.05 |
②PbCl2是白色结晶性粉末,微溶于冷水,易溶于热水、浓盐酸和氢氧化钠溶液。
回答下列问题:
(1)铅膏“浸取”时浓盐酸与水的配比(浓盐酸和水的体积比)及氯化钠的浓度均对铅浸取率有较大影响(如图所示):

①由图甲确定适宜的配比为
②已知70 °C时,NaCl的溶解度为37.8 g,由图乙可知铅的浸出率与NaCl质量分数的关系是
③提高铅的浸出率除浓盐酸与水的配比和w(NaC)外,还可采取的措施有
(2)步骤Ⅵ加入CaCl2的目的是
(3)“浸取”时会发生一系列反应。
①硫酸铅溶于氯化钠生成PbCl
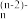 的离子方程式为
的离子方程式为②产生氯气的化学方程式为
您最近一年使用:0次
3 . 三氯化氮(NCl3)是一种强氧化剂,工业上可用于漂白和消毒,实验室可由氯气通入碳酸铵溶液中制得。某化学小组利用此原理进行实验室制备三氯化氮。
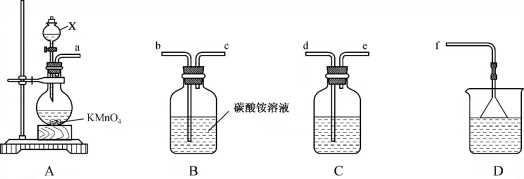
回答下列问题:
(1)装置A中仪器X的名称是_______ ,盛放的试剂是_______ ,装置A中发生反应的离子方程式为_______ 。
(2)整个装置的导管连接顺序为a→_______ →_______ →_______ →_______ →_______ 。
(3)装置B中发生反应的化学方程式为_______ 。
(4)装置C的作用为_______ 。装置D的作用为_______ 。
(5)三氯化氮浓度的测定:准确量取20mL装置B中反应后的溶液,置于100mL容量瓶中,用水稀释至刻度,摇匀,吸取25.0mL于烧杯中,加入足量V1mLc1mol·L-1亚硫酸钠溶液,充分反应后,向烧杯中加入足量V2mLc2mol·L-1盐酸酸化的氯化钡溶液,得沉淀mg。
已知:i._______ Na2SO3+_______ NCl3 +_______=_______Na2SO4 +_______ HCl+ _______NH4Cl;
ii. BaCl2 +Na2SO4=BaSO↓+ 2HCl。
①请完成反应i的化学方程式:i._______ Na2SO3+_______ NCl3+_______=Na2SO4+_______ HCl+_______ NH4Cl
_______
②装置B反应后的溶液中三氯化氮的浓度为_______ mol·L-1。

回答下列问题:
(1)装置A中仪器X的名称是
(2)整个装置的导管连接顺序为a→
(3)装置B中发生反应的化学方程式为
(4)装置C的作用为
(5)三氯化氮浓度的测定:准确量取20mL装置B中反应后的溶液,置于100mL容量瓶中,用水稀释至刻度,摇匀,吸取25.0mL于烧杯中,加入足量V1mLc1mol·L-1亚硫酸钠溶液,充分反应后,向烧杯中加入足量V2mLc2mol·L-1盐酸酸化的氯化钡溶液,得沉淀mg。
已知:i._______ Na2SO3+_______ NCl3 +_______=_______Na2SO4 +_______ HCl+ _______NH4Cl;
ii. BaCl2 +Na2SO4=BaSO↓+ 2HCl。
①请完成反应i的化学方程式:i._______ Na2SO3+_______ NCl3+_______=Na2SO4+_______ HCl+_______ NH4Cl
②装置B反应后的溶液中三氯化氮的浓度为
您最近一年使用:0次
2021-06-16更新
|
761次组卷
|
3卷引用:陕西省宝鸡市2021届高三下学期5月大联考理综化学试题
名校
解题方法
4 . 某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中含有 70.0%及一定量的
70.0%及一定量的 、
、 、
、 和有机物,镍及其化合物的化学性质与铁的类似,但
和有机物,镍及其化合物的化学性质与铁的类似,但 的性质较稳定)。回答下列问题:
的性质较稳定)。回答下列问题:

已知:部分阳离子以氢氧化物的形式完全沉淀时的 如下表所示。
如下表所示。
(1)滤渣a的成分是___________ ,用乙醇洗涤废催化剂的目的是___________ ,从废液中回收乙醇的方法是___________
(2)为提高酸浸速率,可采取的措施有___________ (答一条即可)
(3)硫酸酸浸后所得滤液A中可能含有的金属离子是___________ ,向其中加入 的目的是
的目的是___________ ,反应的离子方程式为___________
(4)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,与电镀相比,化学镀的最大优点是___________
(5)滤液C进行如下所示处理可以制得 。滤液C
。滤液C 溶液D
溶液D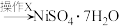
①操作X的名称是___________
② 在强碱溶液中用
在强碱溶液中用 氧化,可制得碱性镍镉电池电极材料—
氧化,可制得碱性镍镉电池电极材料—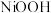 ,该反应的离子方程式是
,该反应的离子方程式是___________
 70.0%及一定量的
70.0%及一定量的 、
、 、
、 和有机物,镍及其化合物的化学性质与铁的类似,但
和有机物,镍及其化合物的化学性质与铁的类似,但 的性质较稳定)。回答下列问题:
的性质较稳定)。回答下列问题:
已知:部分阳离子以氢氧化物的形式完全沉淀时的
 如下表所示。
如下表所示。| 沉淀物 |  |  |  |  |
 | 5.2 | 3.2 | 9.7 | 9.2 |
(1)滤渣a的成分是
(2)为提高酸浸速率,可采取的措施有
(3)硫酸酸浸后所得滤液A中可能含有的金属离子是
 的目的是
的目的是(4)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,与电镀相比,化学镀的最大优点是
(5)滤液C进行如下所示处理可以制得
 。滤液C
。滤液C 溶液D
溶液D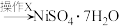
①操作X的名称是
②
 在强碱溶液中用
在强碱溶液中用 氧化,可制得碱性镍镉电池电极材料—
氧化,可制得碱性镍镉电池电极材料—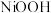 ,该反应的离子方程式是
,该反应的离子方程式是
您最近一年使用:0次
2021-05-23更新
|
547次组卷
|
2卷引用:陕西省宝鸡市陈仓区2021届高三第一次质量检测化学试题
解题方法
5 . 钼酸钠(Na2MoO4)是一种冷却水系统的金属缓蚀剂,工业上通常利用钼精矿(MoS2中硫为-2价)制备金属钼和钼酸钠晶体的流程如图所示。

回答下列问题:
(1)在空气中焙烧时产生对环境有危害气体的化学式是___________ ,焙烧的化学方程式是___________ 。
(2)操作1的实验名称是___________ ,由此可推测MoO3为___________ 性氧化物,该反应的离子方程式为___________ ,进行操作2的步骤是___________ ,过滤、洗涤、干燥。
(3)操作3中硫元素被氧化为最高价,发生反应的离子方程式为___________ 。
(4)钼精矿中MoS2的测定:取钼精矿20g经操作3等,得到Mo的质量为8.64g,假设过程中钼利用率为90%,钼精矿中MoS2的质量分数为___________ 。
(5)电解法制备:用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如图甲所示。b电极上的电极反应式为___________ ,电解槽中使用___________ (填阳离子或阴离子)交换膜。某温度下,BaMoO4在水中的沉淀溶解平衡曲线如图乙所示,要使溶液中钼酸根离子完全沉淀(浓度小于1×10-5mol•l-1),Ba2+的浓度最小为___________ mol•l-1。


回答下列问题:
(1)在空气中焙烧时产生对环境有危害气体的化学式是
(2)操作1的实验名称是
(3)操作3中硫元素被氧化为最高价,发生反应的离子方程式为
(4)钼精矿中MoS2的测定:取钼精矿20g经操作3等,得到Mo的质量为8.64g,假设过程中钼利用率为90%,钼精矿中MoS2的质量分数为
(5)电解法制备:用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如图甲所示。b电极上的电极反应式为

您最近一年使用:0次
解题方法
6 . 对于下列实验,能正确描述其反应的离子方程式是
| A.硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2 + 4H+ = 2I2+2H2O |
| B.向CaCl2溶液中通入CO2:Ca2++H2O+CO2 = CaCO3↓+2H+ |
| C.水垢上滴入CH3COOH溶液有气泡产生:CaCO3+2H+ = Ca2++CO2↑+ H2O |
| D.SO2通入漂白粉溶液中产生白色浑浊:SO2+Ca2++2ClO-+H2O = CaSO3↓+2HClO |
您最近一年使用:0次
2020-11-15更新
|
142次组卷
|
2卷引用:陕西省宝鸡市金台区2021届高三11月检测理综化学试题
解题方法
7 . (1)H2O2水溶液称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口,对下列两个涉及H2O2的反应,填写下列空白:
A.H2O2 + Cl2 = 2HCl + O2 B.H2O2 + 2 + 2H+ = I2 + 2H2O
+ 2H+ = I2 + 2H2O
① H2O2仅体现氧化性的反应是___________ (填代号,下同)
② H2O2仅体现还原性的是_______________
(2)已知CuO具有氧化性,能够与NH3反应生成两种单质和H2O,请写出在加热条件下CuO与NH3反应的化学方程式_________________ ;
(3)在一定条件下, 与Cl2反应如下:
与Cl2反应如下: + Cl2 + 2OH- =
+ Cl2 + 2OH- = 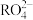 + 2Cl- + H2O,由以上反应可知上述过程中RO
+ 2Cl- + H2O,由以上反应可知上述过程中RO 被
被______ (填“氧化”或“还原”), 元素R的化合价是
元素R的化合价是______ 。
(4)已知如下反应,请针对下述两个反应回答问题:
A 2H2O+Cl2+SO2=H2SO4+2HCl
B 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
① 两反应中的氧化剂的氧化性强弱顺序为________ ,还原剂的还原性强弱顺序为________ (用物质的化学式表示)。
② 在反应②中氯化氢表现出的性质是________ 。
a.还原性 b.酸性 c.氧化性
A.H2O2 + Cl2 = 2HCl + O2 B.H2O2 + 2
 + 2H+ = I2 + 2H2O
+ 2H+ = I2 + 2H2O① H2O2仅体现氧化性的反应是
② H2O2仅体现还原性的是
(2)已知CuO具有氧化性,能够与NH3反应生成两种单质和H2O,请写出在加热条件下CuO与NH3反应的化学方程式
(3)在一定条件下,
 与Cl2反应如下:
与Cl2反应如下: + Cl2 + 2OH- =
+ Cl2 + 2OH- = 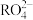 + 2Cl- + H2O,由以上反应可知上述过程中RO
+ 2Cl- + H2O,由以上反应可知上述过程中RO 被
被 元素R的化合价是
元素R的化合价是(4)已知如下反应,请针对下述两个反应回答问题:
A 2H2O+Cl2+SO2=H2SO4+2HCl
B 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
① 两反应中的氧化剂的氧化性强弱顺序为
② 在反应②中氯化氢表现出的性质是
a.还原性 b.酸性 c.氧化性
您最近一年使用:0次
2020-11-13更新
|
145次组卷
|
2卷引用:陕西省宝鸡市金台区2020-2021学年高一上学期期中考试化学试题1
名校
解题方法
8 . 下列解释有关实验现象的离子方程式错误的是
| 选项 | 实验操作 | 实验现象 | 离子方程式 |
| A | 大理石中加入足量醋酸溶液 | 大理石逐渐溶解 | CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
| B | 新制氯水中加过量氢氧化钠溶液 | 溶液由黄绿色变无色 | Cl2+2OH-=Cl-+ClO-+H2O |
| C | 酸性KMnO4溶液中加H2O2溶液 | 溶液紫色褪去,有气泡产生 | 2MnO +3H2O2+10H+=2Mn2++3O2↑+8H2O +3H2O2+10H+=2Mn2++3O2↑+8H2O |
| D | 将稀硫酸滴入淀粉-KI溶液中 | 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I-+O2=2I2+2H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-10更新
|
537次组卷
|
8卷引用:陕西省宝鸡市眉县槐芽高中2021届高三下学期第二次月考化学试题
解题方法
9 . 按指定元素的价态变化,各写一个化学方程式(每个化学方程式只能用一次)。
(1) →
→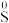 :
:___ ;
(2) →
→ :
:___ ;
(3)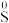 →
→ :
:___ ;
(4)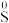 →
→ :
:___ 。
(1)
 →
→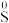 :
:(2)
 →
→ :
:(3)
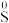 →
→ :
:(4)
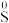 →
→ :
:
您最近一年使用:0次
解题方法
10 . 2019年国庆阅兵上,新一代预警机、无人机、东风 战略核导弹等一批国产武器装备精彩亮相、震撼人心。它们不仅是捍卫国家安全和民族尊严的利器,更是我们每个中国人幸福生活的保障。导弹、装备的制造和化学密不可分,请配平下列方程式:
战略核导弹等一批国产武器装备精彩亮相、震撼人心。它们不仅是捍卫国家安全和民族尊严的利器,更是我们每个中国人幸福生活的保障。导弹、装备的制造和化学密不可分,请配平下列方程式:
(1)______ 
______ 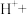
______ 
______ 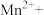
______ 
______ 
(2)______ 
______ 
______ S↓______ 
______ 
 战略核导弹等一批国产武器装备精彩亮相、震撼人心。它们不仅是捍卫国家安全和民族尊严的利器,更是我们每个中国人幸福生活的保障。导弹、装备的制造和化学密不可分,请配平下列方程式:
战略核导弹等一批国产武器装备精彩亮相、震撼人心。它们不仅是捍卫国家安全和民族尊严的利器,更是我们每个中国人幸福生活的保障。导弹、装备的制造和化学密不可分,请配平下列方程式:(1)

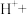



(2)




您最近一年使用:0次



