名校
解题方法
1 . 光催化技术是指利用半导体材料在光照条件下激发产生强氧化性物质,将空气中的污染物分解为CO2、H2O等小分子,Bi2MoO6对可见光有较强的响应,在光催化领域具有稳定高效的催化效果,其制备方法如下:
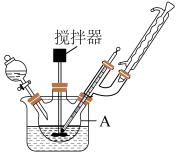
(一)微球状前驱体BiOI的制备
I.向反应仪器A中加入无水乙醇,并加入agBi(NO3)3·5H2O固体和足量KI固体,常温下搅拌30min至溶解完全。
Ⅱ.由分液漏斗滴加氨水调节溶液pH为7后,将反应装置放入油浴中,在80℃下回流3h。
Ⅲ.抽滤收集反应后的砖红色沉淀,经洗涤、干燥后研磨备用。
(二)Bi2MoO6的制备
Ⅳ.将上述制备得到的BiOI,足量Na2MoO4·2H2O和去离子水加入反应釜中,调节体系pH为7后,将反应釜密封好,于150℃下反应24h,自然冷却到室温,抽滤所得沉淀,经洗涤、干燥后得最终产物bg。
已知:①Bi(OH)3的Ksp为6.0×10-31;②Bi(NO3)3·5H2O和KI均可溶于乙醇;③Bi(NO3)3·5H2O的摩尔质量为485g·mol-1,Bi2MoO6的摩尔质量为610g·mol-1。
回答下列问题:
(1)制备BiOI的反应仪器A的名称是___________ 。
(2)I中不选择水作溶剂的主要原因是___________ 。
(3)Ⅱ中加入氨水后,发生反应的离子方程式为___________ 。
(4)Ⅱ中反应需在中性环境下进行。
①不可呈酸性的主要原因是___________ ,
②不可呈碱性的主要原因是___________ 。
(5)Ⅳ中反应的离子方程式为___________ 。
(6)Bi2MoO6的产率为___________ ×100%(用含a,b的代数式表示)。

(一)微球状前驱体BiOI的制备
I.向反应仪器A中加入无水乙醇,并加入agBi(NO3)3·5H2O固体和足量KI固体,常温下搅拌30min至溶解完全。
Ⅱ.由分液漏斗滴加氨水调节溶液pH为7后,将反应装置放入油浴中,在80℃下回流3h。
Ⅲ.抽滤收集反应后的砖红色沉淀,经洗涤、干燥后研磨备用。
(二)Bi2MoO6的制备
Ⅳ.将上述制备得到的BiOI,足量Na2MoO4·2H2O和去离子水加入反应釜中,调节体系pH为7后,将反应釜密封好,于150℃下反应24h,自然冷却到室温,抽滤所得沉淀,经洗涤、干燥后得最终产物bg。
已知:①Bi(OH)3的Ksp为6.0×10-31;②Bi(NO3)3·5H2O和KI均可溶于乙醇;③Bi(NO3)3·5H2O的摩尔质量为485g·mol-1,Bi2MoO6的摩尔质量为610g·mol-1。
回答下列问题:
(1)制备BiOI的反应仪器A的名称是
(2)I中不选择水作溶剂的主要原因是
(3)Ⅱ中加入氨水后,发生反应的离子方程式为
(4)Ⅱ中反应需在中性环境下进行。
①不可呈酸性的主要原因是
②不可呈碱性的主要原因是
(5)Ⅳ中反应的离子方程式为
(6)Bi2MoO6的产率为
您最近一年使用:0次
2023-05-17更新
|
151次组卷
|
2卷引用:江西省宜春市宜丰中学创新部2023-2024学年高三上学期期中考试化学试题
名校
解题方法
2 . 室温下,通过下列实验探究0.1 NaHS溶液的性质。
NaHS溶液的性质。
下列有关说法正确的是
 NaHS溶液的性质。
NaHS溶液的性质。| 实验 | 实验操作和现象 |
| ① | 滴加几滴酚酞溶液,溶液变红 |
| ② | 加入等体积0.1 NaOH溶液充分混合,无明显现象 NaOH溶液充分混合,无明显现象 |
| ③ | 加入少量 溶液,产生黑色沉淀 溶液,产生黑色沉淀 |
| ④ | 加入适量NaClO溶液,有淡黄色沉淀产生 |
A.实验①溶液中: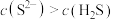 |
B.实验②所得溶液中: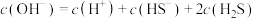 |
C.实验③反应后静置一段时间,上层清液中存在: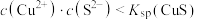 |
D.实验④中反应的离子方程式: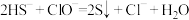 |
您最近一年使用:0次
2023-05-12更新
|
544次组卷
|
3卷引用:江西师范大学附属中学2023-2024学年高三上学期期中考试化学试题
江西师范大学附属中学2023-2024学年高三上学期期中考试化学试题天津市南开区2023届高三下学期质量监测 ( 二 ) 化学试题(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)
名校
3 . 某温度下,Ksp(MnS)=2×10-13,Ksp(PbS)=2×10-28,生产中用MnS作为沉淀剂除去工业废水中Pb2+,其反应原理为Pb2+(aq)+MnS(s) PbS(s)+Mn2+(aq)。下列说法正确的是
PbS(s)+Mn2+(aq)。下列说法正确的是
 PbS(s)+Mn2+(aq)。下列说法正确的是
PbS(s)+Mn2+(aq)。下列说法正确的是| A.该反应的平衡常数K=1015 |
| B.PbS悬浊液中:c(Pb2+)=1×10-14mol•L-1 |
| C.该反应达平衡时c(Mn2+)=c(Pb2+) |
| D.其他条件不变,使平衡体系中c(Mn2+)增大,则c(Pb2+)减小 |
您最近一年使用:0次
2023-05-11更新
|
328次组卷
|
5卷引用:江西省部分学校2023-2024学年高二上学期1月期末化学试题
4 . 化学与日常生活、工业生产息息相关。下列说法不正确的是
| A.天然气的主要成分甲烷,是高效、较洁净的燃料 |
| B.氯乙烷沸点低易汽化,常用于运动员受伤时局部麻醉处理 |
| C.汽油、煤油、柴油等石油分馏的产物,属于不可再生能源 |
| D.工业上可用Na2S和FeS除去废水中的Hg2+,是利用了S2-的还原性 |
您最近一年使用:0次
2023-05-09更新
|
138次组卷
|
2卷引用:江西省赣州市寻乌中学2022-2023学年高二下学期6月月考化学试题
名校
解题方法
5 . 已知:室温下氢硫酸 的电离常数
的电离常数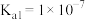 ,
,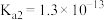 ;
; 和
和 的
的 分别为
分别为 、
、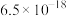 ,下列说法不正确的是
,下列说法不正确的是
 的电离常数
的电离常数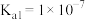 ,
,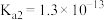 ;
; 和
和 的
的 分别为
分别为 、
、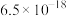 ,下列说法不正确的是
,下列说法不正确的是A.反应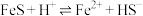 的平衡常数 的平衡常数 的数值为 的数值为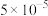 |
B.可以用 除去污水中的 除去污水中的 |
C.从上述数据可得出 难溶于稀硫酸中 难溶于稀硫酸中 |
D. 的 的 溶液中加入等体积 溶液中加入等体积 的 的 溶液,则有: 溶液,则有: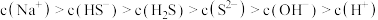 |
您最近一年使用:0次
2023-05-06更新
|
603次组卷
|
3卷引用:江西省鹰潭市余江区第一中学2023-2024学年高三下学期二模考试化学试题
6 . 下列有关实验操作、现象与结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯加热,熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| B | 向10mL0.1mol•L-1Na2S溶液中滴入2mL0.1mol•L-1ZnSO4溶液,再加入2mL0.1mol•L-1CuSO4溶液,先生成白色沉淀,后生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| C | 充分加热铁粉和硫粉的混合物,冷却后取少量固体于试管中,加入足量稀硫酸,再滴入K3[Fe(CN)6]溶液,产生蓝色沉淀 | 无法充分说明铁被硫氧化至二价铁Fe(Ⅱ) |
| D | 某钾盐晶体中滴入浓盐酸,产生的气体通入品红溶液中,品红溶液褪色 | 产生的气体一定是SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 化学与社会、生活密切相关。下列说法不正确的是
| A.打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释 |
| B.纯铁比生铁易生锈 |
| C.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用盐酸除去 |
| D.掩埋废旧电池会造成环境污染 |
您最近一年使用:0次
2023-04-23更新
|
93次组卷
|
3卷引用:江西省宜春市宜丰中学2023届高三模拟预测化学试题
8 . 常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为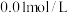 的KCl、
的KCl、 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述
的水解)。下列叙述不正确 的是
 溶液分别滴定浓度均为
溶液分别滴定浓度均为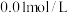 的KCl、
的KCl、 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述
的水解)。下列叙述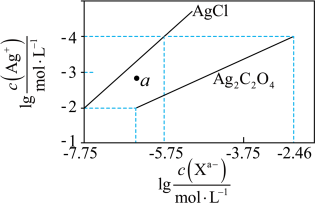
A.计算可得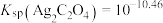 |
| B.a点表示的是AgCl的不饱和溶液 |
C.向 的混合液中滴入 的混合液中滴入 溶液时,先生成AgCl沉淀 溶液时,先生成AgCl沉淀 |
D.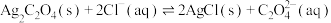 的平衡常数为 的平衡常数为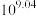 |
您最近一年使用:0次
2023-04-21更新
|
545次组卷
|
5卷引用:江西省宜春市宜丰中学2023届高三模拟预测化学试题
江西省宜春市宜丰中学2023届高三模拟预测化学试题浙江省9+1联盟2022-2023学年高二下学期期中考试化学试题(已下线)【2023】【高二下】【期中考】【9+1联盟】【高中化学】【洪翔峰收集】上海市进才中学2023-2024学年高二下学期3月测试化学试题河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期12月考试化学试题
名校
9 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2支均盛有2mL相同浓度的 溶液的试管中,分别滴入2滴相同浓度的KCl、KI溶液,前者无明显现象,后者有黄色沉淀 溶液的试管中,分别滴入2滴相同浓度的KCl、KI溶液,前者无明显现象,后者有黄色沉淀 |  |
| B | 将红热的木炭放入盛有浓硝酸的试管中,试管中有红棕色气体产生 | 木炭与浓硝酸反应产生 |
| C | 用pH试纸测得: 溶液的pH约为9, 溶液的pH约为9, 溶液的pH约为8 溶液的pH约为8 |  电离出 电离出 的能力比 的能力比 的强 的强 |
| D | 向盛有相同浓度 溶液的两支试管中,分别滴加淀粉溶液和 溶液的两支试管中,分别滴加淀粉溶液和 溶液,前者溶液变蓝,后者有黄色沉淀 溶液,前者溶液变蓝,后者有黄色沉淀 | 溶液中可能存在平衡: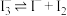 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-13更新
|
187次组卷
|
5卷引用:江西省大余中学2022-2023学年高二下学期4月期中考试化学试题
名校
10 . 已知常温下水溶液中 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ]随pH变化曲线如图1;溶液中
]随pH变化曲线如图1;溶液中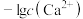 和
和 关系如图2.用
关系如图2.用
 溶液滴定20.00mL
溶液滴定20.00mL
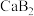 溶液,下列说法错误的是
溶液,下列说法错误的是

 、
、 、
、 、HB、
、HB、 的分布分数δ[如
的分布分数δ[如 ]随pH变化曲线如图1;溶液中
]随pH变化曲线如图1;溶液中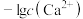 和
和 关系如图2.用
关系如图2.用
 溶液滴定20.00mL
溶液滴定20.00mL
 溶液,下列说法错误的是
溶液,下列说法错误的是
| A.曲线d表示δ(HB) |
B. 的水解平衡常数 的水解平衡常数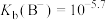 |
| C.滴定过程中溶液会变浑浊 |
D.滴定过程中始终存在: |
您最近一年使用:0次
2023-04-10更新
|
1851次组卷
|
12卷引用:江西省宜丰中学创新部2023-2024学年高二上学期第一次(10月)月考化学试题
江西省宜丰中学创新部2023-2024学年高二上学期第一次(10月)月考化学试题河北省石家庄市部分学校2023届高中毕业年级教学质量检测(二)(一模)化学试题河北省邢台市2022-2023学年高三下学期4月第一次模拟考试化学试题(已下线)专题15 水溶液中的离子平衡山东省东营市第一中学2023届高三下学期二模化学试题东北育才学校高中部2023届高三下学期适应性考试化学试题重庆市七校2023-2024学年高三上学期开学考试化学试题湖南省长郡中学2024届高三上学期月考卷(一)化学试题湖南省长沙市长郡中学2024届高三上学期9月月考化学试题四川省宜宾市叙州区第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)化学(九省联考考后提升卷,河南卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点18 电解质溶液图像分析



