1 . 我国古代四大发明之一的黑火药爆炸时发生的反应为2KNO3+S+3C=K2S+N2↑+3CO2↑。生成物K2S的晶体结构如图。下列有关说法错误的是


| A.反应产物中有两种非极性分子 |
| B.1mol CO2和1mol N2含有的π键数目之比为1:1 |
| C.K2S晶体中阴离子周围最近的阳离子有4个 |
D.若K2S晶体的晶胞边长为a nm,则该晶体的密度为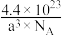 g·cm-3 g·cm-3 |
您最近一年使用:0次
2024-02-06更新
|
465次组卷
|
2卷引用:辽宁省铁岭市某校2023-2024学年高二上学期第二次阶段考试化学试题
名校
解题方法
2 . 化学反应中既有物质变化,也有能量变化。这些变化与化学反应的条件、限度、速率等因素有关。
(1)已知NH4F溶液呈酸性,则水解程度
___________ F-(填“>”、“<”或“=”),稀释后溶液中 的值将会
的值将会 ___________ (填“增大”、“减小”或“不变”)。
(2)某温度下,在体积为5L的密闭容器内发生如下反应:
CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0
①在上述反应的反应物与生成物中,非极性分子为:___________ 。
②上述反应中各物质反应速率之间的关系为:___________ 。
③若反应20min后气体总物质的量增加了10mol,则甲烷的平均反应速率为___________ 。
④下列选项中的物理量不变时,一定可以判断反应达到平衡的是___________ 。
A.容器内氢元素的质量分数
B.容器内气体的密度
C.容器内气体的压强
D.容器内气体的平均相对分子质量
⑤在某一时刻,v正=v逆=v0,反应若改变某一条件,可使得v正<v逆<v0,指出可以改变的条件___________ 。
⑥已知CO与H2合成CH3OH是可逆反应:CO+2H2⇌CH3OH,若上述反应达到平衡时CO与H2的转化率相同,则投料比n(CO):n(H2)=___________ 。
(1)已知NH4F溶液呈酸性,则水解程度

 的值将会
的值将会 (2)某温度下,在体积为5L的密闭容器内发生如下反应:
CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0
①在上述反应的反应物与生成物中,非极性分子为:
②上述反应中各物质反应速率之间的关系为:
③若反应20min后气体总物质的量增加了10mol,则甲烷的平均反应速率为
④下列选项中的物理量不变时,一定可以判断反应达到平衡的是
A.容器内氢元素的质量分数
B.容器内气体的密度
C.容器内气体的压强
D.容器内气体的平均相对分子质量
⑤在某一时刻,v正=v逆=v0,反应若改变某一条件,可使得v正<v逆<v0,指出可以改变的条件
⑥已知CO与H2合成CH3OH是可逆反应:CO+2H2⇌CH3OH,若上述反应达到平衡时CO与H2的转化率相同,则投料比n(CO):n(H2)=
您最近一年使用:0次
名校
3 . 物质的结构决定其性质。下列实例与解释不相符的是
| 选项 | 实例 | 解释 |
| A |  比 比 酸性强 酸性强 |  的电负性比 的电负性比 的电负性强,吸电子能力强,使羟基的极性增强,更容易电离 的电负性强,吸电子能力强,使羟基的极性增强,更容易电离 |
| B |  的沸点高于 的沸点高于 |  的非金属性强于 的非金属性强于 |
| C |  比 比 的稳定性高 的稳定性高 |  键的键能比 键的键能比 键的键能大 键的键能大 |
| D |  在 在 中的溶解度大于在 中的溶解度大于在 中的溶解度 中的溶解度 | 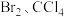 为非极性分子, 为非极性分子, 为极性分子 为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-04更新
|
195次组卷
|
3卷引用:河北省唐山市2023-2024学年高三上学期期末考试化学试题
4 . 下列物质结构与性质或物质性质与用途对应关系不正确的是
A. 与 与 均属于非极性分子,可用 均属于非极性分子,可用 萃取碘水中的 萃取碘水中的 |
| B.石墨晶体的层状结构间存在分子间作用力,可作为导电电极 |
| C.葡萄糖具有还原性,能发生银镜反应,可用于工业制镜 |
| D.SiC中原子以共价键形成空间网状结构,可作砂轮的磨料 |
您最近一年使用:0次
名校
解题方法
5 . 病毒核酸保存液中的胍盐(可由胍与盐酸反应制得,胍的结构简式如下图所示)能使蛋白质变性,胍盐在碱性溶液中水解产物中含有氨和尿素[ ]。下列说法
]。下列说法不正确 的是
 ]。下列说法
]。下列说法
| A.胍的水溶液呈碱性 | B.HCl分子属于极性分子 |
| C.1个尿素分子中含有8个σ键 | D.尿素晶体为分子晶体 |
您最近一年使用:0次
名校
6 . 依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是___________ 。
(2)基态铁原子有___________ 个未成对电子,基态 的价电子排布图为
的价电子排布图为___________ 。
(3)下列说法错误的是___________(填字母)。
(4)过氧化氢( )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。

① 的电子式为
的电子式为___________ ,结构式为___________ 。
② 中存在
中存在___________ 键和___________ 键,为___________ (填“极性”或“非极性”)分子。
(1)基态硅原子的电子排布式是
(2)基态铁原子有
 的价电子排布图为
的价电子排布图为(3)下列说法错误的是___________(填字母)。
A.元素的电负性: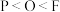 | B.元素的第一电离能: |
C.离子半径: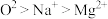 | D.原子的未成对电子数: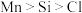 |
(4)过氧化氢(
 )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。
①
 的电子式为
的电子式为②
 中存在
中存在
您最近一年使用:0次
2024-02-03更新
|
339次组卷
|
2卷引用:河南省周口市西华县第一高级中学2023-2024学年高二上学期月考化学试卷
解题方法
7 . 已知O3的空间结构为V形,分子中正电中心和负电中心不重合,下列有关说法正确的是
A. 分子含有的化学键为非极性共价键 分子含有的化学键为非极性共价键 |
B. 分子为非极性分子 分子为非极性分子 |
C. 转化为 转化为 为物理变化 为物理变化 |
D. 在水中溶解度比O2在水中溶解度大 在水中溶解度比O2在水中溶解度大 |
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法不正确的是

下列说法不正确的是
A.沸点: |
| B.CA3分子是非极性分子 |
| C.C形成的单质中σ键与π键个数之比为1:2 |
| D.B、C、D形成的气态氢化物的稳定性依次增强 |
您最近一年使用:0次
名校
解题方法
9 . 下列叙述正确的是
| A.硝酸银溶液中加入氨水先产生沉淀,后沉淀溶解消失 |
B.分子键角由大到小为: |
| C.焰色反应与电子跃迁有关,是化学变化 |
D. 和 和 是中心原子杂化类型不相同的极性分子 是中心原子杂化类型不相同的极性分子 |
您最近一年使用:0次
名校
解题方法
10 . 氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的关键环节。
Ⅰ. 可用作储存氢气的材料,结构如下图所示。
可用作储存氢气的材料,结构如下图所示。
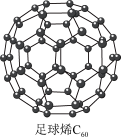
(1)继 后,科学家合成了
后,科学家合成了 、
、 ,三者结构相似。下列说法正确的是
,三者结构相似。下列说法正确的是_______ (填序号)
A. 、
、 、
、 都属于共价晶体
都属于共价晶体
B.由于N-N键能小于 ,故
,故 的稳定性弱于
的稳定性弱于
C.由于C-C键长小于Si-Si键,所以 熔沸点低于
熔沸点低于
Ⅱ.是储氢材料,已知其由 和
和 构成,释放氢气的原理为
构成,释放氢气的原理为 。
。
(2) 中不存在的作用力有
中不存在的作用力有___________ (填序号)。
A.离子键 B.共价键 C.分子间作用力
(3)氢化锂(LiH)是离子化合物,写出其电子式___________ ,LiH中离子半径较大的是___________ ,其原因是___________ 。
Ⅲ.汽车安全气囊中的填充物有 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和氮气。完成下列填空:
遇撞击时能生成金属钠和氮气。完成下列填空:
(4)写出 的电子式:
的电子式:___________ 。
(5) 和
和 是两种不同的化合物,
是两种不同的化合物, 是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。 晶体中存在的化学键类型有
晶体中存在的化学键类型有___________ , 遇
遇 会水解而产生
会水解而产生 和
和 ,
, 晶体中存在的化学键类型有
晶体中存在的化学键类型有___________ 。
(6)汽车安全气囊填充物的三种物质中属于共价化合物的是___________ (填写化学式),所涉及的5种元素中,原子半径最大的是___________ (填写元素符号)。
(7)该题中出现的极性分子有___________ 。
(8)渗氮工艺已经成为钢材处理的重要手段,已知一种磁性氮化铁晶胞如下图,该物质的化学式是___________ 。

Ⅰ.
 可用作储存氢气的材料,结构如下图所示。
可用作储存氢气的材料,结构如下图所示。
(1)继
 后,科学家合成了
后,科学家合成了 、
、 ,三者结构相似。下列说法正确的是
,三者结构相似。下列说法正确的是A.
 、
、 、
、 都属于共价晶体
都属于共价晶体B.由于N-N键能小于
 ,故
,故 的稳定性弱于
的稳定性弱于
C.由于C-C键长小于Si-Si键,所以
 熔沸点低于
熔沸点低于
Ⅱ.是储氢材料,已知其由
 和
和 构成,释放氢气的原理为
构成,释放氢气的原理为 。
。(2)
 中不存在的作用力有
中不存在的作用力有A.离子键 B.共价键 C.分子间作用力
(3)氢化锂(LiH)是离子化合物,写出其电子式
Ⅲ.汽车安全气囊中的填充物有
 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和氮气。完成下列填空:
遇撞击时能生成金属钠和氮气。完成下列填空:(4)写出
 的电子式:
的电子式:(5)
 和
和 是两种不同的化合物,
是两种不同的化合物, 是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1:1的比例构成的化合物。 晶体中存在的化学键类型有
晶体中存在的化学键类型有 遇
遇 会水解而产生
会水解而产生 和
和 ,
, 晶体中存在的化学键类型有
晶体中存在的化学键类型有(6)汽车安全气囊填充物的三种物质中属于共价化合物的是
(7)该题中出现的极性分子有
(8)渗氮工艺已经成为钢材处理的重要手段,已知一种磁性氮化铁晶胞如下图,该物质的化学式是

您最近一年使用:0次



