1 . 腰鼓是汉族传统乐器之一,鼓身为浸过桐油的木制品,鼓面蒙牛皮或骡马皮。下列说法正确的是
| A.桐油是从桐籽中提炼出来的油脂,油脂属于天然高分子化合物 |
| B.鼓身的主要成分为纤维素,纤维素与淀粉均属于多糖,两者均能水解 |
| C.鼓面的牛皮或骡马皮主要成分为蛋白质,蛋白质具有耐酸碱腐蚀的特点 |
| D.铜质鼓环宜采用铁质或锌质铆钉固定 |
您最近一年使用:0次
名校
解题方法
2 . 元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子的最外层电子数与核外电子总数之比为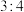 ;M元素原子的最外层电子数与电子层数之比为
;M元素原子的最外层电子数与电子层数之比为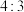 ;N-、Z+、X+的半径逐渐减小;化合物
;N-、Z+、X+的半径逐渐减小;化合物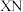 常温下为气体。据此回答:
常温下为气体。据此回答:
(1)元素 形成的常见氧化物属于
形成的常见氧化物属于_______ (“酸性”“碱性”或“不成盐”)氧化物。
(2) 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为_______ , 和
和 形成的氢化物中稳定性较强的是
形成的氢化物中稳定性较强的是_______ (填化学式)。
(3)化合物A、B均为由上述五种元素中的任意三种组成的强电解质,组成元素的原子个数之比均为 ,A的固体具有吸湿性,
,A的固体具有吸湿性, 是“84”消毒液的有效成分。
是“84”消毒液的有效成分。
①写出 的电子式:
的电子式:_______ 。
② 与氢氧化铝反应的离子方程式为
与氢氧化铝反应的离子方程式为_______ 。
③B与浓盐酸反应可制得 的单质,反应的离子方程式为
的单质,反应的离子方程式为_______ 。
(4) 的单质的用途为
的单质的用途为_______ (任写一点)。
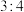 ;M元素原子的最外层电子数与电子层数之比为
;M元素原子的最外层电子数与电子层数之比为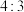 ;N-、Z+、X+的半径逐渐减小;化合物
;N-、Z+、X+的半径逐渐减小;化合物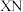 常温下为气体。据此回答:
常温下为气体。据此回答:(1)元素
 形成的常见氧化物属于
形成的常见氧化物属于(2)
 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为 和
和 形成的氢化物中稳定性较强的是
形成的氢化物中稳定性较强的是(3)化合物A、B均为由上述五种元素中的任意三种组成的强电解质,组成元素的原子个数之比均为
 ,A的固体具有吸湿性,
,A的固体具有吸湿性, 是“84”消毒液的有效成分。
是“84”消毒液的有效成分。①写出
 的电子式:
的电子式:②
 与氢氧化铝反应的离子方程式为
与氢氧化铝反应的离子方程式为③B与浓盐酸反应可制得
 的单质,反应的离子方程式为
的单质,反应的离子方程式为(4)
 的单质的用途为
的单质的用途为
您最近一年使用:0次
3 . 乙苯脱氢的反应历程如下图(Ph-为苯基),下列说法正确的是

| A.物质Ⅰ为催化剂 |
B.此反应过程中 是氧化剂 是氧化剂 |
| C.只有过程②有电子转移 |
| D.每脱去1mol氢原子,转移2mol电子 |
您最近一年使用:0次
名校
解题方法
4 . 电化学的发展是化学对人类的一项重大贡献。探究原电池和电解池原理,对生产生活具有重要的意义。
I.利用电化学方法可以将CO2有效地转化为HCOO- (其中C元素的化合价为+2价),装置如图所示。_______ 。
(2)①装置工作时,阴极除有HCOO-生成外,还可能生成副产物,降低电解效率。
已知:电解效率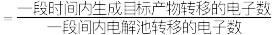
副产物可能是_______ (写出一种即可)。
②标准状况下,当阳极生成氧气的体积为224 mL时,测得整个阴极区内的c(HCOO-)=0.015 mol/L,电解效率为_______ (忽略电解前后溶液的体积变化)。
Ⅱ.利用新型镁—锂双离子二次电池(甲池)作电源同时电解乙池和丙池。_______ (填“m极”或“n极”)移动。
(4)给新型镁—锂双离子二次电池充电时,m极与电源的_______ 极相连,导线中每通过0.2 mol e-,甲池的左室中溶液的质量减少_______ g。
(5)电解一段时间后,乙池中溶液的pH将_______ (填“增大”“减小”或“不变”)。
(6)丙池发生电解反应的总方程式为_______ 。
I.利用电化学方法可以将CO2有效地转化为HCOO- (其中C元素的化合价为+2价),装置如图所示。

(2)①装置工作时,阴极除有HCOO-生成外,还可能生成副产物,降低电解效率。
已知:电解效率
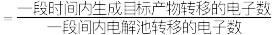
副产物可能是
②标准状况下,当阳极生成氧气的体积为224 mL时,测得整个阴极区内的c(HCOO-)=0.015 mol/L,电解效率为
Ⅱ.利用新型镁—锂双离子二次电池(甲池)作电源同时电解乙池和丙池。
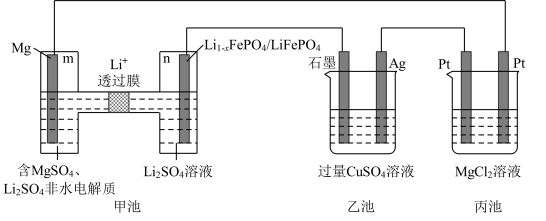
(4)给新型镁—锂双离子二次电池充电时,m极与电源的
(5)电解一段时间后,乙池中溶液的pH将
(6)丙池发生电解反应的总方程式为
您最近一年使用:0次
5 . 下列装置中能构成原电池的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 完成下列问题。
(1)某同学设计了一个甲醚 燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题:
燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题:_____ 。
②乙装置中溶液为500ml,反应一段时间后,乙装置中生成NaOH主要在_____ (填“铁极”或“石墨极”)区,X膜是_____ (填“阳离子交换膜”或“阴离子交换膜”),当消耗标况下 时,乙装置溶液中
时,乙装置溶液中
_____ (忽略溶液体积变化)。
③如果粗铜中含有锌、银等杂质,丙装置中阳极减少的质量_____ 阴极增加的质量(填“大于”“小于”或“等于”)。反应一段时间,硫酸铜溶液浓度将_____ (填“增大”“减小”或“不变”)。
(2)我国科学家采用单原子Ni和纳米Cu作串联催化剂,通过电解法将 转化为乙烯。装置示意图如下。
转化为乙烯。装置示意图如下。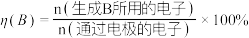
①纳米Cu催化剂上发生反应:_____ ;
②若乙烯的电解效率为60%,电路中通过1mol电子时,电解法将 转化为乙烯的物质的量是
转化为乙烯的物质的量是_____ mol。
(1)某同学设计了一个甲醚
 燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题:
燃料电池并探究氯碱工业原理和粗铜的精炼原理。根据要求回答下列相关问题: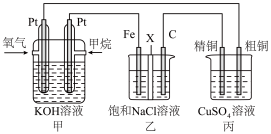
②乙装置中溶液为500ml,反应一段时间后,乙装置中生成NaOH主要在
 时,乙装置溶液中
时,乙装置溶液中
③如果粗铜中含有锌、银等杂质,丙装置中阳极减少的质量
(2)我国科学家采用单原子Ni和纳米Cu作串联催化剂,通过电解法将
 转化为乙烯。装置示意图如下。
转化为乙烯。装置示意图如下。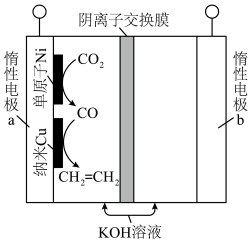
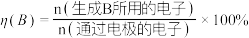
①纳米Cu催化剂上发生反应:
②若乙烯的电解效率为60%,电路中通过1mol电子时,电解法将
 转化为乙烯的物质的量是
转化为乙烯的物质的量是
您最近一年使用:0次
名校
解题方法
7 . 用一种具有“卯榫”结构的双极膜组装电解池(如图),可实现大电流催化电解 溶液制氨。
溶液制氨。_____ ,阳极反应式:_____ 。
(2)工作时,在双极膜界面处 发生解离产生
发生解离产生 和
和 ,产生的
,产生的 移向
移向_____ 极(填“a”或“b”),每生成 ,双极膜处有
,双极膜处有_____ mol的 解离。
解离。
(3)电解过程中,阳极室中KOH的物质的量_____ (填“增加”“不变”或“减少”)
(4)相比于平面结构双极膜,“卯榫”结构可增加接触面积,有利于_____ 。
 溶液制氨。
溶液制氨。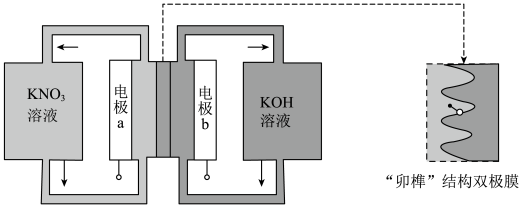
(2)工作时,在双极膜界面处
 发生解离产生
发生解离产生 和
和 ,产生的
,产生的 移向
移向 ,双极膜处有
,双极膜处有 解离。
解离。(3)电解过程中,阳极室中KOH的物质的量
(4)相比于平面结构双极膜,“卯榫”结构可增加接触面积,有利于
您最近一年使用:0次
名校
8 . 工业上可以用 来生产甲醇燃料。在体积为2L的密闭容器中,充入
来生产甲醇燃料。在体积为2L的密闭容器中,充入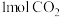 和3 mol H2,一定条件下发生反应
和3 mol H2,一定条件下发生反应 。测得
。测得 和
和 的物质的量随时间变化如图所示。下列描述正确的是
的物质的量随时间变化如图所示。下列描述正确的是
 来生产甲醇燃料。在体积为2L的密闭容器中,充入
来生产甲醇燃料。在体积为2L的密闭容器中,充入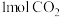 和3 mol H2,一定条件下发生反应
和3 mol H2,一定条件下发生反应 。测得
。测得 和
和 的物质的量随时间变化如图所示。下列描述正确的是
的物质的量随时间变化如图所示。下列描述正确的是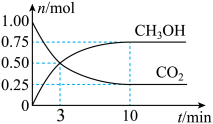
A.达到平衡时, 的转化率为75% 的转化率为75% |
| B.3 min时,达到了化学平衡状态 |
| C.反应进行到10 min时,气体的总压强是开始的0.625倍 |
D.反应开始到10 min时,用 表示的反应速率为0.0375 表示的反应速率为0.0375  |
您最近一年使用:0次
名校
9 . 短周期元素X、Y、Z、M原子序数依次增大,Z的最高价氧化物对应的水化物与其简单氢化物可形成一种盐,M的最高正价与最低负价绝对值之差为4,它们组成的一种分子结构如图。下列说法错误的是
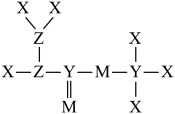
| A.Y与X形成的化合物种类繁多 |
| B.X、Z、M三种元素形成的化合物可能是离子化合物 |
| C.Y、M的最高价氧化物对应水化物的酸性,M的最高价氧化物对应水化物酸性强 |
| D.Z的氧化物对应的水化物都是强酸 |
您最近一年使用:0次
名校
10 . 利用间接转化法可将氮氧化物转化为化工产品以实现氮氧化物的充分利用。
已知:
①
②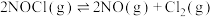
③
若某温度下,向 恒容密闭容器中加入
恒容密闭容器中加入 和
和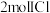 发生上述反应,达到平衡时容器中
发生上述反应,达到平衡时容器中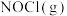 为
为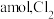 为
为 。下列说法错误的是
。下列说法错误的是
已知:
①

②
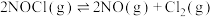
③

若某温度下,向
 恒容密闭容器中加入
恒容密闭容器中加入 和
和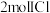 发生上述反应,达到平衡时容器中
发生上述反应,达到平衡时容器中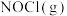 为
为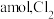 为
为 。下列说法错误的是
。下列说法错误的是A.平衡时 的浓度为 的浓度为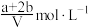 |
| B.若该密闭容器中气体颜色保持不变,说明各反应已达到平衡状态 |
C. 的转化率为 的转化率为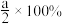 |
| D.若反应①②为吸热反应,③为放热反应,则升高温度反应①②速率增大,③速率减小 |
您最近一年使用:0次
7日内更新
|
52次组卷
|
5卷引用:山东省部分学校2023-2024学年高一下学期五月月考化学试题







