名校
1 . 甲烷和甲醇 既是重要的化工原料,又是未来重要的能源物质。
既是重要的化工原料,又是未来重要的能源物质。
(1)将 和
和 通入容积为
通入容积为 的恒容密闭容器中,恒温条件下发生反应:
的恒容密闭容器中,恒温条件下发生反应: 。
。
①下列描述中能说明该反应已达到平衡状态的是_______ (填标号)。
A.断裂 键时,生成
键时,生成 键
键
B.容器内混合气体的平均摩尔质量保持不变
C.容器内混合气体的压强保持不变
D.容器内CO与H2的体积之比保持不变
②测得在 时该反应达到平衡,此时CH4的物质的量为
时该反应达到平衡,此时CH4的物质的量为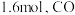 的物质的量浓度为
的物质的量浓度为 。则
。则 内,用CO表示的该反应平均反应速率
内,用CO表示的该反应平均反应速率
_______ mol•L-1•min-1,V=_______  。
。
(2)在容积为 的恒容密闭容器中通入等物质的量的
的恒容密闭容器中通入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。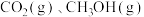 的物质的量随时间的变化关系如图所示。
的物质的量随时间的变化关系如图所示。_______ (填“a”“b”“c”或“d”);用同一物质表示反应速率时,a,c两点的正反应速率:Va_______ (填“ ”“
”“ ”或“
”或“ ”,下同)
”,下同)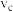 ,该反应达到平衡时,CO2的转化率
,该反应达到平衡时,CO2的转化率_______ 50%。
 既是重要的化工原料,又是未来重要的能源物质。
既是重要的化工原料,又是未来重要的能源物质。(1)将
 和
和 通入容积为
通入容积为 的恒容密闭容器中,恒温条件下发生反应:
的恒容密闭容器中,恒温条件下发生反应: 。
。①下列描述中能说明该反应已达到平衡状态的是
A.断裂
 键时,生成
键时,生成 键
键B.容器内混合气体的平均摩尔质量保持不变
C.容器内混合气体的压强保持不变
D.容器内CO与H2的体积之比保持不变
②测得在
 时该反应达到平衡,此时CH4的物质的量为
时该反应达到平衡,此时CH4的物质的量为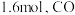 的物质的量浓度为
的物质的量浓度为 。则
。则 内,用CO表示的该反应平均反应速率
内,用CO表示的该反应平均反应速率
 。
。(2)在容积为
 的恒容密闭容器中通入等物质的量的
的恒容密闭容器中通入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 的物质的量随时间的变化关系如图所示。
的物质的量随时间的变化关系如图所示。
 ”“
”“ ”或“
”或“ ”,下同)
”,下同)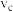 ,该反应达到平衡时,CO2的转化率
,该反应达到平衡时,CO2的转化率
您最近一年使用:0次
2024-06-16更新
|
38次组卷
|
3卷引用:山东省部分学校2023-2024学年高一下学期五月月考化学试题
名校
解题方法
2 . 科学家发明了一种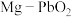 电池,电解质溶液中的溶质为
电池,电解质溶液中的溶质为 、
、 、NaOH,通过M和N两种离子交换膜将电解质溶液隔开,形成A、B、C三个电解质溶液区域(已知:
、NaOH,通过M和N两种离子交换膜将电解质溶液隔开,形成A、B、C三个电解质溶液区域(已知: ;电池工作时,A、B、C区域溶液的溶质成分不变),电池工作的过程中,A区出现沉淀,装置如图,下列说法不正确的是
;电池工作时,A、B、C区域溶液的溶质成分不变),电池工作的过程中,A区出现沉淀,装置如图,下列说法不正确的是
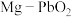 电池,电解质溶液中的溶质为
电池,电解质溶液中的溶质为 、
、 、NaOH,通过M和N两种离子交换膜将电解质溶液隔开,形成A、B、C三个电解质溶液区域(已知:
、NaOH,通过M和N两种离子交换膜将电解质溶液隔开,形成A、B、C三个电解质溶液区域(已知: ;电池工作时,A、B、C区域溶液的溶质成分不变),电池工作的过程中,A区出现沉淀,装置如图,下列说法不正确的是
;电池工作时,A、B、C区域溶液的溶质成分不变),电池工作的过程中,A区出现沉淀,装置如图,下列说法不正确的是
A. 通过M膜移向B区,离子交换膜N为阴离子交换膜 通过M膜移向B区,离子交换膜N为阴离子交换膜 |
| B.B区域的电解质浓度逐渐减小 |
C.放电时,Mg电极反应为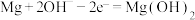 |
| D.消耗2.4gMg时,C区域电解质溶液减少16.0g |
您最近一年使用:0次
名校
3 . 某实验小组用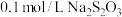 溶液和
溶液和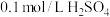 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
已知:实验结果: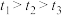 。回答下列问题:
。回答下列问题:
(1)a=___________ ml。
(2)写出Na2S2O3溶液和H2SO4溶液反应的离子方程式:___________ 。
(3)对比实验I、III可知,___________ 能加快反应速率。
(4)进行实验I、II时,依次向试管中加入Na2S2O3溶液、___________ 、___________ ,两者的顺序不可颠倒,理由是:___________ 。
(5)经查阅资料,构成原电池也能加快反应速率。某小组用一定的锌与足量的0.1 mol/L H2SO4溶液反应,下列物质即能加快反应速率,又不影响生成气体量的是:___________
a.适当升温 b.滴加几滴0.15 mol/LHCl c.滴加几滴 溶液
溶液
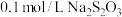 溶液和
溶液和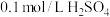 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。| 实验序号 | 温度/℃ | Na2S2O3溶液体积/mL | H2SO4溶液体积/mL | H2O体积/mL | 出现沉淀所需的时间/s |
| I | 20 | 5.0 | 5.0 | 10.0 | t1 |
| II | 20 | 5.0 | 10.0 | a | t2 |
| III | 60 | 5.0 | 5.0 | 10.0 | t3 |
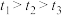 。回答下列问题:
。回答下列问题:(1)a=
(2)写出Na2S2O3溶液和H2SO4溶液反应的离子方程式:
(3)对比实验I、III可知,
(4)进行实验I、II时,依次向试管中加入Na2S2O3溶液、
(5)经查阅资料,构成原电池也能加快反应速率。某小组用一定的锌与足量的0.1 mol/L H2SO4溶液反应,下列物质即能加快反应速率,又不影响生成气体量的是:
a.适当升温 b.滴加几滴0.15 mol/LHCl c.滴加几滴
 溶液
溶液
您最近一年使用:0次
名校
4 . 向含有0.01 mol Cu,amol Cu2O、bmol CuO的混合物中滴加6 mol/L的稀硝酸溶液至10 mL时,固体恰好完全溶解,得到标准状况下224 mL气体(纯净物)。下列说法不正确的是
| A.反应过程中转移0.03 mol电子 | B.a∶b=1∶1 |
| C.等量上述稀硝酸中最多能溶解0.84 g Fe | D.被还原的硝酸为0.01 mol |
您最近一年使用:0次
5 . 下列说法正确的是
A.向NaHSO3溶液中滴加氢硫酸,产生淡黄色沉淀,证明 具有氧化性 具有氧化性 |
| B.加热浓硫酸与NaCl固体的混合物可制备HCl,说明浓硫酸酸性强于HCl |
| C.将CO2通入Ba(NO3)2,溶液无明显现象,则将SO2通入Ba(NO3)2溶液也无明显现象 |
| D.向浓HNO3中插入红热的炭,产生红棕色气体,证明炭可与浓HNO3反应生成NO2 |
您最近一年使用:0次
6 . 某小组在实验室模拟侯氏制碱过程,如下图,选择所给仪器或操作方法错误的是
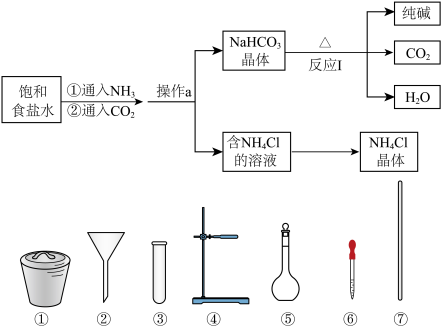
A.饱和食盐水中应先通入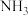 |
| B.操作a用到的仪器有②④⑦ |
| C.反应Ⅰ发生的容器是① |
D.由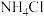 溶液得到晶体的操作为蒸发结晶 溶液得到晶体的操作为蒸发结晶 |
您最近一年使用:0次
解题方法
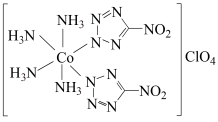
7 . 高性能炸药BNCP的结构如下所示,回答下列问题: 的基态价层电子排布图是
的基态价层电子排布图是_______ , 的配位数是
的配位数是_______ ,阴离子 的中心原子杂化类型是
的中心原子杂化类型是_______ 。
(2)
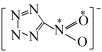 配体中的
配体中的 键的数目是
键的数目是_______ ,已知该配体是平面结构,图中标记的 原子与
原子与 原子之间的
原子之间的 键是由
键是由 原子的
原子的_______ 杂化轨道与O原子的_______ 轨道重叠形成的。
(3)比较 、
、 、
、 的键角大小:
的键角大小:_______ 。
(4)比较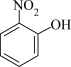 、
、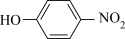 的沸点并说明理由:
的沸点并说明理由:_______ 。
(5)比较 与
与 的极性大小并说明理由:
的极性大小并说明理由:_______ 。
(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐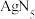 的晶体结构中:
的晶体结构中: 采取面心立方最密堆积,
采取面心立方最密堆积, 填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的
填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的 的数目是
的数目是_______ , 与
与 最近的距离是
最近的距离是_______ (用 表示)。
表示)。
 的基态价层电子排布图是
的基态价层电子排布图是 的配位数是
的配位数是 的中心原子杂化类型是
的中心原子杂化类型是(2)

 配体中的
配体中的 键的数目是
键的数目是 原子与
原子与 原子之间的
原子之间的 键是由
键是由 原子的
原子的(3)比较
 、
、 、
、 的键角大小:
的键角大小:(4)比较
 、
、 的沸点并说明理由:
的沸点并说明理由:(5)比较
 与
与 的极性大小并说明理由:
的极性大小并说明理由:(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐
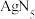 的晶体结构中:
的晶体结构中: 采取面心立方最密堆积,
采取面心立方最密堆积, 填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的
填在正四面体空隙中,从晶胞上方俯视的投影图如图所示。每个晶胞中含有的 的数目是
的数目是 与
与 最近的距离是
最近的距离是 表示)。
表示)。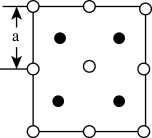
您最近一年使用:0次
名校
8 . 近年来,我国航天科技事业取得了辉煌的成就。下列说法错误的是
| A.“天舟六号”为中国空间站送去推进剂Xe气,Xe是54号元素,位于p区 |
| B.某型长征运载火箭以液氧和煤油为推进剂,液氧分子间靠范德华力凝聚在一起 |
C.我国科学家由嫦娥五号带回的月壤样品中,首次发现了天然玻璃纤维,该纤维中的主要氧化物 属于分子晶体 属于分子晶体 |
| D.“神州十五号”航天员使用塑料航天面窗,塑料属于高分子材料 |
您最近一年使用:0次
9 . 回答下列问题:
(1)铅蓄电池的电池总反应式为:Pb+PbO2+4H++2SO
 2PbSO4+2H2O,当外电路通过1 mol电子时,理论上负极板的质量增加
2PbSO4+2H2O,当外电路通过1 mol电子时,理论上负极板的质量增加____ g。
(2)银锌电池电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。
(3)汽车发动机工作时会引发N2和O2反应,生成NOX等污染大气,其中生成NO的能量变化如图所示,若反应生成2molNO气体(填“吸收”或“放出”)________ 热量。___________ 口通入(填“A"或“B"),当外电路通过0.4mol的电子时,消耗O2的体积___________ L(标况下)。
(1)铅蓄电池的电池总反应式为:Pb+PbO2+4H++2SO

 2PbSO4+2H2O,当外电路通过1 mol电子时,理论上负极板的质量增加
2PbSO4+2H2O,当外电路通过1 mol电子时,理论上负极板的质量增加(2)银锌电池电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。
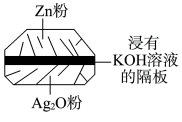
| A.在使用过程中,电解质KOH被不断消耗 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
(3)汽车发动机工作时会引发N2和O2反应,生成NOX等污染大气,其中生成NO的能量变化如图所示,若反应生成2molNO气体(填“吸收”或“放出”)


您最近一年使用:0次
解题方法
10 . 常温下 与
与 的反应为
的反应为 ,当加入
,当加入 时生成更难溶的Ca5(PO4)3F,氟磷比
时生成更难溶的Ca5(PO4)3F,氟磷比 为1∶10、10∶1的两种水溶液中加入过量
为1∶10、10∶1的两种水溶液中加入过量 ,平衡时
,平衡时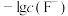 、
、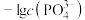 与
与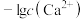 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是
 与
与 的反应为
的反应为 ,当加入
,当加入 时生成更难溶的Ca5(PO4)3F,氟磷比
时生成更难溶的Ca5(PO4)3F,氟磷比 为1∶10、10∶1的两种水溶液中加入过量
为1∶10、10∶1的两种水溶液中加入过量 ,平衡时
,平衡时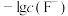 、
、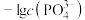 与
与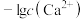 的关系如图。下列说法错误的是
的关系如图。下列说法错误的是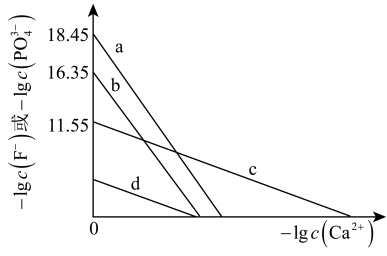
A.曲线a、b均表示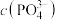 与 与 的关系,氟磷比a>b 的关系,氟磷比a>b |
B. |
C.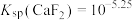 |
D.将氟磷比由10∶1提高至20∶1可有效降低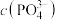 |
您最近一年使用:0次



