1 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如图所示(夹持和加热仪器已省略)。

有关物质性质如表:
实验过程:
I.合成:装置C中盛有0.1molFeCO3和250mL1.0mol·L-1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置c中空气排净后,加热并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
II.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是____ ;装置C中,仪器b与a相比的优点是____ 。
(2)装置B中盛有的试剂是____ ;合成过程加入柠檬酸的作用是促进FeCO3溶解和____ 。
(3)实验过程中装置D的导管一直伸入液面下的必要性是____ 。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用化学方程式表示为____ 。
(5)过程II中加入无水乙醇的目的是_____ 。
(6)检验产品中是否含有Fe3+的试剂是____ 溶液(写化学式)。
(7)本实验制得13.77g甘氨酸亚铁(M=204g/mol),则其产率是____ 。

有关物质性质如表:
| 物质名称 | 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 性质 | 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
| 两性化合物 | 强酸性、强还原性 | 还原性 |
I.合成:装置C中盛有0.1molFeCO3和250mL1.0mol·L-1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置c中空气排净后,加热并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
II.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是
(2)装置B中盛有的试剂是
(3)实验过程中装置D的导管一直伸入液面下的必要性是
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用化学方程式表示为
(5)过程II中加入无水乙醇的目的是
(6)检验产品中是否含有Fe3+的试剂是
(7)本实验制得13.77g甘氨酸亚铁(M=204g/mol),则其产率是
您最近一年使用:0次
2022-07-13更新
|
306次组卷
|
2卷引用:福建省厦门外国语学校石狮分校、泉港区第一中学2021-2022学年高二下学期期末联考化学试题
2 . 氯吡脲(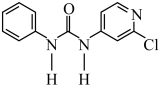 )属苯脲类细胞分裂素,可用作植物生长调节剂,广泛用于农业上促进果实肥大,提高产量,保鲜等。可用2,4-二氯吡啶与苯基脲反应合成氯吡脲:
)属苯脲类细胞分裂素,可用作植物生长调节剂,广泛用于农业上促进果实肥大,提高产量,保鲜等。可用2,4-二氯吡啶与苯基脲反应合成氯吡脲:
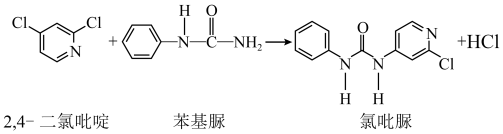
(1)苯基脲分子中除H外,电负性最大的元素为____ (填元素符号)。
(2)氯吡脲分子中,碳原子与氯原子形成的化学键为____ σ键(填序号)。
A.s-p B.p-p C.sp-p D.sp2-p E.sp2-s F.sp3-P
氮原子的杂化轨道类型有____ 。
(3)氯吡脲能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①H2O分子中的H-O-H键角为105°,则NH3分子中的H-N-H键角____ (填“>”、“<”或“=”)105°。
②氨气溶于水时,大部分NH3与H2O用氢键(用“●●●”表示)结合形成NH3•H2O分子。根据氨水的性质可推知NH3•H2O的结构式为____ (填标号)。
A.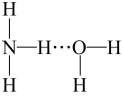 B.
B.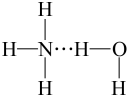 C.
C.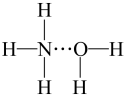 D.
D.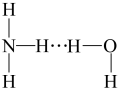
(4)苯基脲的生产方法:将尿素、盐酸及苯胺加入反应釜,加热搅拌,在100-104℃回流1h,充分反应后,加水搅拌,冷却,甩滤,用水洗涤滤饼,干燥即得成品。
①写出苯基脲分子中含有的官能团的名称:____ 。
②请写出苯基脲在稀盐酸中水解的化学方程式:____ 。
③写出符合下列条件的苯基脲的同分异构体M的结构简式____ (写一种即可)。
a.能发生银镜反应
b.分子中有4种不同化学环境的氢,核磁共振氢谱图有4组峰,峰面积之比为4:2:1:1
④已知: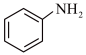 +ROH
+ROH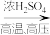
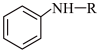 ,则
,则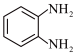 与乙二醇在该条件下发生反应生成的有机物的结构简式为
与乙二醇在该条件下发生反应生成的有机物的结构简式为____ 。
 )属苯脲类细胞分裂素,可用作植物生长调节剂,广泛用于农业上促进果实肥大,提高产量,保鲜等。可用2,4-二氯吡啶与苯基脲反应合成氯吡脲:
)属苯脲类细胞分裂素,可用作植物生长调节剂,广泛用于农业上促进果实肥大,提高产量,保鲜等。可用2,4-二氯吡啶与苯基脲反应合成氯吡脲:
(1)苯基脲分子中除H外,电负性最大的元素为
(2)氯吡脲分子中,碳原子与氯原子形成的化学键为
A.s-p B.p-p C.sp-p D.sp2-p E.sp2-s F.sp3-P
氮原子的杂化轨道类型有
(3)氯吡脲能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①H2O分子中的H-O-H键角为105°,则NH3分子中的H-N-H键角
②氨气溶于水时,大部分NH3与H2O用氢键(用“●●●”表示)结合形成NH3•H2O分子。根据氨水的性质可推知NH3•H2O的结构式为
A.
 B.
B. C.
C. D.
D.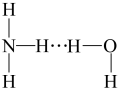
(4)苯基脲的生产方法:将尿素、盐酸及苯胺加入反应釜,加热搅拌,在100-104℃回流1h,充分反应后,加水搅拌,冷却,甩滤,用水洗涤滤饼,干燥即得成品。
①写出苯基脲分子中含有的官能团的名称:
②请写出苯基脲在稀盐酸中水解的化学方程式:
③写出符合下列条件的苯基脲的同分异构体M的结构简式
a.能发生银镜反应
b.分子中有4种不同化学环境的氢,核磁共振氢谱图有4组峰,峰面积之比为4:2:1:1
④已知:
 +ROH
+ROH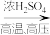
 ,则
,则 与乙二醇在该条件下发生反应生成的有机物的结构简式为
与乙二醇在该条件下发生反应生成的有机物的结构简式为
您最近一年使用:0次
3 . Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下列说法正确的是
| A.非金属性:X>Q | B.单质的熔点:X>Y |
| C.最高价含氧酸的酸性:Z<Y | D.简单氢化物的沸点:Z<Q |
您最近一年使用:0次
名校
解题方法
4 . 中成药连花清瘟胶囊对于治疗轻型和普通型的新冠肺炎患者有确切的疗效。其有效成分绿原酸的结构简式如下图所示,下列有关绿原酸的说法不正确的是

| A.分子式为C16H18O9 |
| B.该分子中有4个手性碳原子 |
| C.绿原酸分子存在顺反异构体 |
| D.1mol绿原酸可消耗6molNa、5molNaOH、4molBr2 |
您最近一年使用:0次
2022-07-12更新
|
659次组卷
|
2卷引用:福建省漳州市四校2021-2022学年高二下学期期末联考化学试题
解题方法
5 . 生活中处处可见有机化学知识,下列说法正确的是
| A.大米酿酒是淀粉分解成乙醇 | B.茶叶中的茶多酚属于芳香族化合物 |
| C.糖类与油脂都能水解 | D.尼龙-66由6个己二酸和6个己二胺组成 |
您最近一年使用:0次
解题方法
6 . 我国提出2030年实现“碳达峰”,2060年实现“碳中和”, 的再利用成为热门话题。回答下列问题:
的再利用成为热门话题。回答下列问题:
Ⅰ.光热化学循环分解 为CO和
为CO和 的反应为温室气体减排提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示。
的反应为温室气体减排提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示。
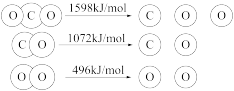
(1)已知: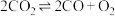 ,根据数据计算,分解
,根据数据计算,分解 需吸收
需吸收_______ kJ的能量。
Ⅱ.工业上可用 来生产燃料甲醇
来生产燃料甲醇 ,实验室模拟该过程,在体积为2L的密闭容器中,充入
,实验室模拟该过程,在体积为2L的密闭容器中,充入 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
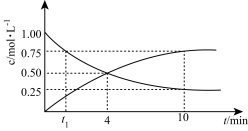
(2) 时刻,正、逆反应速率大小:v(正)
时刻,正、逆反应速率大小:v(正)_______ v(逆)(填“>”“=”或“<”),在0min到4min时间段,
_______  。
。
(3)下列措施能增大反应速率的是_______ (填字母)。
a.升高温度 b.扩大容器体积
c.充入一定量氦气 d.加入催化剂
(4)能说明上述反应达到平衡状态的是_______ (填字母)。
a.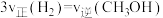
b. 的物质的量不再变化
的物质的量不再变化
c.容器内气体的总质量保持不变
d.单位时间内,每生成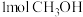 ,同时生成
,同时生成
e.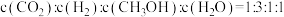
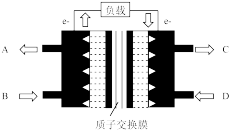
(5) 可以作燃料电池,工作原理如图。电池放电时,应从
可以作燃料电池,工作原理如图。电池放电时,应从_______ (填“B”或“D”)通入 ,该电极发生
,该电极发生_______ 反应(填“氧化”或“还原”),理论上每消耗 转移
转移_______ mol电子。
 的再利用成为热门话题。回答下列问题:
的再利用成为热门话题。回答下列问题:Ⅰ.光热化学循环分解
 为CO和
为CO和 的反应为温室气体减排提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示。
的反应为温室气体减排提供了一个新途径,该反应各分子化学键完全断裂时的能量变化如图所示。
(1)已知:
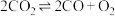 ,根据数据计算,分解
,根据数据计算,分解 需吸收
需吸收Ⅱ.工业上可用
 来生产燃料甲醇
来生产燃料甲醇 ,实验室模拟该过程,在体积为2L的密闭容器中,充入
,实验室模拟该过程,在体积为2L的密闭容器中,充入 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
(2)
 时刻,正、逆反应速率大小:v(正)
时刻,正、逆反应速率大小:v(正)
 。
。(3)下列措施能增大反应速率的是
a.升高温度 b.扩大容器体积
c.充入一定量氦气 d.加入催化剂
(4)能说明上述反应达到平衡状态的是
a.
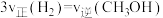
b.
 的物质的量不再变化
的物质的量不再变化c.容器内气体的总质量保持不变
d.单位时间内,每生成
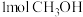 ,同时生成
,同时生成
e.
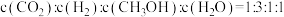
(5)
 可以作燃料电池,工作原理如图。电池放电时,应从
可以作燃料电池,工作原理如图。电池放电时,应从 ,该电极发生
,该电极发生 转移
转移
您最近一年使用:0次
7 . 催化剂(Fe,Al)/MIL-53可直接选择性氧化甲烷制甲醇,节省能耗。

(1)(Fe,Al)/MIL-53制备方法如下:Al(NO3)3•9H2O +Al/MIL-53
+Al/MIL-53 (Fe,Al)/MIL-53。
(Fe,Al)/MIL-53。
①对苯二甲酸的结构简式为_______ ,该分子中最多_______ 个原子共平面。
②生成(Fe,Al)/MIL-53过程中溶液pH_______ (填“变大”或“变小”)。
③(Fe,Al)/MIL-53中Fe3+位于O原子形成的_______ 空隙中,1个对苯二甲酸根离子最多能形成_______ 个配位键。
(2)(Fe,Al)/MIL-53催化CH4制CH3OH的机理如图,其中虚线表示吸附状态。

①ii转化为iii的过程中,破坏的微粒间作用力有_______ (填标号)。
A.σ键 B.配位键 C.离子键 D.极性键 E.非极性键
②该催化循环中铁元素价态有_______ 种。
(3)用FeCl3•6H2O和对苯二甲酸合成Fe/MIL-53。两种催化剂在上述催化过程中相对能量的变化情况如图。

①Fe/MIL-53催化过程中决速步骤为_______ (化学键变化角度答题)。
②(Fe,Al)/MIL-53催化效果更佳的原因是_______ 。

(1)(Fe,Al)/MIL-53制备方法如下:Al(NO3)3•9H2O
 +Al/MIL-53
+Al/MIL-53 (Fe,Al)/MIL-53。
(Fe,Al)/MIL-53。①对苯二甲酸的结构简式为
②生成(Fe,Al)/MIL-53过程中溶液pH
③(Fe,Al)/MIL-53中Fe3+位于O原子形成的
(2)(Fe,Al)/MIL-53催化CH4制CH3OH的机理如图,其中虚线表示吸附状态。

①ii转化为iii的过程中,破坏的微粒间作用力有
A.σ键 B.配位键 C.离子键 D.极性键 E.非极性键
②该催化循环中铁元素价态有
(3)用FeCl3•6H2O和对苯二甲酸合成Fe/MIL-53。两种催化剂在上述催化过程中相对能量的变化情况如图。

①Fe/MIL-53催化过程中决速步骤为
②(Fe,Al)/MIL-53催化效果更佳的原因是
您最近一年使用:0次
8 . [Co(en)2Cl2]Cl配合物存在顺反异构现象。制备trans-[Co(en)2Cl2]Cl的实验过程如下。

乙二胺缩写为en,实验过程含钴离子依次发生如下变化:[Co(H2O)6]2+→[Co(en)2(H2O)2]2+→[Co(en)2(H2O)2]3+→[Co(en)2C12]+
(1)“溶解”过程Co(II)的配位数_______ 变化(填“发生”或“未发生”)。
(2)“氧化”过程Co(II)转化为Co(III)的离子方程式为_______ 。
(3)“氯化”过程使用浓盐酸而不用NaCl。浓盐酸的作用有_______ 。
(4)“蒸发浓缩”至_______ 停止加热。
(5)trans-[Co(en)2Cl2]Cl转化为cis-[Co(en)2Cl2]Cl的实验如下。

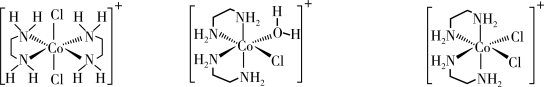
①由上述实验可知;生成trans-[Co(en)2Cl2]Cl是_______ 决速(填“热力学”或“动力学”,下同),生成cis-[Co(en)2Cl2]Cl是_______ 决速。
②设计实验将cis-[Co(en)2Cl2]Cl转化为trans-[Co(en)2Cl2]Cl_______ 。

乙二胺缩写为en,实验过程含钴离子依次发生如下变化:[Co(H2O)6]2+→[Co(en)2(H2O)2]2+→[Co(en)2(H2O)2]3+→[Co(en)2C12]+
(1)“溶解”过程Co(II)的配位数
(2)“氧化”过程Co(II)转化为Co(III)的离子方程式为
(3)“氯化”过程使用浓盐酸而不用NaCl。浓盐酸的作用有
(4)“蒸发浓缩”至
(5)trans-[Co(en)2Cl2]Cl转化为cis-[Co(en)2Cl2]Cl的实验如下。


①由上述实验可知;生成trans-[Co(en)2Cl2]Cl是
②设计实验将cis-[Co(en)2Cl2]Cl转化为trans-[Co(en)2Cl2]Cl
您最近一年使用:0次
9 . 一种固态聚合物金属锂电池中电解质(LiEFA)与聚合物基体(PEO)之间相互作用示意如图。

下列说法错误的是

下列说法错误的是
| A.PEO能传输Li+的原因是Li+与PEO的氧原子可形成微弱的配位键 |
| B.PEO能降低EFA-迁移速率的原因是两者微粒间存在氢键作用 |
C.磺酰亚胺结构(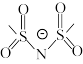 )中负电荷高度分散的原因是存在大π键 )中负电荷高度分散的原因是存在大π键 |
| D.将LiEFA中-CF3替换为-CH3,LiEFA解离出Li+所需要的能量升高 |
您最近一年使用:0次
解题方法
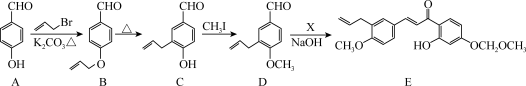
10 . 下图是化合物E的合成路线:
已知: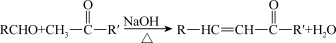
回答下列问题:
(1)A→B的反应类型为_______ ,B中含氧官能团的名称为_______ 。
(2)C→D的反应方程式为:_______ 。
(3)写出 的结构简式:
的结构简式:_______ 。
(4)检验B中含有碳碳双键的实验方法是_______ 。
(5)写出满足下列条件的B的同分异构体的结构简式_______ (任写2种)。
i.除苯环外无其他环
ii.苯环上含2种化学环境的氢原子
iii.能与 溶液发生反应产生气泡
溶液发生反应产生气泡

已知:

回答下列问题:
(1)A→B的反应类型为
(2)C→D的反应方程式为:
(3)写出
 的结构简式:
的结构简式:(4)检验B中含有碳碳双键的实验方法是
(5)写出满足下列条件的B的同分异构体的结构简式
i.除苯环外无其他环
ii.苯环上含2种化学环境的氢原子
iii.能与
 溶液发生反应产生气泡
溶液发生反应产生气泡
您最近一年使用:0次



