名校
1 . 普鲁士蓝可用于氨氮废水的处理,利用柠檬酸铁铵和赤血盐可制备得到普鲁士蓝。
Ⅰ.柠檬酸铁铵的制备
实验步骤:向已加有铁粉的三颈烧瓶中滴加柠檬酸溶液并搅拌,控温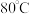 至生成柠檬酸亚铁白色沉淀。降温至
至生成柠檬酸亚铁白色沉淀。降温至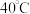 ,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温
,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温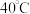 ,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。
,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。 的名称是
的名称是______ 。
(2)控温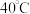 的原因
的原因______ 。
(3)“一系列操作”包括蒸发浓缩、冷却结晶、过滤、______ 、干燥。
Ⅱ.赤血盐的制备
用 在
在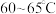 氧化黄血盐
氧化黄血盐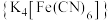 制备赤血盐
制备赤血盐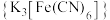 的装置如下图所示(夹持装置略)。
的装置如下图所示(夹持装置略)。______ ,装置B中试剂是______ 。
(5)反应结束后通入 一段时间的目的
一段时间的目的______ 。
(6)黄血盐会被酸性高锰酸钾彻底氧化为 和
和 ,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因
,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因______ 。
Ⅲ.普鲁士蓝的制备及应用
在紫外光作用下柠檬酸铁铵中的三价铁离子被还原为二价铁离子,再与赤血盐反应,进行电子转移后生成相对稳定的普鲁士蓝。酸化后的普鲁士蓝加双氧水可处理氨氮废水(主要含 ),原理如下:
),原理如下:
ⅰ.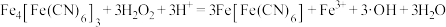
ⅱ. 将氨氮氧化为
将氨氮氧化为
(7)用实验制得的普鲁士蓝处理某氨氮废水,收集到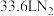 (已折成标准状况)。实验中消耗的
(已折成标准状况)。实验中消耗的 的质量至少为
的质量至少为______ g。
Ⅰ.柠檬酸铁铵的制备
实验步骤:向已加有铁粉的三颈烧瓶中滴加柠檬酸溶液并搅拌,控温
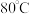 至生成柠檬酸亚铁白色沉淀。降温至
至生成柠檬酸亚铁白色沉淀。降温至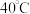 ,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温
,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵。继续控温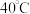 ,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。
,缓慢滴加一量的双氧水充分反应,经一系列操作,得到产品。已知:柠檬酸铁铵易溶于水,不溶于乙醇。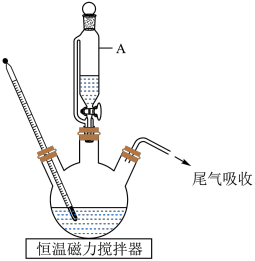
 的名称是
的名称是(2)控温
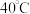 的原因
的原因(3)“一系列操作”包括蒸发浓缩、冷却结晶、过滤、
Ⅱ.赤血盐的制备
用
 在
在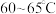 氧化黄血盐
氧化黄血盐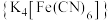 制备赤血盐
制备赤血盐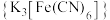 的装置如下图所示(夹持装置略)。
的装置如下图所示(夹持装置略)。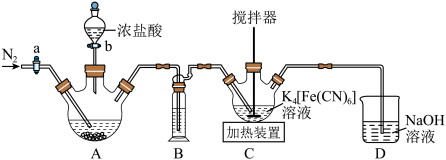
(5)反应结束后通入
 一段时间的目的
一段时间的目的(6)黄血盐会被酸性高锰酸钾彻底氧化为
 和
和 ,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因
,用离子方程式说明不用酸性高锰酸钾制备赤血盐的原因Ⅲ.普鲁士蓝的制备及应用
在紫外光作用下柠檬酸铁铵中的三价铁离子被还原为二价铁离子,再与赤血盐反应,进行电子转移后生成相对稳定的普鲁士蓝。酸化后的普鲁士蓝加双氧水可处理氨氮废水(主要含
 ),原理如下:
),原理如下:ⅰ.
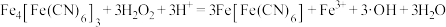
ⅱ.
 将氨氮氧化为
将氨氮氧化为
(7)用实验制得的普鲁士蓝处理某氨氮废水,收集到
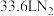 (已折成标准状况)。实验中消耗的
(已折成标准状况)。实验中消耗的 的质量至少为
的质量至少为
您最近一年使用:0次
2024-05-16更新
|
212次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
2 . 已知反应: 为阿伏加德罗常数的值,若消耗
为阿伏加德罗常数的值,若消耗 (标准状况)
(标准状况) ,下列叙述错误的是
,下列叙述错误的是
 为阿伏加德罗常数的值,若消耗
为阿伏加德罗常数的值,若消耗 (标准状况)
(标准状况) ,下列叙述错误的是
,下列叙述错误的是A.转移的电子数为 | B.生成的 价层电子对数为 价层电子对数为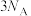 |
C.参加反应的单质硫质量为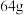 | D.参加反应的 分子数为 分子数为 |
您最近一年使用:0次
2024-05-16更新
|
178次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
解题方法
3 . 以 为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废
为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废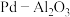 催化剂(主要含有Pd、
催化剂(主要含有Pd、 ,还有少量PdO、
,还有少量PdO、 、C)为原料制备氯化钯的流程如下:
、C)为原料制备氯化钯的流程如下:
(1)“氯化浸出”前必须“焙烧”去除废催化剂表面积碳,原因是_______ ,焙烧时间过长,“氯化浸出”率下降,可能的原因是_______ 。
(2) 中Cl原子的杂化类型是
中Cl原子的杂化类型是_______ ,“氯化浸出”时,若盐酸浓度过高,可能发生的副反应离子方程式为_______ 。
(3)滤渣1主要成分为_______ ,已知 ,若要使溶液中
,若要使溶液中 不高于
不高于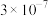 ,则应加入氨水使pH不低于
,则应加入氨水使pH不低于_______ 。
(4)工业上也可用 还原
还原 制取海绵Pd,该历程对环境友好。该反应的化学方程式为
制取海绵Pd,该历程对环境友好。该反应的化学方程式为_______ 。
(5)工业上测定Pd含量的原理为:试样用硝酸及盐酸溶解后,加过量EDTA络合钯,用锌标准溶液滴定过剩的EDTA.具体步聚如下:
I.标定锌标准溶液对钯的滴定度:
a.吸取25mLEDTA溶液置于烧杯中,滴加4~5滴盐酸,加适量水,用锌标准溶液滴定至终点,消耗锌标准溶液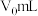 。
。
b.吸取15mL含0.0010gPd的Pd标准溶液于烧杯中,加入25mLEDTA溶液,加适量水用锌标准溶液滴定至试液由黄色变成紫红色为终点,消耗锌标准溶液 。
。
Ⅱ.滴定式样:
称取0.1000g试样置于烧杯中,加适量硝酸及盐酸充分溶解并作妥善处理,加入25mLEDT溶液,用锌标准溶液滴定至终点,消耗锌标准溶液VmL。则试样中Pd的质量分数为_______ %(用含V、 、
、 的式子表示)。
的式子表示)。
 为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废
为载体的钯催化剂常用于石化行业加氢催化裂化过程中,工业上以失活后的废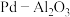 催化剂(主要含有Pd、
催化剂(主要含有Pd、 ,还有少量PdO、
,还有少量PdO、 、C)为原料制备氯化钯的流程如下:
、C)为原料制备氯化钯的流程如下: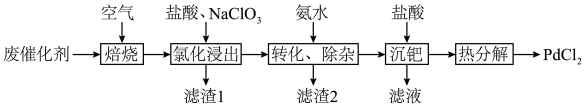
(1)“氯化浸出”前必须“焙烧”去除废催化剂表面积碳,原因是
(2)
 中Cl原子的杂化类型是
中Cl原子的杂化类型是(3)滤渣1主要成分为
 ,若要使溶液中
,若要使溶液中 不高于
不高于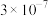 ,则应加入氨水使pH不低于
,则应加入氨水使pH不低于(4)工业上也可用
 还原
还原 制取海绵Pd,该历程对环境友好。该反应的化学方程式为
制取海绵Pd,该历程对环境友好。该反应的化学方程式为(5)工业上测定Pd含量的原理为:试样用硝酸及盐酸溶解后,加过量EDTA络合钯,用锌标准溶液滴定过剩的EDTA.具体步聚如下:
I.标定锌标准溶液对钯的滴定度:
a.吸取25mLEDTA溶液置于烧杯中,滴加4~5滴盐酸,加适量水,用锌标准溶液滴定至终点,消耗锌标准溶液
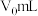 。
。b.吸取15mL含0.0010gPd的Pd标准溶液于烧杯中,加入25mLEDTA溶液,加适量水用锌标准溶液滴定至试液由黄色变成紫红色为终点,消耗锌标准溶液
 。
。Ⅱ.滴定式样:
称取0.1000g试样置于烧杯中,加适量硝酸及盐酸充分溶解并作妥善处理,加入25mLEDT溶液,用锌标准溶液滴定至终点,消耗锌标准溶液VmL。则试样中Pd的质量分数为
 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
名校
4 . 标准电极电位指离子有效浓度为1mol/L时相对标准氢电极的电极电位差值,电对的标准电极电势 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①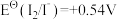 ;②
;②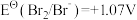 ;③
;③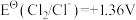 ;④
;④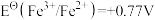 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是
 越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①
越高,其电对中氧化剂的氧化性越强。酸性介质中,以下电对的标准电极电势为:①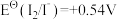 ;②
;②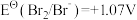 ;③
;③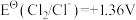 ;④
;④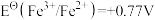 ;⑤
;⑤ ;⑥
;⑥ 。下列有关说法正确的是
。下列有关说法正确的是A.向1mol/L的HBr溶液中滴加 溶液,无明显现象发生 溶液,无明显现象发生 |
B.2mol/L的 与2mol/L的稀盐酸等体积混合有大量 与2mol/L的稀盐酸等体积混合有大量 产生 产生 |
C.在含 、 、 、 、 的混合溶液中若仅氧化 的混合溶液中若仅氧化 ,最佳的氧化剂是 ,最佳的氧化剂是 |
D.浓度相等时,还原性: |
您最近一年使用:0次
名校
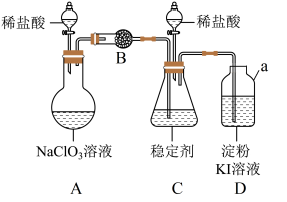
5 . 二氧化氯是一种生活中常用的消毒剂。实验室通过如下装置制备、研究二氧化氯。___________ 。
(2)常温下,装置A中生成两种气体产物,其一是 ,则装置A中发生反应的化学方程式为
,则装置A中发生反应的化学方程式为___________ 。
(3)为使 在装置C中被稳定剂充分吸收,装置A中滴加稀盐酸的速度宜
在装置C中被稳定剂充分吸收,装置A中滴加稀盐酸的速度宜___________ (填“较快”或“较慢”)。
(4) 在装置C中被完全吸收生成
在装置C中被完全吸收生成 ,此时装置D中溶液的颜色不变,则装置B的作用是
,此时装置D中溶液的颜色不变,则装置B的作用是___________ 。
(5)已知在酸性条件下 可发生反应生成
可发生反应生成 并释放出
并释放出 (不考虑其他副反应),
(不考虑其他副反应), 在装置C中完全吸收后,打开装置C中分液漏斗活塞,装置C中发生反应,则此时装置D的作用是
在装置C中完全吸收后,打开装置C中分液漏斗活塞,装置C中发生反应,则此时装置D的作用是___________ 。
(6)取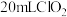 消毒过的自来水(密度为
消毒过的自来水(密度为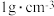 ,加稀硫酸酸化,加入
,加稀硫酸酸化,加入 过量
过量 溶液充分反应,再加2滴淀粉溶液,用
溶液充分反应,再加2滴淀粉溶液,用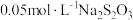 标准溶液滴定碘单质,达到滴定终点时消耗
标准溶液滴定碘单质,达到滴定终点时消耗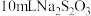 标准溶液(已知:
标准溶液(已知: )。
)。
①)该过程中 与
与 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
②达到滴定终点时现象是___________ ,原自来水中 的质量分数为
的质量分数为___________ 。
(2)常温下,装置A中生成两种气体产物,其一是
 ,则装置A中发生反应的化学方程式为
,则装置A中发生反应的化学方程式为(3)为使
 在装置C中被稳定剂充分吸收,装置A中滴加稀盐酸的速度宜
在装置C中被稳定剂充分吸收,装置A中滴加稀盐酸的速度宜(4)
 在装置C中被完全吸收生成
在装置C中被完全吸收生成 ,此时装置D中溶液的颜色不变,则装置B的作用是
,此时装置D中溶液的颜色不变,则装置B的作用是(5)已知在酸性条件下
 可发生反应生成
可发生反应生成 并释放出
并释放出 (不考虑其他副反应),
(不考虑其他副反应), 在装置C中完全吸收后,打开装置C中分液漏斗活塞,装置C中发生反应,则此时装置D的作用是
在装置C中完全吸收后,打开装置C中分液漏斗活塞,装置C中发生反应,则此时装置D的作用是(6)取
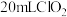 消毒过的自来水(密度为
消毒过的自来水(密度为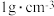 ,加稀硫酸酸化,加入
,加稀硫酸酸化,加入 过量
过量 溶液充分反应,再加2滴淀粉溶液,用
溶液充分反应,再加2滴淀粉溶液,用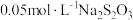 标准溶液滴定碘单质,达到滴定终点时消耗
标准溶液滴定碘单质,达到滴定终点时消耗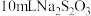 标准溶液(已知:
标准溶液(已知: )。
)。①)该过程中
 与
与 发生反应的离子方程式为
发生反应的离子方程式为②达到滴定终点时现象是
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
6 . 尿素(分子式 )水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
)水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
 )水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
)水溶液热解产生的NH3可去除尾气中的NOx,流程如下: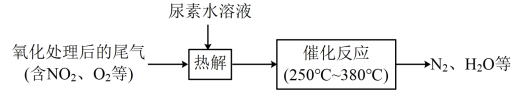
| A.尿素中氮元素的化合价为-3 |
B.“催化反应”过程中NH3还原NO2的化学方程式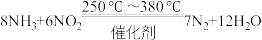 |
| C.若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。硫酸盐的产生是因为SO2被O2、H2O还原成H2SO4,再与NH3反应而得 |
D.“催化反应”过程中需控制温度在 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低 |
您最近一年使用:0次
名校
解题方法
7 . 已知反应: ,
, 为阿伏加德罗常数的值,若消耗
为阿伏加德罗常数的值,若消耗 ,下列叙述的错误的是
,下列叙述的错误的是
 ,
, 为阿伏加德罗常数的值,若消耗
为阿伏加德罗常数的值,若消耗 ,下列叙述的错误的是
,下列叙述的错误的是A.转移电子数为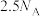 |
B.断裂的 键数为 键数为 |
| C.还原产物比氧化产物多0.5mol |
D.将生成物配制成1L水溶液,溶液中 |
您最近一年使用:0次
解题方法
8 . 用锰废料(含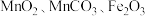 和少量
和少量 )制备
)制备 的工艺流程如下:
的工艺流程如下:
(1)流程中将锰废料粉碎的原因是_________ 。
(2)通入 时,
时, 发生还原反应,此时发生反应的化学方程式为
发生还原反应,此时发生反应的化学方程式为__________ ,能证明“吸收”后上层清液中没有 的试剂为
的试剂为_________ 。
(3)加入 的目的是将
的目的是将 氧化成
氧化成 ,写出“氧化”时的离子方程式
,写出“氧化”时的离子方程式________ ,所得“滤渣”的主要成分为_________ 。
(4)“化浆”操作中,________ (填“能”或“不能”)将稀硫酸换成稀盐酸;
(5)“转化”过程中,只有锰元素变价,则氧化剂与还原剂的物质的量之比为____ 。
(6)“系列操作”是过滤、洗涤、干燥,证明 洗涤干净的操作为
洗涤干净的操作为______ 。
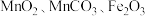 和少量
和少量 )制备
)制备 的工艺流程如下:
的工艺流程如下: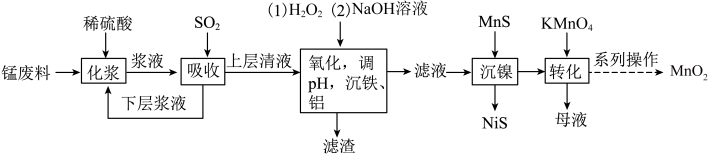
(1)流程中将锰废料粉碎的原因是
(2)通入
 时,
时, 发生还原反应,此时发生反应的化学方程式为
发生还原反应,此时发生反应的化学方程式为 的试剂为
的试剂为(3)加入
 的目的是将
的目的是将 氧化成
氧化成 ,写出“氧化”时的离子方程式
,写出“氧化”时的离子方程式(4)“化浆”操作中,
(5)“转化”过程中,只有锰元素变价,则氧化剂与还原剂的物质的量之比为
(6)“系列操作”是过滤、洗涤、干燥,证明
 洗涤干净的操作为
洗涤干净的操作为
您最近一年使用:0次
名校
解题方法
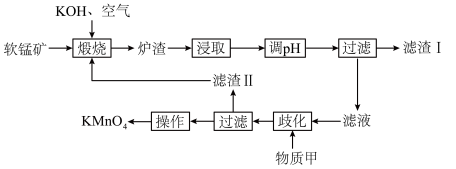
9 . 高锰酸钾为常见的强氧化剂,常用于消毒杀菌。工业上常以软锰矿(主要成分为MnO2,含少量Si、Al的氧化物)为原料制备,流程如下:
回答下列问题:
(1)基态Mn2+的价电子轨道表示式为___________ 。K2MnO4中Mn的化合价为___________ 。
(2)煅烧后,炉渣主要成分为K2MnO4,写出MnO2发生的化学方程式___________ 。
(3)浸取后通入CO2调节pH,则滤渣Ⅰ的主要成分为___________ 、___________ 。
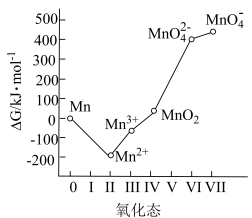
(4)流程中的“歧化”可加入的物质甲是___________(填字母)。
(5)歧化时发生的离子方程式为___________ 。
(6)实验室常用草酸标准溶液测定产品中高锰酸钾的纯度。取0.5000g样品溶于水,配成100mL溶液,取10.00mL于锥形瓶中,滴入5滴稀硫酸酸化,用0.1500mol/L草酸标准溶液滴定,达终点时消耗标准液5.100mL。
①滴定终点的现象为___________ 。
②样品中高锰酸钾(摩尔质量为158g·mol-1)的纯度为___________ %(结果保留小数点后两位)。
回答下列问题:
(1)基态Mn2+的价电子轨道表示式为
(2)煅烧后,炉渣主要成分为K2MnO4,写出MnO2发生的化学方程式
(3)浸取后通入CO2调节pH,则滤渣Ⅰ的主要成分为
(4)流程中的“歧化”可加入的物质甲是___________(填字母)。
| A.亚硫酸 | B.浓盐酸 | C.乙二酸 | D.稀硫酸 |
(5)歧化时发生的离子方程式为
(6)实验室常用草酸标准溶液测定产品中高锰酸钾的纯度。取0.5000g样品溶于水,配成100mL溶液,取10.00mL于锥形瓶中,滴入5滴稀硫酸酸化,用0.1500mol/L草酸标准溶液滴定,达终点时消耗标准液5.100mL。
①滴定终点的现象为
②样品中高锰酸钾(摩尔质量为158g·mol-1)的纯度为
您最近一年使用:0次
名校
解题方法
10 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体 ,回答下列问题:
,回答下列问题: 的溶解度数据表
的溶解度数据表
(1)仪器A右侧玻璃导管的作用为___________ ,仪器A中使用饱和食盐水代替蒸馏水的目的是___________ 。
(2)装置乙的作用是除杂,写出 被除去的离子方程式
被除去的离子方程式___________ 。
(3)在装置丙中已加入催化剂,请写出生成 的化学方程式
的化学方程式___________ ,研究表明当硝酸的质量分数超过 或温度高于
或温度高于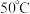 ,草酸的产率开始下降,其原因是
,草酸的产率开始下降,其原因是___________ 。
(4)装置丁的作用是___________ 。
(5)待反应结束后,从装置丙中分离出 晶体的操作为
晶体的操作为___________ 、___________ 、过滤、洗涤、低温干燥。
(6)草酸纯度的测定(杂质不与空气反应)
步骤1:称取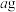 产品放置于管式炉中。
产品放置于管式炉中。
步骤2:将纯化后的空气 (已换算为标况)通入管式炉中与产品充分反应。
(已换算为标况)通入管式炉中与产品充分反应。
步骤3:测出混合气体中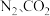 的体积分数分别为
的体积分数分别为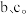
产品中草酸的质量分数为___________ ( 的摩尔质量为
的摩尔质量为 ,化为最简式)。
,化为最简式)。
 ,回答下列问题:
,回答下列问题:
 的溶解度数据表
的溶解度数据表温度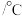 | 20 | 40 | 60 | 80 |
溶解度 | 9.52 | 21.5 | 44.3 | 84.5 |
(1)仪器A右侧玻璃导管的作用为
(2)装置乙的作用是除杂,写出
 被除去的离子方程式
被除去的离子方程式(3)在装置丙中已加入催化剂,请写出生成
 的化学方程式
的化学方程式 或温度高于
或温度高于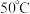 ,草酸的产率开始下降,其原因是
,草酸的产率开始下降,其原因是(4)装置丁的作用是
(5)待反应结束后,从装置丙中分离出
 晶体的操作为
晶体的操作为(6)草酸纯度的测定(杂质不与空气反应)
步骤1:称取
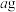 产品放置于管式炉中。
产品放置于管式炉中。步骤2:将纯化后的空气
 (已换算为标况)通入管式炉中与产品充分反应。
(已换算为标况)通入管式炉中与产品充分反应。步骤3:测出混合气体中
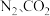 的体积分数分别为
的体积分数分别为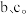
产品中草酸的质量分数为
 的摩尔质量为
的摩尔质量为 ,化为最简式)。
,化为最简式)。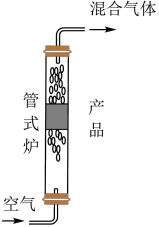
您最近一年使用:0次



